
Прогностическая оценка состояния
Коматозное состояние в течение 48 и более часов выступает предиктором плохого неврологического исхода. Если через 72 часа после остановки кровообращения неврологический дефицит составляет ≤ 5 баллов по шкале ком Глазго, в отсутствие двигательной реакции в ответ на болевое раздражение или зрачкового рефлекса, это является предиктором развития персистирующего вегетативного состояния у всех больных.
Также активно исследуются биохимические маркеры, позволяющие определить степень повреждения головного мозга, по аналогии с кардиоспецифическими ферментами при остром инфаркте миокарда. В основном исследуют уровень двух ферментов: нейронспецифической энолазы (NSE) и астроглиального протеина S-100.
Так, концентрация в плазме NSE более чем 22 мкг/л (80% чувствительность и 100% специфичность), определяемая в течение первой недели после перенесенной остановки кровообращения, ассоциируется с развитием персистирующей комы.
Уровень протеина S-100 более 0,7 мкг/л в первые 24 часа постреанимационного периода ассоциируется с плохим неврологическим исходом [12].
Современные принципы интенсивной терапии
Экстрацеребральный гомеостаз
После восстановления спонтанного кровообращения терапия постреанимационного периода должна строится на следующих принципах [13, 16]:
1. Поскольку происходит срыв ауторегуляции мозгового кровотока, его уровень становится зависимым от уровня среднего артериального давления. В первые 15–30 минут постреанимационного периода рекомендуется обеспечить гипертензию (САД < 150 мм рт.ст.), с последующим поддержанием нормотензии (как выраженная гипотензия, так и гипертензия должна быть корригированы).
В экспериментальных исследования было показано, что наличие гипертензии (САД 150–200 мм рт.ст.) в течение короткого периода (1–5 мин) в сравнении с группой нормотензии предупреждает после восстановления спонтанного кровообращения феномен no-reflow и коррелирует с улучшением неврологических исходов. Отмечено, что индукция кратковременной гипертензии более эффективно достигается титрованным введением адреналина или норадреналина, нежели мезатоном и дофамином.
2. Поддержание нормального уровня РаО2 и РаСО2.
3. Поддержание нормотермии тела. Риск плохого неврологического исхода повышается на каждый градус > 37 °С.
4. Поддержание нормогликемии (4,4–6,1 ммоль/л). Персистирующая гипергликемия ассоциирована с плохим неврологическим исходом. Пороговый уровень, при достижении которого необходимо начинать коррекцию инсулином, — 6,1–8,0 ммоль/л.
5. Уровень гематокрита в пределах 30–35 %. Проведение мягкой гемодилюции, обеспечивающей снижение вязкости крови, которая значительно повышается в микроциркуляторном русле вследствие ишемии.
6. Контроль судорожной активности введением бензодиазепинов.
В целом современная стратегия церебральной реанимации представлена на рис. 2.
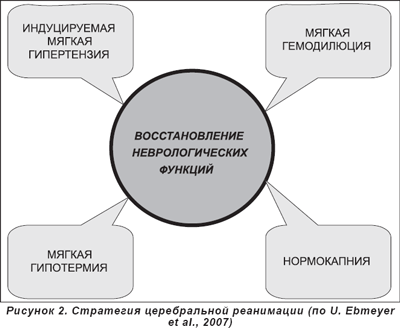
Интрацеребральный гомеостаз
1. Фармакологические методы. На данный момент отсутствуют, с точки зрения доказательной медицины, эффективные и безопасные методы фармакологического воздействия на головной мозг в постреанимационном периоде. Проведенные на нашей кафедре исследования позволили установить целесообразность применения перфторана в постреанимационном периоде. Перфторан уменьшает отек головного мозга, выраженность постреанимационной энцефалопатии и повышает активность коры мозга и подкорковых структур, способствуя быстрому выходу из коматозного состояния. Перфторан рекомендуется вводить внутривенно в первые 6 часов постреанимационного периода в дозе 5–7 мл/кг [6].
2. Физические методы. В настоящее время гипотермия является наиболее многообещающим методом нейропротекторной защиты головного мозга.
Повторное рождение терапевтической гипотермии (ТГ) связано с открытием в 1987 г. П. Сафаром и соавт. нейропротекторного эффекта мягкой гипотермии, которая является более безопасной, нежели умеренная гипотермия, использование которой лимитировалось рядом побочных эффектов (аритмогенность, коагулопатия, инфекции легких и пр.).
Точками приложения терапевтической гипотермии при ПРБ является целый ряд патофизиологических сдвигов в организме. Так, тяжесть ишемического повреждения в постреанимационном периоде увеличивается при повышении температуры тела на 0,5 °С или более 37 °С. При этом скорость образования свободных радикалов и реализация глутаматного каскада прямо пропорциональны уровню температуры в зоне ишемии. Гипертермия активирует NMDA-рецепторы, которые увеличивают уровень внутриклеточного Са2+, эффект свободнорадикального повреждения при индуцировании активации арахидоновой кислоты. Начальное нейрональное повреждение после ишемии и реперфузии является триггерным механизмом последующей хронической воспалительной реакции, реализуемой клетками микроглии, которая вызывает прогрессирующую нейродегенерацию.
Терапевтический эффект гипотермии обеспечивается реализацией следующих механизмов:
— сохранение пула АТФ и улучшение утилизации глюкозы тканью мозга;
— ингибирование деструктивных энзиматических реакций (на 1,5 % при снижении на 1 °С температуры тела);
— супрессия свободнорадикальных реакций и ингибирования аккумуляции продуктов липидной пероксидации;
— уменьшение внутриклеточной мобилизации Са2+;
— протекция пластичности липопротеинов цитоплазматических мембран;
— снижение потребления О2 в регионах головного мозга с низким кровотоком;
— снижение внутриклеточного лактат-ацидоза;
— ингибирование биосинтеза и продукции эксайтотоксичных нейротрансмиттеров;
— снижение нейтрофильной миграции в зонах ишемии;
— снижение риска развития цитотоксического и вазогенного отека головного мозга [9, 10, 17].
Выявлено, что снижение температуры тела на 1 °С в среднем уменьшает скорость церебрального метаболизма на 6–7 % [11].
Обеспечивается улучшение доставки О2 в ишемические зоны головного мозга, а также снижение внутричерепного давления.
Необходимо отметить, что в здоровом головном мозге применение анестетиков, вызывающих молчание электроэнцефалограммы, снижает скорость церебрального потребления О2 (CMRO2) только на 50 % за счет блокирования активного метаболизма. В то же время гипотермия уменьшает CMRO2 практически до нуля путем снижения базального метаболизма головного мозга. В частности, CMRO2 снижается на 7 % на каждый градус в диапазоне температур 38–28 °С, ингибируя активный метаболизм, при 28 °С — до 50 %, а при 18 °С — до 10 % (подавление базального метаболизма).
При проведении клинических исследований терапевтической гипотермии был выявлен ряд побочных эффектов:
— повышение вязкости крови (так, снижение температуры на 1 °С повышает гематокрит на 2 %);
— холодовой диурез (однако без нарушения функции почек);
— гипокалиемия;
— тромбоцитопения;
— пневмония;
— дрожь, повышение мышечного тонуса (что приводит к повышению потребления O2 тканями);
— снижение чувствительности к катехоламинам [9].
В 1997 г. S.A. Bernard et al. применили ТГ у больных с внегоспитальной остановкой кровообращения. ТГ (33 °С) была индуцирована у 22 больных в течение 12 ч наружным методом, в сравнении с группой нормотермии получено достоверное увеличение хорошего неврологического исхода (50 % против 13 %) при отсутствии осложнений.
В 2002 г. было проведено рандомизированное клиническое испытание при внегоспитальной остановке кровообращения ТГ у 43 больных (33 °С в течение 12 ч) в сравнении с 34 больными с нормотермией. В результате 49 % (21пациентов) в группе ТГ были выписаны из больницы с хорошим неврологическим исходом в сравнении с 26 % (9 человек) в группе контроля.
Было отмечено, что ТГ вызывает гемодинамические эффекты: снижение СВ и повышение общего периферического сопротивления сосудов, при этом число случаев возникновения аритмий было идентично в обеих группах, других осложнений отмечено не было.
В Европейское мультицентровое клиническое испытание (2002) с догоспитальной остановкой кровообращения было включено 273 больных, из них 136 больным индуцирована ТГ (33 °С в течение 24 часов). Через 6 месяцев отмечен хороший неврологический исход у 55 % в сравнении с 39 % при нормотермии. Число осложнений в группах было одинаковым. Однако было отмечено, что использование наружного охлаждения связано с низкой скоростью индукции ТГ — 0,3–0,9 °С в час и определенными техническими трудностями по подключению гипотерма, что приводило к задержке начала ТГ. При этом было показано, что чем раньше начата гипотермия, тем лучше неврологический исход. Последнее и стимулировало использование внутривенного метода индукции ТГ как более быстрой методики с более высокой скоростью охлаждения и более управляемой [9–11].
Согласно современным рекомендациям Европейского совета по реанимации 2005 года, пациентам без сознания, перенесшим остановку кровообращения во внебольничных условиях по механизму фибрилляции желудочков, необходимо обеспечить проведение гипотермии тела до 32–34 °С в течение 12–24 часов. Этот же режим гипотермии рекомендован пациентам с другими механизмами остановки, а также в случае внутрибольничных остановок кровообращения [16].
На рис. 3 представлен алгоритм интенсивной терапии постреанимационной болезни.
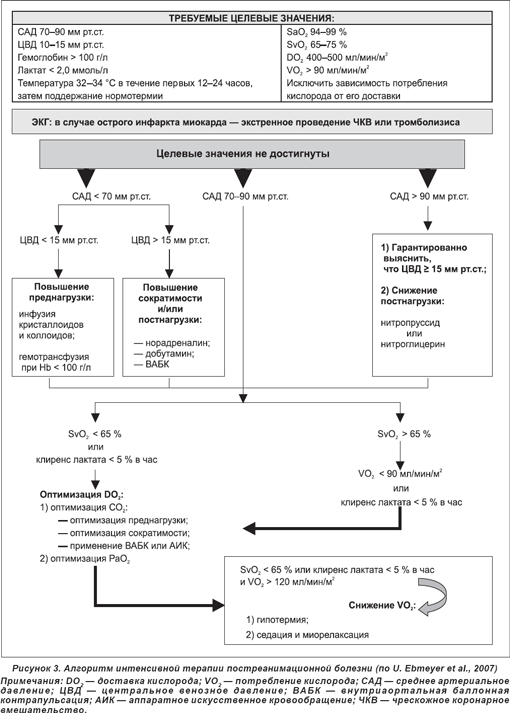
В заключение необходимо подчеркнуть, что неврологическое восстановление продолжает оставаться лимитирующим фактором СЛЦР, несмотря на почти 40-летний период научных изысканий, и пока делаются первые шаги на пути решения данной проблемы, что обусловлено крайней сложностью механизмов повреждения нейронов, запускаемых ишемией и реперфузией, мультифакторностью прир
