
- •Розділ і. Будова і властивості металів
- •1.1. Будова металів
- •1.2. Кристалізація металів
- •Розділ II. Сплави
- •2.1. Типи сплавів
- •2.2. Діаграми стану сплавів
- •2.3. Діаграма залізо-цементит
- •Розділ III. Залізовуглецеві сплави
- •3.1. Характеристика компонентів. Домішки
- •3.2. Класифікація сталей
- •3.3. Вуглецеві конструкційні сталі
- •3.5. Інструментальні сталі
- •3.6. Сталі спеціального призначення
- •3.7. Чавуни
Розділ III. Залізовуглецеві сплави
3.1. Характеристика компонентів. Домішки
Залізовуглецеві сплави — це сплави, отриманні методом розплаву заліза з вуглецем. До них відносяться сталь і чавун. Оскільки основними компонентами їх є залізо та вуглець, то спочатку розглянемо їх більш детально.
Залізо — це хімічний елемент з явно вираженими металічними властивостями. Воно добувається з надр землі, де знаходиться в рудах частіше всього в окислах Fe203. Воно має сріблясто-білий колір. Густина заліза 7,8 г/см3. Температура плавлення 1539 °С . Кристалічна решітка ОЦК. При зміні температури залізо має поліморфні перетворення, які позначаються Feα, Feγ, Feδ . Атомний номер заліза 26, атомна вага 55,85. Залізо — феромагнітний матеріал, але при температурі 768 °С (точка Кюрі) воно стає немагнітним. Найбільш чисте залізо, отримане в лабораторних умовах, має 99,9917% Fe. Залізо має невисоку твердість (80 НВ) і міцність (280 мн/м2).
Вуглець у природі зустрічається у двох модифікаціях: у формі алмазу із складною кубічною решіткою, та у формі графіту з простою гексагональною решіткою. Густина графіту 2,25 г/см3. При нагріванні до 3650 °С графіт починає сублімувати. Діаметр атома вуглецю — 0,154 нм.
Виходячи з типів комірок, розмірів атомів заліза та вуглецю, можна зробити висновок, що вуглець в α-залізі не розчиняється, а в γ-залізі розчиняється. Однак, експериментальна перевірка показує, що все-таки незначна кількість вуглецю розчиняється і в α-залізі. Пояснюється це наявністю в реальних решітках дефектів, особливо по границях зерен.
Основним конструкційним металічним матеріалом у промисловості є вуглецева сталь. Крім заліза і вуглецю в сталях є багато домішок. Вони можуть бути корисні та шкідливі, постійні та випадкові. Як вуглець, так і кожна з домішок впливають на властивості сталі. Особливо на властивості сталі впливає вуглець. Навіть при незначній зміні кількості вуглецю помітно змінюються властивості сталі. На рисунку 12 показана залежність між кількістю вуглецю і механічними та фізичними властивостями сталі.
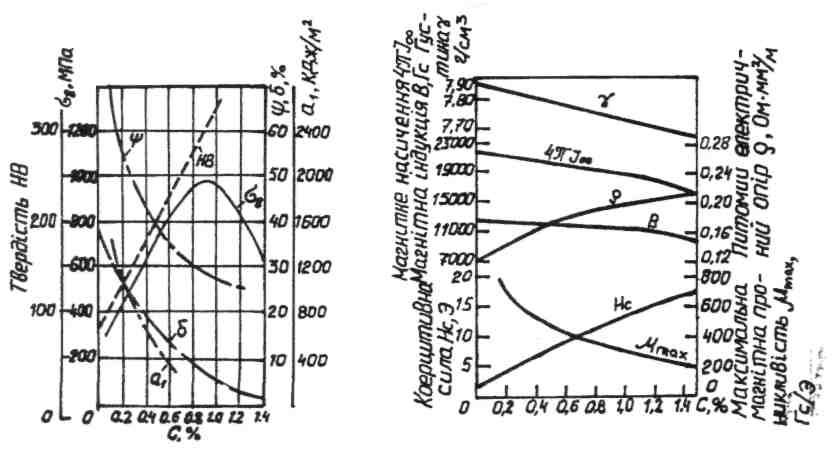
Рис. 12.
Постійними домішками в сталі є марганець, кремній, фосфор, сірка, а також гази: водень, азот та кисень.
Марганець суттєво впливає на властивості сталі, підвищує міцність, нейтралізує шкідливі з'єднання сірки тощо.
Кремній позитивно впливає на сталь. Його дія аналогічна до марганцю.
Фосфор є шкідливою домішкою в сталі. Розчиняючись у фериті, він різко підвищує температуру переходу в крихкий стан, викликаючи холодноломкість (синьоломкість) сталі.
Сірка, як і фосфор, потрапляє в метал із руд та разом з паливом. Вона теж шкідлива. Але не розчиняється в сталі. Сірка в будь-який кількості утворює із залізом сірчасті з'єднання — сульфіди заліза, які є евтектичними з температурою плавлення 988 °С і вище, тобто в районі температур червоного кольору. Тому це явище називають червоноломкі-стю. Це явище особливо небезпечне при обробці сталі тиском, тому що при гарячій обробці тиском у металі з'являється надриви та тріщини.
Уведення в сталь марганцю зменшує шкідливий вплив сірки. Марганець з'єднується з сіркою, утворюючи сульфід марганцю, який плавиться при температурі 1620 °С .
Кількість фосфору і сірки обмежують. Фосфору у сталі допускається не більше 0,05 %, а сірки — 0,03 %.
Водень, азот, кисень знаходяться в сталі в незначній кількості. їх кількість залежить від способу виробництва. У сталях вони знаходяться в раковинах, розчиняються у фериті, утворюють різні з'єднання (нітриди, оксиди). Наявність цих газів у металі приводить до шкідливих наслідків. Водень сприяє утворенню надривів (флокенів). Азот і кисень дуже впливають на зменшення в'язкості металу, зменшують ударну в'язкість.
