
- •4. Охорона навколишнього середовища і хімічна технологія
- •4. 1. Класифікація промислових забруднень біосфери
- •4.2. Основи промислової екології
- •4.3. Основні положення екології
- •4.4. Екологічні проблеми хімічної технології
- •4.5. Очищення промислових газових викидів
- •4.6. Утилізація твердих відходів
- •4.7. Очищення стічних вод хімічних виробництв
- •5. Виробництво сульфатної кислоти
- •5. 1. Основні властивості та застосування сульфатної кислоти
- •5.2. Методи виробництва сульфатної кислоти
- •5.3. Сировинна база сульфатнокислотного виробництва
- •5.4. Хімічна схема виробництва сульфатної кислоти з колчедану
- •5.5. Фізико–хімічне обґрунтування технологічних режимів стадій виробництва сульфатної кислоти
- •5.6. Технологічна схема виробництва сульфатної кислоти методом пкпа
- •5.7. Удосконалення сульфатнокислотного виробництва
- •6. Технологія аміаку і нітратної кислоти
- •6.2. Синтез аміаку
- •6.3. Способи виробництва аміаку з азоту повітря кон-тактним методом
- •6.4. Хімічна і принципова схеми виробництва аміаку
- •6.5. Фізико-хімічне обґрунтування режимів виробництва синтез− газу
- •6.6. Очищення природного і конвертованого газів
- •6.7.Фізико-хімічні основи синтезу аміаку
- •6.8. Технологічна схема синтезу аміаку під середнім тиском
- •6.9. Виробництво нітратної кислоти
- •6.9.1. Сорти і області застосування нітратної кислоти
- •6.9.2. Хімічна і функціональна схеми виробництва розведеної нітратної кислоти
- •6.10. Технологічна схема виробництва розведеної нітратної кислоти
- •6. 11. Виробництво концентрованої нітратної кислоти
- •6.11.1. Концентрування нітратної кислоти
- •6.11.2. Прямий синтез концентрованої нітратної кислоти
- •6.12. Охорона навколишнього середовища у виробництві нітратної кислоти
5. Виробництво сульфатної кислоти
5. 1. Основні властивості та застосування сульфатної кислоти
Безводна Н2SО4 (моногідрат)–важка, оліїста рідина з густиною 1,8305 г/см3 (за 20°С), кипить за 279,6 С і тиску 101325 Па, кристалізується за 10,37°С. При нагріванні вище 200°С безводна Н2SО4 частково розкладається за схемою:
Н2SО4![]() SО3
+ Н2О,
(5.1)
SО3
+ Н2О,
(5.1)
утворюючи азеотропну суміш, яка містить 98,3% Н2SО4 і 1,7% Н2О, і має температуру кипіння 338,8°С. Сульфатна кислота змішується з Н2О у будь-яких співвідношеннях, утворюючи гідрати (Н2SО4·Н2О; Н2SО4∙2Н2О; Н2SО4∙4Н2О) з виділенням великої кількості тепла (937,84 кДж/кг Н2SО4. З SО3 безводна сульфатна кислота утворює дві сполуки: Н2SО4∙SО3 і Н2SО4∙2SО3. Розчин SО3 у Н2SО 4 від 18 до 65% називають олеумом. На рис. 5.1. наведена діаграму кристалізації гідратів Н2SО4.
Для виробництва, транспортування і застосування Н2SО4 велике значення мають зміни температури плавлення і кипіння її залежно від концентрації. Як видно з діаграми, Н2SО4 з водою утворює кілька евтектичних сумішей. Суміш, що має найнижчу температуру кристалізації, містить 38% Н2SО4.
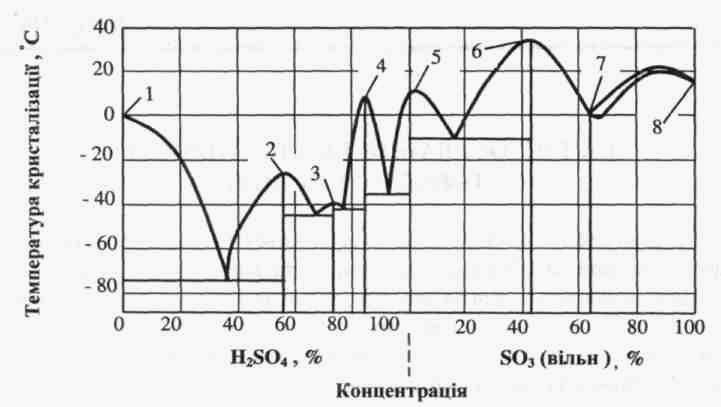
Рис. 5.1. Температура кристалізації розчинів сульфатної кислоти: 1 - Н2О; 2 -Н2SО4 4Н2О; 3-Н2SО4 2Н2О; 4 - Н2SО4 Н2О; 5-Н2SО4; 6-Н2SО4 SО3; 7-Н2SО4 2SО3; 8-SО3
Окремі види Н2SО4 за своїм складом близькі до таких евтектичних сумішей: 75%–ий розчин Н2SО4 (кристалізується при –41°С); 93,3%–а Н2SО4 (кристалізується при –37,85° С); олеум з вмістом 18,07% вільного SО3 (кристалізується при –17,05°С), а також неевтектична суміш 98%–ої Н2SО4 (кристалізується при +0,1°С). Розчини Н2SО4, що містять близько 70% Н2SО4, при нагріванні виділяють тільки водяну пару, а над олеумом, в якому понад 20% S03, практично знаходиться пара SО3.
Діаграму кипіння водних розчинів Н2SО4, наведену на рис. 5.2 використовують для визначення режиму концентрування розведеної Н2SО4.
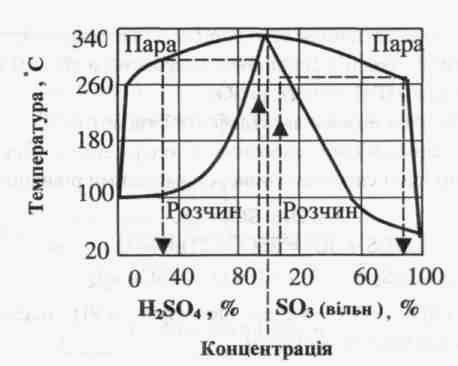
Рис. 5.2. Залежністъ темпера-тури кипіння сульфатної кислоти вiд її складу (діаграма фазової рівноваги між рідиною та парами) за атмосферного тиску
Як видно з діаграми, температура кипіння розчину, в якому міститься менш як 80% Н2SО4 лежить нижче 200°С. Під час нагрівання до пари переходить майже виключно вода. Якщо концентрація кислоти вища за 93%, у паровій фазі значно підвищується вміст Н2SО4. Пара Н2SО4 з підвищенням температури дисоціює за рівнянням (5.1), при температурах вищих за 400°С молекул SО3 у паровій фазі більше, ніж Н2SО4. При подальшому нагріванні відбувається дисоціація оксиду SО3, який за температури вищої за 1000°С дисоціює майже повністю.
Сульфатна кислота надзвичайно активна, вона дуже добре сполучається з водою, відбираючи її навіть від хімічних сполук. Рослинні і тваринні тканини, що містять у своєму складі вуглеводні (целюлозу, крохмаль, цукор), обвуглюються концентрованою Н2SО4. У розведеній Н2SО4 целюлоза і крохмаль перетворюються на цукор. На шкірі людини Н2SО4 викликає тяжкі опіки.
Переважна більшість Н2SО4 витрачається на виробництво мінеральних добрив. Майже усі інші кислоти і багато солей виробляються за участю Н2SО4; її широко використовують у виробництві кольорових і рідкісних металів; у металообробній промисловості. Н2SО4 та її солі застосовують для протравлення металевих виробів перед їх лудінням, нікелюванням, хромуванням або цинкуванням.
Значну кількість Н2SО4 використовують для очищення нафтопродуктів, у виробництві барвників, лаків, ліків, спиртів, ефірів, синтетичних миючих засобів, отрутохімікатів, вибухових речовин, пластичних мас та ін. Її застосовують у текстильній промисловості для протравлення тканин, для сульфування органічних сполук, у промисловості органічного синтезу, для виробництва іонообмінників, штучного волокна. Сульфатну кислоту застосовують у харчовій промисловості для виробництва крохмалю, патоки та інших продуктів, а також для сушіння газів, при концентруванні різних кислот.
Серед мінеральних кислот, які виробляються хімічною промисловістю, сульфатна кислота (СК) за об’ємом виробництва і споживанням займає перше місце. Пояснюється це і тим , що вона сама дешева з усіх кислот, а також її властивостями. СК не димить, у концентрованому вигляді не руйнує чорні метали, у той же час являється однією з самих сильних кислот, у широкому діапазоні температур (від –40 –20 до 260–336,5оС) знаходиться у рідкому стані. Галузі використання С. К. наведені на рис. 5.4.
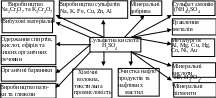
Рис. 5.4. Застосування сульфатної кислоти
Виробництво Н2SО4 в усьому світі весь час зростає. Відповідно до державних стандартів виробляється три сорти Н2SО4: технічна, акумуляторна і реактивна. Крім Н2SО4 виробляється також олеум («0 % вільного SО3, кристалізується при -110 С).
Технічна кислота завдяки домішкам має темний колір. За концентрації 92,50 С технічна кислота кристалізується при -350 С.
До акумуляторної кислоти ставляться високі вимоги відносно її чистоти. Нормуються вміст Mn, Fe, As, оксидів азоту, важких металів, нелеткого залишку та ін. Акумуляторну кислоту виробляють контактним методом, вона містить 92—94% Н2SО4.
Реактивну Н2SО4 виробляють трьох марок: хімічно чисту (х. ч.), чисту для аналізу (ч. д. a.) i чисту (ч.).
Як правило, її добувають у кварцовій або платиновій апаратурі контактним способом, вона містить 96-98% Н2SО4.
