
- •Фізична та колоїдна хімія
- •Техніка безпеки та правила роботи в хімічній лабораторії
- •Основні теоретичні відомості
- •Обладнання та реактиви
- •Порядок виконання роботи
- •Обробка експериментальних даних графічним методом
- •Обробка експериментальних даних аналітичним методом
- •Контрольні запитання
- •Лабораторна робота 17 Визначення середнього розміру частинок “білих” золів оптичними методами
- •Основні теоретичні відомості
- •Обладнання та реактиви
- •Порядок виконання роботи
- •Оформлення результатів досліджень
- •Контрольні запитання
- •Лабораторна робота 18 Визначення поверхневого натягу поверхнево-активних речовин сталагмометричним методом та параметрів адсорбційного процесу на границі поділу фаз рідина-газ
- •Основні теоретичні відомості
- •Обладнання та реактиви
- •Порядок виконання роботи
- •Обробка експериментальних даних
- •Контрольні запитання
- •Лабораторна робота 19 Визначення площі питомої поверхні адсорбента
- •Основні теоретичні відомості
- •Обладнання та реактиви
- •Порядок виконання роботи
- •Обробка експериментальних даних
- •Контрольні запитання
- •Лабораторна робота 20 Визначення теплоти змочування калориметричним методом
- •Основні теоретичні відомості
- •Обладнання та реактиви
- •Порядок виконання роботи
- •Обробка експериментальних даних
- •Контрольні запитання
- •Лабораторна робота 21 Досліджування в’язкості структурованих розчинів
- •Основні теоретичні відомості
- •Обладнання та реактиви
- •Порядок виконання роботи
- •Обробка експериментальних даних
- •Контрольні питання
- •Додатки
- •Список літератури
- •Фізична та колоїдна хімія
Обробка експериментальних даних
Визначивши у попередній роботі значення констант A і B у рівнянні Шишковського, поверхневий натяг води при температурі досліду σ0 та поверхневий натяг розчинів після адсорбції σ, рівноважні концентрації спирту розраховують за допомогою рівняння Шишковського (18.6), кмоль/м3:
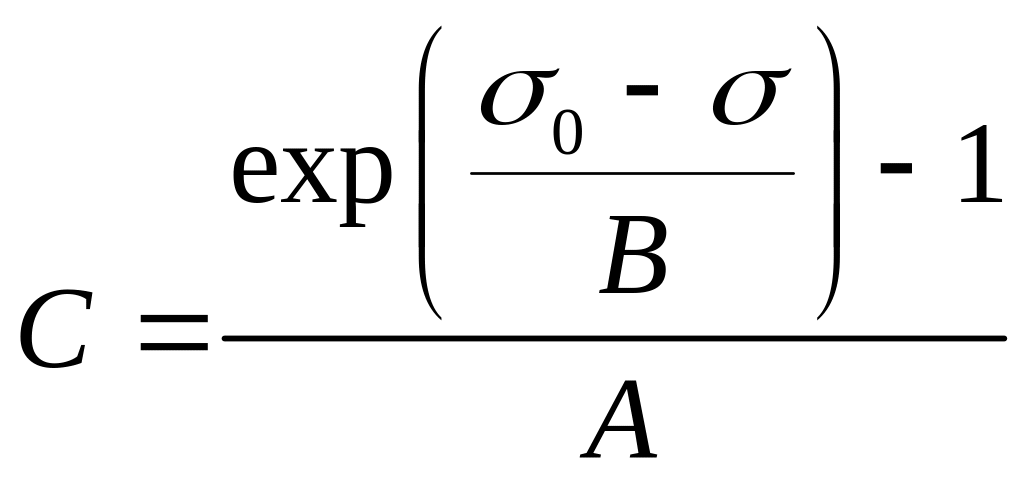 (19.3)
(19.3)
За відомими концентраціями розчинів до та після адсорбції, розраховують значення питомої адсорбції спирту:
![]() (19.4)
(19.4)
де х – кількість молів адсорбованого спирту; m – наважка вугілля; V – об’єм розчину спирту. Результати розрахунків записують в таблицю 19.3.
Таблиця 19.3
Експериментальні та розрахункові величини процесу адсорбції спирту на границі поділу фаз активоване вугілля-розчин
mсорбенту =……...кг; Vрозчину спирту = 25·10–6 м3 |
||||
Концентрація розчину, кмоль/м3 |
С0 – С, кмоль/м3 |
а, кмоль/кг |
С/а, кг/м3 |
|
Вихідна, С0 |
Рівноважна, С |
|||
|
|
|
|
|
Будують залежність С/а= f(C), знаходять граничне значення питомої адсорбції як котангенс кута нахилу прямої до осі абсцис (див. рис. 18.3) та згідно (19.1) розраховують площу питомої поверхні адсорбенту. Нагадуємо, значення S0 потрібно взяти з лабораторної роботи 18.
Контрольні запитання
Чим відрізняється адсорбція з розчинів від адсорбції газів і ПАР? Які рівняння використовують для описання цих процесів?
Дайте визначення площі питомої поверхні адсорбенту. Поясніть рівняння, за яким визначається ця величина.
Представте рівняння Ленгмюра у лінійній формі та визначте граничну адсорбцію.
Поясніть фізичний зміст констант у рівняннях Ленгмюра і Шишковського.
Лабораторна робота 20 Визначення теплоти змочування калориметричним методом
Мета роботи – визначення теплоти змочування та коефіцієнтів змочування поверхонь дисперсних порошків полярними і неполярними рідинами.
Основні теоретичні відомості
Такі поверхневі явища як змочування і розтікання мають велике практичне значення. Можливість їхнього передбачення й управління ними становить наукову основу багатьох виробничих процесів, зокрема, фарбування тканин, флотації, видалення забруднень сорбентами тощо. Ці явища відбуваються на границі поділу трьох фаз, роз'єднаних і в той же час зв'язаних трьома поверхневими шарами. Кожний з них характеризується власним значенням вільної поверхневої (або міжфазной) енергії . Співвідношення величин у такій системі визначає умови механічної рівноваги об'ємних фаз та поведінку рідини на поверхні твердого тіла.
Рідина на поверхні твердого тіла може розтікатися або збиратися у вигляді крапель різної форми. Умову самочинного розтікання краплі можна виразити нерівністю:
тг > тж, (20.1)
де тг і тр — міжфазні вільні енергії на границях тверде тіло – газ і тверде тіло – рідина відповідно. При цьому відбувається заміна поверхні з більшою вільною енергією на поверхню з меншою енергією, що приводить до зменшення запасу вільної енергії в системі; і, навпаки, при тг < тж — прагнення системи до мінімуму вільної енергії приводить до мимовільного зменшення площі контакту в процесі "стягування" краплі. У першому випадку відбувається змочування, а в другому — незмочування твердого тіла рідиною.
Мірою змочування поверхні рідиною є крайовий кут змочування θ, який утворює крапля з поверхнею твердого тіла. Крайовий кут змочування представляє собою кількісну характеристику змочування (θ – кут між твердою поверхнею і дотичною в точці дотику трьох фаз, який зчитується у бік рідкої фази). Чим менший крайовий кут, тим краще змочування поверхні рідиною.
Якщо крайовий кут змочування менший за 90º, то поверхня рідиною змочується і називається ліофільною поверхнею. Якщо крайовий кут більший за 90º, то поверхня рідиною не змочується і називається ліофобною поверхнею. Відповідно, тверді тіла, змочувані водою, називаються гідрофільними, а не змочувані – гідрофобними. Гідрофільними тілами є оксиди, карбонати, сульфати, солі кисневих кислот, скло; гідрофобними — сірка, графіт, сульфіди металів, полімерні матеріали.
Умови змочування поверхні рідиною визначає рівняння Юнга:
![]() (20.2)
(20.2)
З аналізу рівняння Юнга можна зробити висновок, що при тг тр, cos 0, < 90° і спостерігається змочування, а при тг тр, cos 0, 90° — незмочування.
Величини міжфазної енергії визначаються роботою молекулярних сил, двох типів: сили когезії (злипання) і сили адгезії (прилипання). Перші діють між молекулами усередині фази, другі — між молекулами, що перебувають у різних фазах. Робота сил адгезії Wa може бути обчислена за рівнянням Дюпре:
W = рг + тг – тр, (20.3)
або Юнга-Дюпре:
W=рг(1 + сos). (20.4)
Ці рівняння дозволяють обчислити роботу адгезії за відомим значенням рг і .
Про зміну характеру взаємодії твердої поверхні зі змочувальною рідиною в результаті адсорбції ПАР можна твердити, оцінюючи величину роботи змочування Wзм, що визначається як різниця між значеннями т-г і т-р. Для розрахунку використовують рівняння:
Wзм=ж-гcos (20.5)
Визначення крайового кута змочування для порошкоподібних тіл неможливе, тому характеристикою їх змочування є теплота змочування, яка представляє собою кількість теплоти, що виділяється при зануренні твердого тіла у рідину. Для порошкоподібних речовин теплоту змочування розраховують на 1 г речовини.
Теплота змочування завжди позитивна величина і дорівнює зменшенню поверхневої енергії твердого тіла при перенесенні його з повітря або з вакууму в рідину. Для гідрофільних тіл теплота змочування водою більша, ніж теплота змочування неполярними розчинниками, а для гідрофобних тіл — навпаки.
Характеристикою гідрофільності речовини може бути відношення теплот змочування водою Q1, та неполярною рідиною Q2:
β = Q1/Q2, (20.6)
яке називається коефіцієнтом змочування. Для гідрофільних тіл β > 1, для гідрофобних — β < 1.
