
Донбаський гірничо – металургійний інститут
Кафедра автоматизованих систем управління теплоенергетичними процесами
Методичні вказівки
до виконання лабораторних робіт за курсом
«Термодинаміка й теплотехніка»
(для студентів фаху 6.092501)
Затверджено на засіданні
кафедри АСУТП
Протокол № 1 от 18. 09. 2000
Рекомендовано
Методичною Советом ДГМИ
Протокол № 3 от 15. 12. 2000
Алчевськ 2001
УДК536.7
Методичні вказівки до самостійної роботи студентів за курсом «Термодинаміка й теплотехніка» (для студентів фаху 6. 092501) / Укл. В.П.Алексєєв - Алчевськ: ДГМІ, 2000. - 11с.
Містить рекомендації й розрахункові формули, які необхідні при виконанні домашніх завдань по відповідних поділах технічної термодинаміки й теорії теплообміну.
Укладач В.П.Алексєєв, доц.
Відп. за випуск В.І.Жиляков, доц.
Відп. редактор І.Д.Регішевська, ст.викл.
Методичні вказівки призначені для студентів фаху 6. 092501 (Автоматизація і комп'ютерно-інтегрировані технології) для самостійної роботи студентів за курсом «Термодинаміка і теплотехніка». Відповідно до навчального плану курс «Термодинаміка і теплотехніка» студент вивчає на другому курсі в третьому семестрі. На самостійну роботу приділяється 3 часу в тиждень. Ці часи приділяються для проробки лекційного матеріалу, підготуванню до лабораторних робіт і практичних занять, а також для самостійного виконання домашніх завдань.. Розподіл часів відповідно: підготування лекційного матеріалу • 1,5 часу; підготування до лабораторних робіт - 0,5 часу; до практичних занять - 0,5 часу і виконання домашніх завдань - 0,5 часу.
Перелік поділів курсу, а також перелік контрольних питань, котрі студенти повинні вивчити при підготуванні до лабораторних і практичних занять приводяться в методичних указівках до виконання лабораторних і практичних занять.
Протягом семестру студенти виконують чотири домашніх завдання (задача по різноманітних поділах курсу).
Домашнє завдання 1
Перед виконанням ДЗ 1 необхідно проробити відповідні поділи по конспекту лекцій і літературі що рекомендується. Для виконання ДЗ 1 необхідно вивчити і знати такі питання: термодинамічні параметри стану ідеальних газів, перший закон термодинаміки, теплоємність газів і термодинамічні процеси зміни стану ідеальних газів.
Приклад виконання ДЗ 1
Газ-повітря з початковою температурою t1 стискується в одноступінчатому поршневому компресорі від тиску Р1 до Р2. Стиск відбувається по ізотермі, адіабаті і політропі з показником політропи n. Визначити для кожного з трьох процесів стиску кінцеву температуру газу t 2, відведену теплість Q (кВт), і теоретичну потужність компресора, якщо його продуктивність G. Дати зведену таблицю і зображення процесів стиску в РV і ТS - діаграмах. Розрахунок звістки без урахування залежності теплоємності від температури.
Рішення
Приймаючи склад повітря 21% О2 і 79% N2 i рахуючи його ідеальним газом визначний молекулярну масу повітря і газову постійну.
О![]() б'ємна
частка кисню
б'ємна
частка кисню
об'ємна частка азоту
Молекулярна маса (для газової суміші)
![]()
![]()
lе µо2 і µN2 - молекулярна маса відповідно кисню й азоту (32 і 28).
Газова постійна

Початковий питомий обсяг визначаємо з рівняння стану для 1 кг ідеального газу (рівняння Клапейрона).
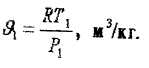
![]()
1. Роздивимося ізотермічний стиск.
Ізотермічний процес протікає при постійній температурі Т= const, тому
T2 = T1.
Кількість відведеної теплості для ізотермічного процесу визначаємо по формулі
кВт
де G - продуктивність компресора в кг/ч;
Розмірності тисків Р і і Р2 у кПа(кН/м2).
Тому що в ізотермічному процесі уся витрачена робота на стиск у компресорі приділяється у виді теплісті, то теоретична потужність дорівнює
кВт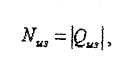
2. Роздивимося адіабатний стиск.
Адіабатним називається процес, що протікає без теплообміну з навколишнім середовищем (тобто до системи теплість не підводиться і не відділяється від неї)
![]()
Рахуючи повітря двохатомним ідеальним газом визначний показник адіабати к (без урахування залежності його від температури). Ізобарна і ізохорна мольна теплоємність для 2х атомних ідеальних газів відповідно рівні (див.табл.6-1 [1]).

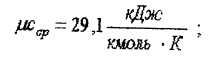
![]()
Кінцеву температуру визначимо зі співвідношення між основними термодинамічними параметрами для адіабатного процесу

Кількість відведеної теплості дорівнює нулю.
Теоретична потужність компресора дорівнює
![]()
де m - секундна масова продуктивність компресора, кг/с;
Іад - питома робота на привід компресора, кДж/кг.

де R – в кДж/(кгК).
