
- •170034, Г. Тверь, пр. Чайковского, д. 9, оф. 504,
- •Список сокращений
- •Характеристика системы гемостаза
- •Морфологические компоненты системы гемостаза:
- •Сосудистая стенка
- •Эндотелий
- •Продукты эндотелиоцитов, участвующие в гемостазе
- •Контроль активности тромбоцитов
- •Тромбомодулин
- •Прокоагулянтная роль эндотелия, регуляция сосудистого тонуса
- •Роль эндотелия в регуляции сосудистого тонуса
- •Сосудистая стенка
- •Тканевой фактор
- •Коллаген
- •Тромбоциты
- •Рецепторы мембраны тромбоцитов
- •Рецепторы для высокомолекулярных белков
- •Интегрины
- •Фактор роста тромбоцитов (pdgf)
- •Фактор XIII
- •Адгезия тромбоцитов
- •Тромбоциты
- •Активация тромбоцитов
- •Агрегация тромбоцитов
- •Ретракция сгустка крови
- •Участие моноцитов в свертывании крови
- •Плазменные белки гемостаза
- •1) Многоступенчатый этап, приводящий к акти вации протромбина и превращению его в ак тивный фермент - тромбин;
- •Роль кофакторов и микроокружения в процессе свертывания крови
- •Роль кальция в гемостатических реакциях
- •Ингибиторы ферментов системы гемостаза
- •Антитромбин и гепарин
- •Протеин s
- •Система фибринолиза
- •Активатор плазминогена тканевого типа
- •Внутренний путь активации фибринолиза
- •Внешний путь активации фибринолиза
- •Ингибиторы тканевого активатора плазминогена (pai)
- •Активируемый тромбином ингибитор фибринолиза (tafi)
- •Другие элементы системы фибринолиза
- •Реологические аспекты гемостаза
- •Функция тромбоцитов в различных гемодинамических условиях
- •Современная теория свертывания крови
- •Особенности физиологии и исследования гемостаза у плодов, новорожденных и детей раннего возраста
- •Тромбоциты
- •О собенности физиологии и исследования гемостаза у женщин при менструации и беременности
- •Клинический пример 1
- •Обеспечение диагностики нарушении гемостаза в
- •Подбор антикоагулянтов
- •Динамический анализ функции тромбоцитов
- •2 Агонистов (индукторов агрегации) возможно селективное выделение аспириновых тромбоцитопа-тий. По типу измерения pfa-100 является динамическим агрегометром.
- •Тромбоцитокрит (рст)
- •Агрегация тромбоцитов
- •Клинический пример 2
- •Исследования агрегации тромбоцитов в образцах цельной крови
- •Молекулярно-биологические методы
- •Коагуляционные методы
- •Ручные методы
- •Автоматизированные коагулометры
- •Оптико-механические коагулометры
- •Турбидиметрические коагулометры
- •Нефелометрические коагулометры
- •Преимущества и недостатки различных методов обнаружения сгустка
- •Иммунохимические методы
- •Скрининговые тесты оценки плазменного звена гемостаза
- •Диагностическое значение ачтв
- •Использование ачтв для выявления волчаночного антикоагулянта
- •Контроль лечения гирудином
- •Скрининговый тест на основе ачтв для оценки антикоагулянтной активности протеина с
- •Протромбиновое время
- •3) Протромбиновое отношение (по), которое определяется как
- •Тканевые тромбопластины
- •Протромбиновый тест (пт) по Квику
- •0,5 Г/л (врожденная или приобретенная гипо/
- •Рептилазное время (батроксобиновое время)
- •Турбидиметрический метод
- •Интерпретация результатов
- •Определение фактора Виллебранда (vWf)
- •Определение фактора VII с использованием хромогенного субстрата
- •Определение протромбина (фактора II) с использованием хромогенного субстрата
- •Определение фактора XIII
- •Преаналитические факторы, влияющие на результаты определения гепарина
- •Определение протеина с
- •Определение протеина s
- •Определение антитромбина
- •Тесты аля исслелования фибринолитической системы
- •Определение α2-антиплазмина
- •Опрелеление ингибитора активатора плазминогена типа 1 (pai-1)
- •Паракоагуляционные тесты
- •Стандарты воз
- •Внутрилабораторный контроль качества
- •Патология гемостаза
- •Без правильных современных лабораторных исследований невозможно лечение и профилактика нарушений гемостаза.
- •Гемофилия а
- •Коагулограмма при гемофилии а
- •Исследование восстановления фактора VIII в крови
- •Клинический пример 3
- •500 Me 1 раз в 2 дня. Исследование коагулог-раммы через год показало отсутствие ингибитора к ф.VIII у пациента.
- •Клинический пример 4
- •Патология гемостаза
- •VWf:Ag - антиген фактора Виллебранда, vWf:rCo - коллаген-связывающая активность фактора Виллебранда, ф.VIII - фактор коагуляции VIII, а-д - аутосомно-доминантное, а-р - аутосомно-рецессивное.
- •Клинический пример 5
- •Клинический пример 6
- •Иммунная тромбоцитопеническая пурпура (итп)
- •Клинический пример 7
- •3 Недель.
- •Приобретенный ингибитор к фактору VIII (приобретенная гемофилия а)
- •Клинический пример 8
- •Приобретенный ингибитор к фактору V
- •Приобретенные ингибиторы к протромбину, факторам VII и X
- •Приобретенные ингибиторы к фибриногену, фибрину, ф.Хiii и промежуточным продуктам
- •Приобретенный дефицит витамина к
- •Лечение антикоагулянтами непрямого действия, отравление антагонистами витамина к
- •Клинический пример 9
- •Лабораторные тесты при тромбофилии
- •Клинический пример 10
- •Дефицит протеина с
- •Клинический пример 11
- •Дефицит протеина s
- •Мутация протромбина 20210а
- •Дефицит антитромбина
- •Гипергомоцистеинемия
- •Клинический пример 12
- •Высокая активность фактора VIII и фактора Виллебранда
- •Дисфибриногенемия
- •Антифосфолипидный синдром и волчаночный антикоагулянт
- •Клинический пример 14
- •110%, Ачтв 45,9 с (норма 28-40 с), активность ф.Iх 68%, ф.Хi 80%, ф.Хii 96%, ф.VIII 120%, скринин-говый тест на волчаночный антикоагулянт положительный.
- •Клинический пример 15
- •Клинический пример 16
- •Фибринолитическая терапия
- •Этиология и патогенез двс
- •Виды двс-синдрома
- •Тромбоцитарно-сосудистый гемостаз при двс-синдроме
- •Плазменный гемостаз при двс-синдроме
- •И фазы двс-синдрома
- •Клинический пример 18
- •Наиболее значимые факторы патологического тромбообразования у детей первого полугодия жизни
- •Приложение
- •Новорожденных в первые 6 месяцев жизни
- •В течение первых 6 месяцев жизни
- •У детей первых 6 месяцев жизни
- •По сравнению с взрослыми
- •По сравнению с взрослыми
- •Обеспечение качества лабораторной
- •Вторичные комплексные нарушения
Исследование восстановления фактора VIII в крови
Известно, что активность ф.VIII в крови после введения концентратов в дозе 1 МЕ/кг веса по-
вышается в 1,5-2 раза, а период полувыведения составляет около 12 часов. Однако возможны значительные индивидуальные колебания этих показателей. Проведение теста восстановления активности ф.VIII включает определение его активности в плазме, собранной непосредственно перед введением известной дозы фактора, и через определенные интервалы. Имеются разные методики проведения теста. Если есть возможность, необходимо определить активность через 15 мин, 6, 12, 24 и 48 часов после введения препарата. Доза вводимого препарата должна быть не менее 25 МЕ/кг, но желательно не более 50 МЕ/кг. На основании полученных результатов можно построить график, по которому в дальнейшем удобно вычислять ожидаемую активность препарата. Тест восстановления необходимо проводить неоднократно на протяжении жизни пациента, поскольку активность метаболизма факторов и соотношение объема плазмы и веса тела меняются по мере роста и взросления ребенка. Важно помнить, что тест восстановления необходимо проводить в период, когда нет значимых геморрагических проявлений, чтобы на его результаты не оказывало влияние потребление фактора из-за кровотечения.
Таблица 40
Данные для определения активности ингибитора фактора VIII по методу Бетезда

Клинический пример 3
Больной, возраст 2,5 года. Страдает гемофилией А тяжелой формы, ф.VIII:С 0,8%, получал гемостатическую терапию по требованию концентратом фактора VIII в дозе 250 ME на введение. В возрасте 1 года после травмы слизистой полости рта началось кровотечение. После двукратного введения 500 ME концентрата фактора VIII с интервалом в 3 часа кровотечение не прекратилось. Проведено исследование коагулог-раммы. ПТ 120%, АЧТВ 120 с (норма 28-43 с),
ф.VIII <0,5%, ф.IХ 95%, ф.ХI 105%, ф.ХII 73%. АЧТВ после смешивания 1:1с нормальной плазмой (активность ф.VIII 100%) 89 с. Предположили наличие специфического ингибитора к ф.VIII. Исследование ингибитора по методу Бетезда показало, что его титр равен 2,5 БЕ. Проведено лечение концентратом фактора VIII в дозе 200 МЕ/кг ежедневно в течение 4 дней. Кровотечение остановилось после первого введения. В дальнейшем начата профилактика концентратом ф.VIII в дозе 2000 ME 1 раз в 2 дня. Исследование ингиби-
Патология гемостаза
тора через 6 месяцев показало его следовую активность, пациент был переведен на профилактическое лечение концентратом ф.VIII в дозе
500 Me 1 раз в 2 дня. Исследование коагулог-раммы через год показало отсутствие ингибитора к ф.VIII у пациента.
Таблица
41
Изменения
лабораторных показателей при гемофилии
В
Гемофилия В
Гемофилия В - геморрагическая коагулопа-тия, возникающая вследствие снижения активности фактора IX. Частота встречаемости приблизительно 1 на 30 000 мальчиков. Заболевание сцеплено с полом, клинически сходно с гемофилией А. Классификация по тяжести аналогична классификации гемофилии А, основана на определении активности фактора IX в крови: тяжелая форма - ГХа <1%, среднетяже-лая - 1-5%, легкая форма - >5-30%. Встречаются врожденные и приобретенные формы. Причина меньшей частоты врожденных и приобретенных форм этого заболевания, возможно, кроется в меньшем размере гена и молекулы ф.IХ, чем гена и молекулы ф. VIII По этой же причине, вероятно, частота развития ингибитор-ных форм гемофилии В также значительно меньше, чем при гемофилии А.
В настоящее время для лечения гемофилии В применяются свежезамороженная плазма, крио-супернатант (концентрат нативной плазмы), различные препараты концентрированного фактора IX. Осложнения лечения гемофилии В сходны с осложнениями лечения гемофилии А.
В табл. 41 представлены изменения основных коагулологических тестов у больных гемофилией В. Следует помнить, что при легких формах гемофилии В может не быть удлинения АЧТВ. При тяжелой и умеренной степени дефицита ф.IХ имеет место удлинение АЧТВ, однако результат во многом зависит от коммерческого набора реактивов. При наличии клинических проявлений легкой гемофилии необходимо исследовать активность ф.VIII и ф.IХ.
Исследования активности ингибитора и теста восстановления проводятся по схеме, аналогичной схеме у больных гемофилией А. Однако при проведении теста восстановления необходимо учитывать более длительный период полувыведения. Соответственно взятие материала будет проводиться по схеме: до введения, через 15-30 минут после введения, через 12, 24, 48 и 72 часа.
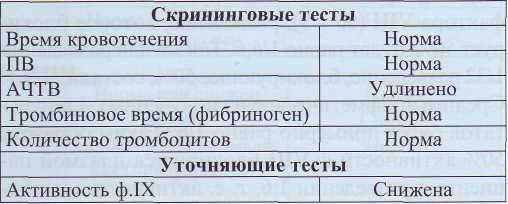
Дефицит фактора XI
Дефицит фактора XI (ранее заболевание определялось как гемофилия С) - геморрагическое заболевание, возникающее из-за дефекта гена фактора XI. Дефицит фактора XI передается как аутосомно-рецессивный признак. Это заболевание достаточно часто встречается в популяции евреев-ашкенази, среди которых гомозиготное носительство составляет от 0,1 до 0,3%, а гетерозиготное - от 5,5 до 11%. В других группах людей описаны лишь спорадические случаи. Клинически дефицит ф.ХI значительно отличается от гемофилии А и В, вследствие этого термин «гемофилия С» исключен из классификации. У больных с гомозиготной формой заболевания активность ф.ХI в крови составляет от 0 до 15%, у гетерозиготных носителей - от 25 до 70%о.
При дефиците ф.ХI имеется умеренно выраженный геморрагический синдром в виде большого количества кожных геморрагических элементов, носовых, маточных кровотечений, длительных кровотечений после хирургических вмешательств, кровотечений после удаления зуба или тонзиллэктомии. В каждом конкретном случае трудно предсказать, как больной среагирует на хирургическое вмешательство. Тяжесть геморрагического синдрома может не коррелировать с активностью ф.ХI в крови. Клинические проявления возникают при остаточной активности ф.ХI менее 30%, однако возможны минимальные
Патология гемостаза
проявления у гетерозиготных носителей с активностью ф.ХI между 50 и 70%.
Лечение. Для лечения геморрагических проявлений при дефиците ф.ХI используется свежезамороженная плазма. Разработаны и концентрированные очищенные препараты ф.ХI, которые применяются в некоторых странах.
Лабораторная диагностика дефицита ф.ХI основана на проведении стандартных тестов ко-агулограммы и на определении активности ф.ХI в плазме (табл. 42).
Таблица 42
Изменения лабораторных показателей при дефиците ф.Х1
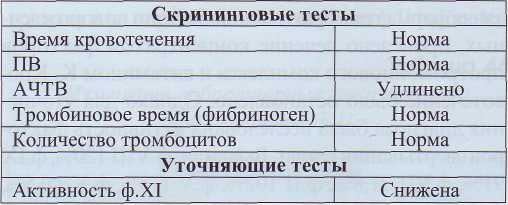
Врожденный дефицит фактора VII (гипопроконвертинемия)
Геморрагическое заболевание, возникающее вследствие дефицита активности ф.VII в плазме (гипопроконвертинемия), передается как аутосомно-рецессивный признак. Литературных данных о распространенности этого заболевания практически нет, что, вероятно, связано с отсутствием клинических проявлений у многих пациентов с уровнем активности ф.VII выше 5%. При тяжелой форме с активностью ф.VII ниже 3% геморрагический синдром похож на проявления у больных тяжелой формой гемофилии А, включая эпизоды гемартрозов. Первые проявления могут возникать сразу после рождения: кровотечения из пупочного канатика, пупочной ранки, кефалогематомы, внутричерепные гематомы. В дальнейшем характерны кожные геморрагические проявления в виде множественных гематом и экхимозов, носовые, маточные кровотечения, длительные кровотечения после травм и хирургических процедур. Реже встречаются гематомы мягких тканей. Тяжесть геморрагических проявлений коррели-
рует с активностью ф.VII. С целью коррекции гемостаза при дефиците ф.VII может вводиться свежезамороженная плазма, концентраты факторов протромбинового комплекса. Имеется очищенный концентрат ф.VII.
Лабораторная диагностика дефицита ф.VII основана на изменении стандартных тестов коа-гулограммы и на определении активности ф.VII (табл. 43).
Таблица 43
Изменения лабораторных показателей при дефиците ф. VII
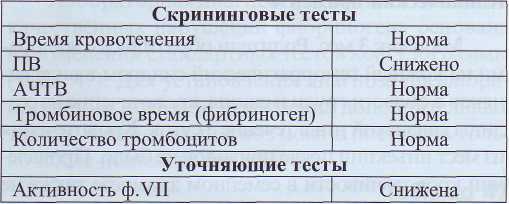
Дефицит фактора X (болезнь Стюарта-Прауэра)
Болезнь Стюарта-Прауэра - редкое геморрагическое заболевание, вызванное дефицитом активности ф.Х. Имеются немногочисленные литературные описания этого заболевания. Болезнь Стюарта-Прауэра передается как аутосомно-рецессивный признак. Наследственный дефицит ф.Х встречается в популяциях с частыми родственными браками. Клинические проявления имеются в основном у гомозиготных носителей, у которых активность ф.Х составляет около 1%. Реже у гомозигот может быть активность до 25%. Тяжесть заболевания коррелирует с активностью ф.Х в крови. При тяжелой форме заболевания проявления сходны с таковыми при тяжелой гемофилии: гемартрозы, гематомы мягких тканей, кровотечения из ран слизистых, тяжелые послеоперационные кровотечения. Очень характерны для тяжелого врожденного дефицита ф.Х внутричерепные кровоизлияния сразу после рождения и на первом году жизни, когда диагноз еще неизвестен. Часто эти эпизоды заканчиваются гибелью ребенка.
Геморрагические проявления при болезни Стюарта-Прауэра купируются применением све-
>•--■ •••■•:..;:,..,•'
Патология гемостаза
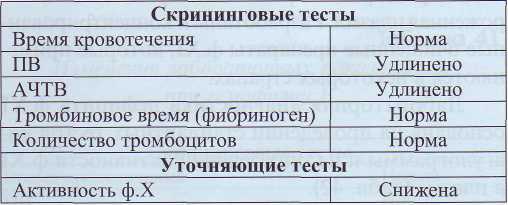
Лабораторная диагностика дефицита ф.Х основана на изменении стандартных тестов ко-агулограммы и определении активности ф.Х (табл. 44).
Таблица 44
Изменения лабораторных показателей при дефиците ф.Х
