
- •Часть 1
- •Раздел 3.2 .Модель идеального вытеснения. 40
- •Раздел 3.4. Диффузионная модель 47
- •Раздел 5. Синтез моделей технологических объектов на базе их гидродинамических моделей и уравнений химической кинетики. 124
- •1. Введение. Основные понятия систем
- •1.1.Очень большая система
- •1.2.Общая структура сложных объектов систем и основные этапы моделирования.
- •1.2.1.Формализованное описание.
- •1.2.2.Математическое описание.
- •1.2.3.Моделирующий алгоритм.
- •2. Общие принципы и этапы построения математических моделей систем.
- •2.1. Структурный анализ и структурный синтез сложных технологических систем
- •2.2. Обобщенная структурная модель металлургического процесса.
- •3. Модели структуры потоков для технологических объектов.
- •3.1 Модель идеального перемешивания.
- •Применение преобразования Лапласа для анализа математических моделей.
- •Раздел 3.2 .Модель идеального вытеснения.
- •3.3. Ячеечная модель аппарата
- •Раздел 3.4. Диффузионная модель
- •Стационарный метод определения критерия Пекле.
- •3.5.Комбинированные модели
- •3.5.1.Модель с застойной зоной
- •3.5.2.Модель с байпасным потоком.
- •3.5.3.Последовательное соединение ячеек идеального вытеснения и идеального смешения.
- •3.5.4.Гидродинамические модели многофазных потоков.
- •3.6.Методы определения параметров моделей структуры потоков.
- •3.6.1. Характеристики кривых отклика аппаратов на возмущения с помощью моментов.
- •3.6.2. Связь передаточных функций с моментами кривых
- •3.6.3.Ячеечная модель
- •3.6.4.Диффузионная однопараметрическая модель
- •3.6.5.Вычисление моментов по экспериментальным данным.
- •3.6.6.Определение параметров гидродинамических моделей по экспериментальным данным путем решения обратной задачи методами нелинейного программирования.
- •4. Кинетические модели для описания химических превращений.
- •4.1.Основные закономерности химической кинетики
- •4.2. Методы определения параметров кинетических моделей.
- •4.2.1.Определение констант скорости параллельных реакций:
- •4.3.Определение кинетических констант сложных реакций методами нелинейного программирования.
- •4.4. Кинетика гетерогенных процессов.
- •4.4.1 Типы гетерогенных процессов
- •4.4.2.Основные стадии гетерогенных процессов.
- •4.4.3.Определение области протекания гетерогенного процесса.
- •Влияние формы межфазной поверхности раздела фаз на скорость гетерогенных процессов.
- •Раздел 5. Синтез моделей технологических объектов на базе их гидродинамических моделей и уравнений химической кинетики.
- •5.1. Модель идеального смешения
- •5.2.Модель идеального вытеснения:
- •5.3. Диффузионная модель
- •Литература
4.4.3.Определение области протекания гетерогенного процесса.
Область
гетерогенного процесса можно определить
по зависимости эффективной скорости
процесса
![]() от
условий протекания процесса.
от
условий протекания процесса.
По зависимости наблюдаемой скорости процесс от относительной скорости движении фаз.
Если
наблюдаемая скорость процесс зависит
от скорости движения фаз, то общая
скорость процесса контролируется
скоростью массопереноса. Это означает,
что
![]() и
процесс происходит в диффузионной
области, так как скорость массопередачи
увеличивается при увеличении скорости
обтекания твердой фазы, за счет уменьшения
толщины диффузионного пограничного
слоя, в соответствии с уравнениями,
вытекающими из 1-гозакона Фика. Лимитирующей
стадией процесса при протекании процесса
в диффузионной области является скорость
диффузии через неподвижный диффузионный
слой на поверхности раздела фаз:
и
процесс происходит в диффузионной
области, так как скорость массопередачи
увеличивается при увеличении скорости
обтекания твердой фазы, за счет уменьшения
толщины диффузионного пограничного
слоя, в соответствии с уравнениями,
вытекающими из 1-гозакона Фика. Лимитирующей
стадией процесса при протекании процесса
в диффузионной области является скорость
диффузии через неподвижный диффузионный
слой на поверхности раздела фаз:
 (4.4.8)
(4.4.8)
Где
![]() -
толщины диффузионного пограничного
слоя, которая зависит от скорости
обтекания.
-
толщины диффузионного пограничного
слоя, которая зависит от скорости
обтекания.
Например, на рис. Показано влияние скорости перемешиваниия на скорость растворения цинка в кислоте
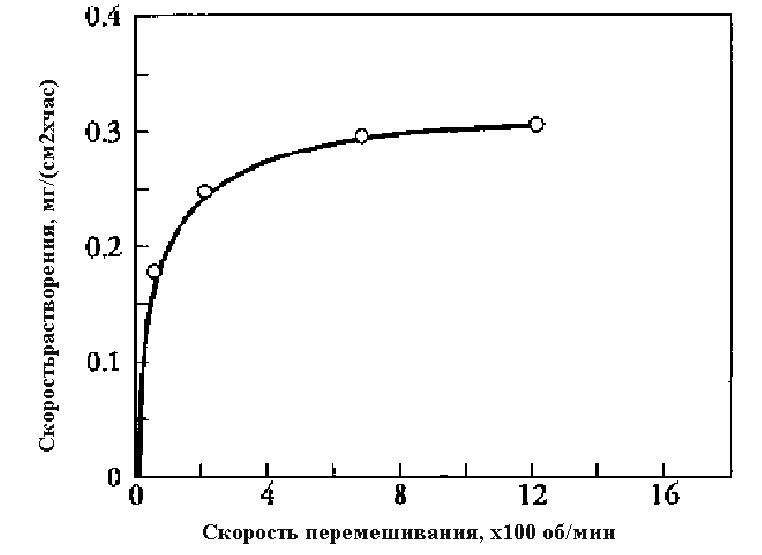
Рис.4.4.1. Зависимость скорости растворения цинка от скорости вращения мешалки.
Из рисунка видно, что при увеличении скорости вращения мешалки до 800 об/мин дальнейшее увеличение скорости растворения практически прекращается. Причиной этого может быть переход процесса в кинетическую область, где скорость процесс не зависит от скорости транспорта реагента к поверхности раздела фаз, на которой происходит химическое превращение.
Другим способом определения области протекания гетерогенного процесса является исследование зависимости общей скорости процесса от температуры.
Известно, что энергия активации химических процессов находится обычно в интервале 40200 кДж/моль. В то время как энергия активации диффузионных процессов, протекающих в жидких или газообразных средах находится в пределах 420 кДж/моль
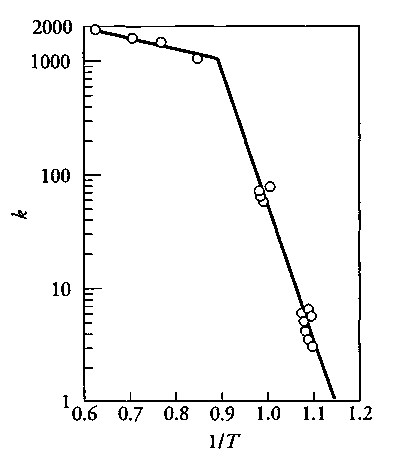
Рис.4.4.2: Влияние температуры на реакцию C+½O2→CO. В интервале температур 600-800°C, E=174 кДж/моль (химический контроль), и в интервале 1100-1300°C, E=6.3 кДж/моль (диффузионный контроль)
На рис.4.4.2 показано влияние температуры на реакцию окисления углерода при недостатке кислорода. Из рисунка видно, что в интервале температур 600-800°C, поверхностная реакция окисления является боле медленной стадией, чем скорость транспорта кислорода к реакционной поверхности. При достижении температуры 1000С скорость поверхностной реакции увеличивается настолько, что скорость транспорта кислорода к реакционной поверхности становится медленнее возможной скорости его расхода и гетерогенный процесс окисления переходит в область диффузионного контроля.
Влияние формы межфазной поверхности раздела фаз на скорость гетерогенных процессов.
Форма твердого вещества, подвергаемого реакции в жидкой или газовой фазе играет важную роль в определении скорости процесса. Если твердое вещество имеет форму пластины или диска, площадь поверхности будет оставаться постоянной в ходе реакции и, следовательно, скорость процесса также будет постоянной. Однако, если твердое вещество имеет форму сферы или таблетки, поверхность будет непрерывно изменяться в ходе реакции и, следовательно, скорость будет также изменяться. Если это изменение ввести в рассмотрение, можно предсказать изменение скорости процесса по мере его протекания
Рассмотрим реакцию «твердое-жидкость», например реакцию растворения металла в кислоте.
Скорость растворения твердых частиц металла в кислоте может быть описана уравнением:
![]() (4.4.9)
(4.4.9)
где W-масса металла в произвольный момент времени, кг
А – поверхность частиц металла, м2.
![]() концентрация
кислоты на поверхности раздела фаз
концентрация
кислоты на поверхности раздела фаз
Пусть частицы металла имеют сферическую форму радиуса r . Тогда
![]() -
радиус частицы в начальный момент
времени, м
-
радиус частицы в начальный момент
времени, м
![]() -
масса частиц в начальный момент времени,
кг
-
масса частиц в начальный момент времени,
кг
![]() -
масса одной частицы в произвольный
момент времени, кг
-
масса одной частицы в произвольный
момент времени, кг
![]() -
плотность частицы, кг/м3.
-
плотность частицы, кг/м3.
![]() -
масса частицы в
начальный момент времени, кг
-
масса частицы в
начальный момент времени, кг
![]() -
радиус частицы в начальный момент
времени, м.
-
радиус частицы в начальный момент
времени, м.
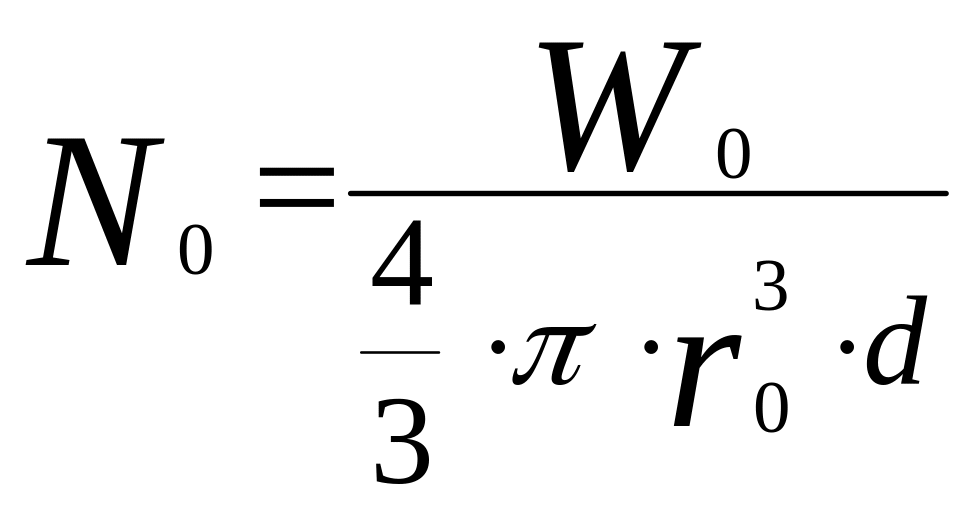 - число частиц в
начальный момент времени.
- число частиц в
начальный момент времени.
Допуская, что число частиц в процессе не изменяется, а изменяется только масса частицы, можно получить следующее выражение для текущей массы частицы:
![]() - где W
– текущая масса частиц в любой момент
времени, кг
- где W
– текущая масса частиц в любой момент
времени, кг
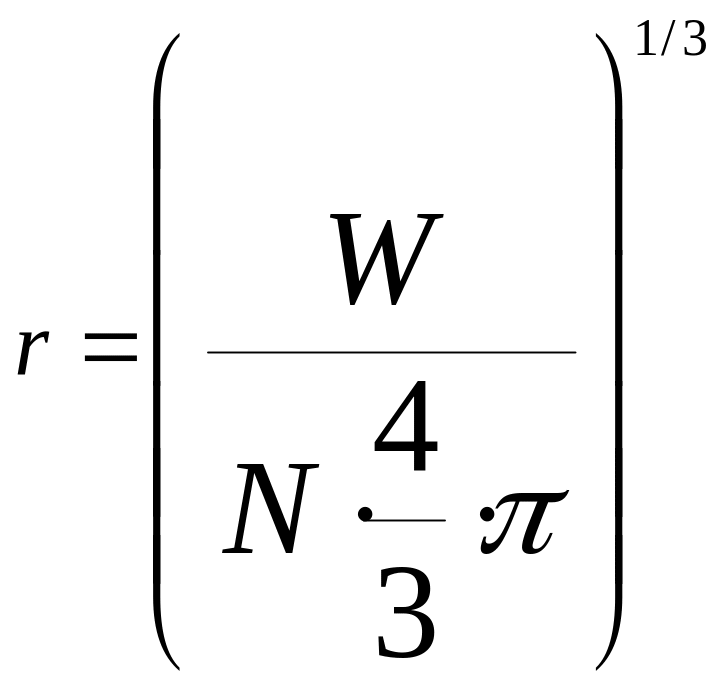 -радиус
частицы в произвольный момент времени,
м
-радиус
частицы в произвольный момент времени,
м
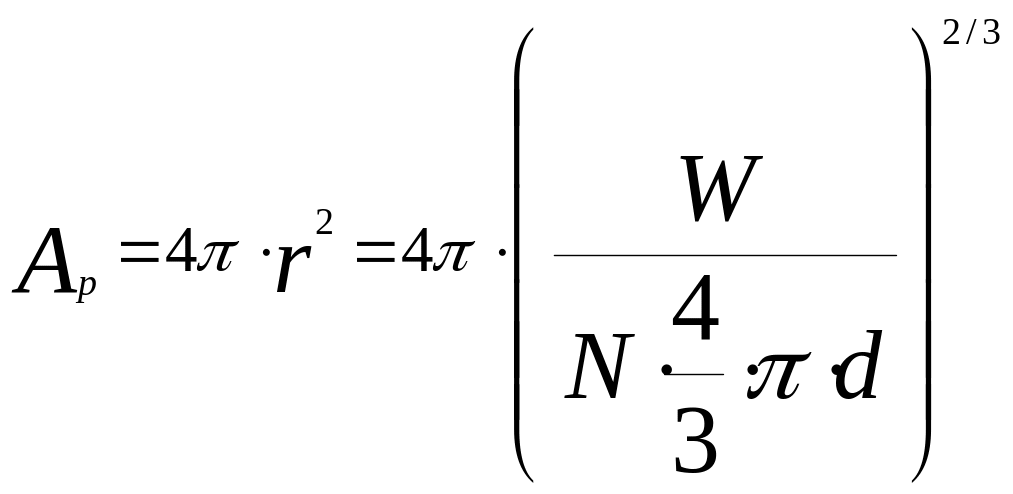 -поверхность
частицы в произвольный момент времени,
м2.
-поверхность
частицы в произвольный момент времени,
м2.
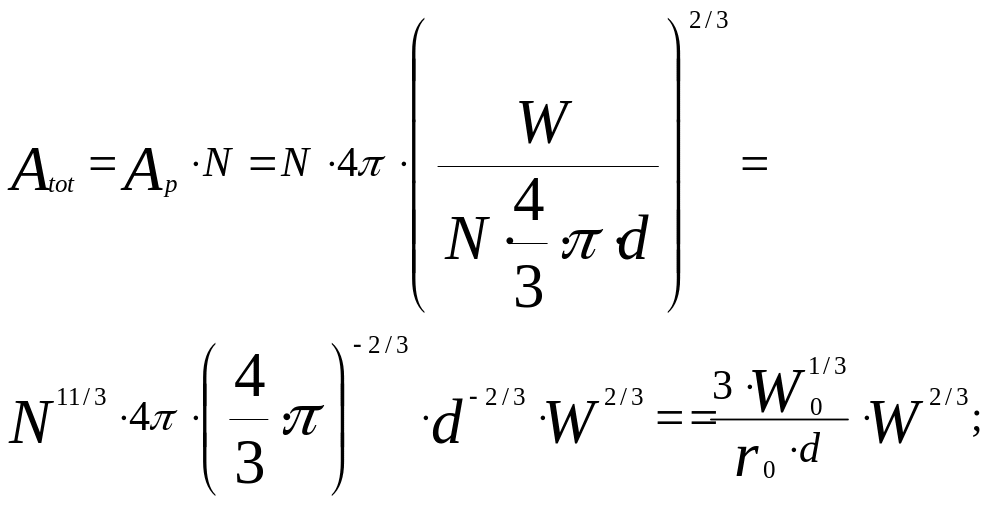
![]() -общая
поверхность всех частиц при текущей
массе частиц W,
м2.
-общая
поверхность всех частиц при текущей
массе частиц W,
м2.
Обозначим
через
![]() удельную
поверхность частиц- поверхность,
приходящую на единицу объем реактора,
получим следующее уравнение, выражающее
ее величину как функцию текущей массы
металла:
удельную
поверхность частиц- поверхность,
приходящую на единицу объем реактора,
получим следующее уравнение, выражающее
ее величину как функцию текущей массы
металла:
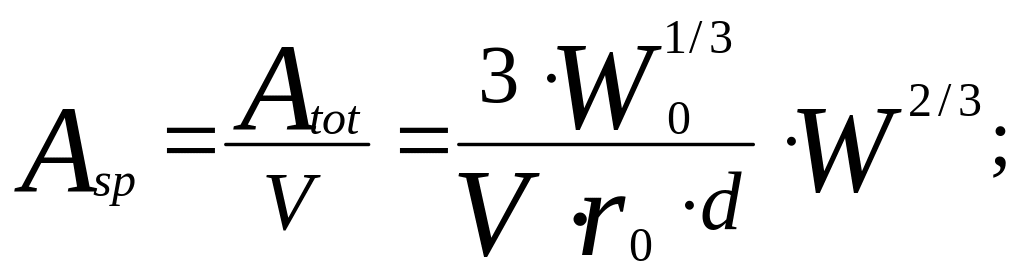 (4.4.11)
(4.4.11)
- удельная поверхность частиц, м2/м3.
Подставляя это значение удельной поверхности в уравнения для скоростей отдельных стадий процесса, записанного как для гомогенной реакции, мы получим уравнение скорости реакции, протекающей на поверхности твердой фазы, содержащейся в единице реакционного объем:
![]() (4.4.12)
(4.4.12)
Где
![]() - скорость гетерогенной и гомогенной
реакций , соответственно.
- скорость гетерогенной и гомогенной
реакций , соответственно.
Выразим теперь текущее значение веса твердого реагента через его мольную концентрацию и объем реактора:
![]() (4.4.13)
(4.4.13)
Ms –молекулярная масса твердой фазы, кг|кмоль
![]() -
мольная концентрация твердой фазы в
объеме реактора, кмоль/м3.
-
мольная концентрация твердой фазы в
объеме реактора, кмоль/м3.
Продифференцировав обе части уравнения (12) по времени, с учетом уравнения (11),получим выражение для скорости изменения веса твердого реагента:
![]() (4.4.14)
(4.4.14)
Где
![]() имеют
размерность кг/м3.
имеют
размерность кг/м3.
Используя уравнение (4.4.12) можно записать уравнения математической модели для остальных компонентов в следующем виде:
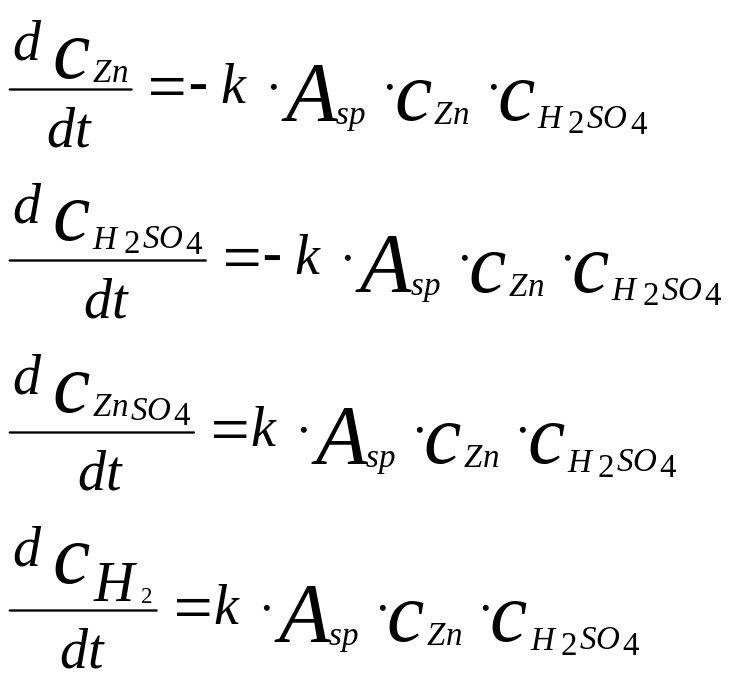 (4.4.15)
(4.4.15)
Таким образом, для получения математической модели гетерогенного процесса с использованием с использованием квазигомогенной модели можно использовать программный комплекс ReactOp, создав нестандартную модель следующим образом:
Записать уравнения химических реакций для всех стадий.
Записать уравнение для текущего значения массы твердой фазы( если она изменяется.
Записать выражение для удельной поверхности контакта фаз.
Умножить скорости изменения концентраций компонентов, полученные в программе ReactOp на величину удельной поверхности контакта фаз.
Эта процедура занимает немного времени и выполняется очень просто с использованием алгоритмического языка Fortran, близком к языку обычной записи математических формул.
