
- •РаствоРы электролитов
- •1. Отступление от законов Вант-Гоффа и Рауля в растворах электролитов.
- •2. Основные положения теории сильных электролитов
- •3. Активность и ионная сила электролита.
- •4. Электропроводность растворов.
- •5. Удельная электропроводность
- •6. Эквивалентная электропроводность растворов
2. Основные положения теории сильных электролитов
Как уже упоминалось, величина электропроводности сильных электролитов далеко не соответствует полной диссоциации их молекул на ионы. Однако при оптических и спектральных исследованиях растворов сильных электролитов в них не обнаруживается характерных свойств молекул, что отличает эти растворы от растворов слабых электролитов, в которых можно обнаружить недиссоциированные молекулы. Рентгенографическое исследование кристаллов сильных электролитов, например КС1 и НаС1, показало, что эти электролиты даже в твердом агрегатном состоянии не содержат молекул и имеют ионные кристаллические решетки. Однако если принять полную диссоциацию сильных электролитов и этим ограничиться, то совершенно необъяснимы будут другие явления. Например, экспериментально определяемые величины понижения температуры замерзания и повышения температуры кипения оказываются у сильных электролитов меньше, чем следовало бы ожидать при полной диссоциации молекул на ионы. Таким образом, теория электролитической диссоциации уже не могла полностью объяснить всех свойств растворов.
СЛ.
6 (0)
В 1923г. Дебай и Гюккель создали теорию
сильных электролитов.
Согласно этой теории в растворах
сильных электролитов действуют
электростатические силы притяжения
между разноименными ионами и силы
отталкивания — между одноименными.
Вокруг каждого иона образуется ионная
атмосфера, состоящая из ионов
противоположного знака. Каждый из ионов
этой атмосферы находится в окружении
другой ионной атмосферы. Поэтому раствор
сильного электролита можно рассматривать
как систему равномерно распределенных
по всему объему сосуда разноименных
ионов, каждый из которых
находится
в центре силового поля, создаваемого
окружающими ионами (рис.
1
СЛ. 6 (1)).
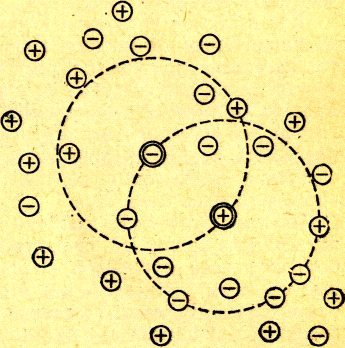
Все это обусловливает довольно сложные взаимоотношения между компонентами раствора, которые не могут не сказаться на его свойствах.
Рис. 1. Модель ионной атмосферы, принятая теорией Дебая и Гюккеля.
Исходя из того, что сильные электролиты полностью диссоциированы, можно было ожидать, что коэффициент Вант-Гоффа i для электролита, диссоциирующего, например, на два иона, должен равняться двум не только в разбавленных, но и в достаточно концентрированных растворах. Однако опыты не подтверждают этого. Коэффициент i в растворах сильных электролитов в значительной степени зависит от концентрации электролита, уменьшаясь с увеличением концентрации раствора. Такая зависимость i от концентрации в растворах объясняется взаимодействием ионов между собой.
В электрическом поле постоянного тока ионы в растворах сильных электролитов имеют меньшую подвижность ввиду межионного взаимодействия.
Дело в том, что под влиянием внешнего электрического поля «ионная атмосфера» смещается к одному полюсу, а ион, находящийся в центре этой атмосферы, стремится к другому полюсу. Кроме того, увлекаемые ионами сольватные (гидратные) оболочки также способствуют их торможению. Чем выше концентрация растворов, тем плотнее «ионная атмосфера» и тем медленнее движутся ионы.
Межионное взаимодействие, а также сольватация ионов уменьшают не только абсолютную скорость их движения, но и осмотическое давление растворов, величину понижения давления пара над ними и т. д. Создается впечатление, что в растворе находится меньше ионов, чем на самом деле. Поэтому величина является не истинной, а кажущейся степенью электролитической диссоциации сильного электролита.
В слабых электролитах, растворы которых содержат относительно малое количество ионов, взаимодействие последних сравнительно невелико. Кажущаяся степень диссоциации для них практически отвечает истинному значению.
