
- •РаствоРы электролитов
- •1. Отступление от законов Вант-Гоффа и Рауля в растворах электролитов.
- •2. Основные положения теории сильных электролитов
- •3. Активность и ионная сила электролита.
- •4. Электропроводность растворов.
- •5. Удельная электропроводность
- •6. Эквивалентная электропроводность растворов
6. Эквивалентная электропроводность растворов
СЛ.
13
Под эквивалентной
электропроводностью понимают
электропроводность столба раствора,
содержащего 1 г-экв
растворенного
вещества, заключенного между
электродами, находящимися друг от друга
на расстоянии в 1 см.
Обозначается
эквивалентная электропроводность
буквой
(греч.
«ламбда»), причем индексом внизу
показывают обычно объем (в литрах), в
котором содержится 1 г-экв
электролита.
Например, 10
–
эквивалентная электропроводность 0,1
н. раствора электролита, т. е. раствора,
содержащего 1 г-экв
растворенного
вещества.
Физический
смысл эквивалентной электропроводности
состоит в следующем (рис.
3 СЛ.
14).
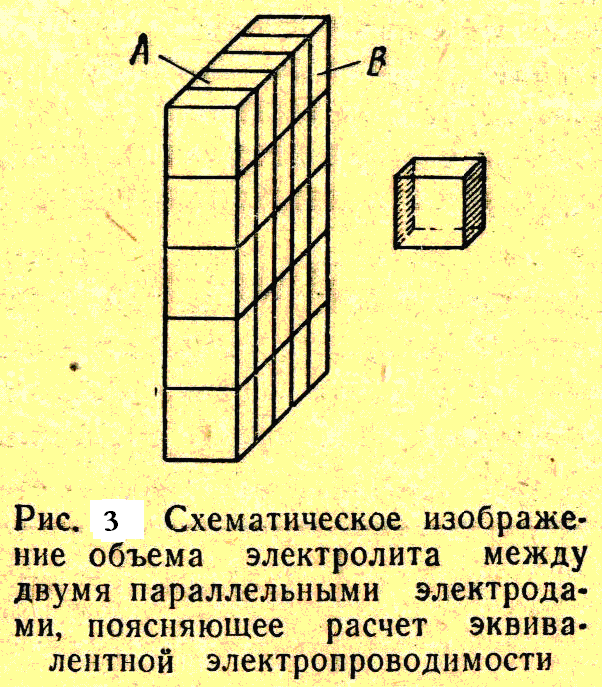
Предположим, что какой-то объем раствора электролита, содержащий 1 г-экв растворенного вещества, находится в сосуде с плоскопараллельными стенками А и В, которые представляют собой платиновые электроды и находятся на расстоянии 1 см друг от друга. Если объем данного раствора составляет 1 см3, то его электропроводность удельная. Если же объем раствора больше, например, 1 см3, то разобьем мысленно этот объем на n-е число кубиков (на рис. 3 этот кубик показан справа), каждый из которых будет иметь удельную электропроводность .
Тогда
суммарная или в данном случае СЛ.
15 (0)
эквивалентная электропроводность
всего раствора будет равна: =n.
Поскольку
в каждом кубике содержится 1/n
грамм-эквивалентов
растворенного вещества, концентрация
раствора С:
в
этом кубике также будет равна 1/п.
(1)
Отсюда эквивалентная электропроводность
будет:
![]()
(2)
Учитывая, что С1
= С/1000, где С — число грамм-эквивалентов
в 1 л
раствора,
после подстановки этого выражения в
последнее уравнение получим:
![]()
(3)
Поскольку концентрация С
— величина
обратная разбавлению V,
последнее
уравнение может быть представлено так:
=1000V
где V — разбавление раствора (т. е. объем в литрах, содержащий 1 г-экв электролита).
Таким образом, эквивалентная электропроводность раствора электролита равна его удельной электропроводности, умноженной на разбавление, выраженное в см3 на 1 г-экв электролита. Отсюда размерность эквивалентной электропроводности выразится в [см2 – Ом-1 • г-экв-1. Последний множитель определяется уже самим названием эквивалентной электропроводности. Его иногда опускают, и в качестве единицы измерения эквивалентной электропроводности указывают [см2 • олг1], подразумевая на 1 г-экв.
СЛ.
16
Эквивалентная электропроводность у
сильных и слабых электролитов
возрастает с увеличением разбавления
(т. е. с уменьшением концентрации
раствора) и достигает некоторого
предельного значения, которое называется
электропроводностью
при бесконечном разбавлении.
Обозначается
она буквой
или
0.
Это явление объясняется тем, что по мере
разбавления растворов слабых электролитов
растет степень электролитической
диссоциации ,
для сильных же электролитов
увеличивается расстояние между ионами,
в результате чего силы взаимного
притяжения ослабевают и скорость
движения ионов повышается.
Если
выразить зависимость
от
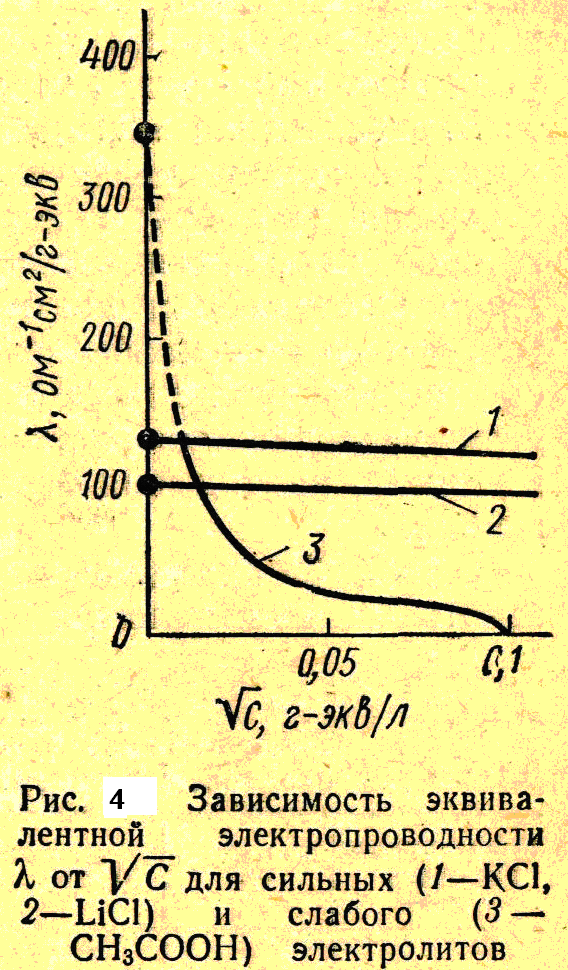
![]() графически, то для слабых электролитов
в области больших разбавлений получается
кривая, а для сильных — прямая линия
(рис.
4
графически, то для слабых электролитов
в области больших разбавлений получается
кривая, а для сильных — прямая линия
(рис.
4
СЛ. 17).
СЛ.
18 (0)
Для разбавленных растворов (не выше
0,002 н.) сильных электролитов зависимость
от
(1)
довольно хорошо выражается эмпирическим
уравнением:
![]()
(2)
где а
— угловой коэффициент, зависящий от
природы растворителя, температуры и
валентности электролита. Второй член
этого уравнения а
характеризует
уменьшение электропроводности вследствие
взаимного торможения ионов, природа
которого обусловлена наличием ионных
атмосфер, окружающих все находящиеся
в растворе ионы.
Эквивалентная
электропроводность зависит от температуры.
Для большинства электролитов
электропроводность увеличивается с
повышением температуры, что объясняется
увеличением скорости движения ионов в
растворе. (3)
Это увеличение имеет линейный характер:
t = 18[1+ (t-18)]
где t и 18 — эквивалентная электропроводность при температуре 18°С, — температурный коэффициент электропроводности. Увеличение температуры на один градус приводит к возрастанию эквивалентной электропроводности в среднем на 2—2,5%. Вот почему при всех измерениях электропроводности необходимо тщательное термостатирование.
Для некоторых электролитов электропроводность с увеличением температуры уменьшается, что характерно для неводных растворов и обусловлено уменьшением диэлектрической проницаемости растворителя.
