
- •Аналитическая химия
- •Часть 1
- •Isbn 985-466-015-х
- •Раздел 1
- •Глава 1
- •Разложение пробы
- •1.3. Виды анализа
- •Экстракционная фотометрия
- •Глава 2
- •2.1. Аналитические реакции
- •2.2. Систематический и дробный анализ
- •Комплексообразование
- •2.3. Общая характеристика, классификация и способы обнаружения катионов
- •2.4. Общая характеристика, классификация и способы обнаружения анионов
- •Глава 3
- •3.1. Общая характеристика химического равновесия. Константа химического равновесия
- •3.2. Активность и коэффициент активности
- •3.3. Отклонения от идеальности в растворах сильных электролитов
- •3.4. Виды констант химического равновесия, используемые в аналитической химии
- •3.5. Общие принципы расчёта состава равновесных систем
- •Глава 4
- •4.1. Важнейшие теории кислот и оснований
- •4.2. Количественное описание силы кислот и оснований
- •4.3. Влияние растворителя на кислотно-основные свойства растворённого вещества
- •4.4. Нивелирующее и дифференцирующее действие растворителя. Сильные и слабые кислоты и основания
- •4.5. Расчёт рН водных растворов различных прото- литов
- •4.6. Расчёт состава равновесных смесей протолитов при заданном значении рН
- •4.7. Кислотно-основные буферные растворы
- •Глава 5
- •5.1. Понятие о комплексном соединении
- •5.2. Классификация комплексных соединений
- •5.3. Равновесия в растворах комплексных соединений
- •Общая константа образования
- •5.4. Влияние различных факторов на комплексообразование в растворах
- •5.5. Применение органических реагентов в аналитической химии
- •Лиганды с одним типом донорных атомов о,о-лиганды
- •Шестичленные циклы
- •Органические реагенты
- •6.1. Произведение растворимости малорастворимого электролита
- •Глава 6
- •6.2. Растворимость
- •6.3. Влияние различных факторов на растворимость
- •6.4. Общие принципы растворения осадков малорастворимых электролитов
- •Глава 7
- •7.1. Общая характеристика окислительно-восстановительных реакций
- •7.2. Количественная оценка окислительно-восстановительной способности веществ
- •7.3. Влияние различных факторов на протекание окислительно-восстановительных реакций
- •Глава 8
- •8.1. Отбор пробы
- •Анализируемым образец
- •I эмпирический
- •Генеральная проба
- •Лабораторная проба
- •8.2. Разложение пробы
- •9.1. Общая характеристика и классификация
- •Глава 9
- •9.2. Жидкость - жидкостная экстракция
- •Реэкстракт
- •Реэкстракция
- •Сложные эфиры фосфорной кислоты, фосфоновых, фосфиновых кислот, фосфиноксиды, сульфоксиды, диантипирилметан
- •Третичные амины, четвертичные аммониевые соли, соли тетрафениларсония и тетрафенилфосфония.
- •Глава 10
- •10.1. Приближённые вычисления и значащие цифры
- •3 Значащие цифры
- •1 Значащая цифра
- •10.2. Понятие об аналитическом сигнале
- •10.3. Методы расчёта концентрации вещества по величине аналитического сигнала
- •10.4. Неопределённость и погрешности измерений
- •10.5. Некоторые основные положения математической статистики, используемые в аналитической химии
- •10.6. Пример статистической обработки результатов измерений. Исключение промахов
- •10.7. Основные характеристики методики анализа
- •Раздел 2
- •Глава 11
- •11.3. Понятие о механизме образования осадка
- •11.4. Коллоидная стадия образования осадка
- •11.5. Причины загрязнения осадка и способы их устранения
- •11.6. Основные этапы методики гравиметрического определения методом осаждения
- •11.7. Гравиметрия в фармацевтическом анализе
- •Глава 12 общая характеристика титриметрических методов анализа
- •12.1. Основные понятия титриметрии
- •Исчезновение окраски фенолфталеина
- •Появление розовой окраски раствора
- •12.2. Классификация титриметрических методов анализа и способов титрования
- •12.3. Стандартные растворы и стандартные вещества
- •12.4. Расчёты, связанные с приготовлением растворов титрантов и титрованием
- •Vисх_mрисх_m(hCl) _n(hCl) - m(hCl) _c(hCl) - V - m(hCl) _p _ra(hCl) -p_ ra(hCl) -p _p-ra(hCl)
- •Глава 13 кислотно-основное титрование
- •13.1. Титранты и стандартные вещества
- •13.2. Обнаружение конечной точки титрования. Кислотно-основные индикаторы
- •13.3. Кривые титрования
- •13.4. Факторы, влияющие на величину скачка титрования
- •0,1МNaOh (1), 0,001мhCl 0,001мNaOh (2) и или основания (рис. 13.4).
- •0,1МhCl 0,1мNaOh (3)Прямое титрование таких
- •13.5. Погрешности титрования
- •13.6. Некоторые случаи практического применения кислотно-основного титрования в водных растворах
- •Глава 14 кислотно-основное титрование в неводных средах
- •14.3. Применение в фармацевтическом анализе
- •Глава 15 комплексометрическое титрование
- •15.1. Общая характеристика
- •15.2. Меркуриметрическое титрование
- •Ind HgInd фиолетовый Ind жёлтыйHg[Fe(cn)sNo]
- •15.3. Комплексонометрическое титрование
- •Глава 16
- •16.3. Меркурометрическое титрование
- •Глава 17
- •17.1. Общая характеристика и классификация
- •17.2. Кривые титрования
- •17.3. Способы обнаружения конечной точки титрования. Окислительно-восстановительные индикаторы
- •Глава 18
- •18.1. Иодометрическое титрование
- •18.2. Хлориодометрическое титрование
- •18.3. Иодатометрическое титрование
- •18.4. Броматометрическое титрование
- •18.5. Нитритометрическое титрование
- •I" крахмал избыток NaNo2 i4
- •18.6. Перманганатометрическое титрование
- •18.8. Дихроматометрическое титрование
- •18.8. Цериметрическое титрование
- •Раздел 3
- •Глава 19
- •19.1. Природа и свойства электромагнитного излучения
- •19.2. Классификация спектроскопических методов анализа
- •Глава 20
- •20.2. Отклонения от основного закона светопоглощения
- •20.3. Атомно-абсорбционная спектроскопия
- •20.4. Молекулярная абсорбционная спектроскопия в уф- и видимой области
- •Сурьмяно-цезиевый фотоэлемент кислородно-цезиевый фотоэлемент
- •20.4.3. Практическое применение и основные приёмы фотометрического анализа
- •Измерение светопоглощения хлороформного экстракта
- •Метод отношения пропусканий
- •Метод предельной точности
- •20.5.1. Процессы, приводящие к появлению аналитического сигнала
- •20.5.2. Общая характеристика ик-спектров
- •20.5.3. Измерение аналитического сигнала
- •20.5.4. Практическое применение
- •Глава 21 эмиссионные спектроскопические методы анализа
- •21.1. Атомно-эмиссионная спектроскопия
- •21.1.1. Процессы, приводящие к появлению аналитического сигнала
- •21.1.2. Измерение аналитического сигнала
- •Пламенная фотометрия
- •3000-7000 °C невысокая воспроизводимостьтолько щелочные, щелочноземельные металлы и т.П.
- •Фотоэлементы, фотоумножители, фотодиоды
- •21.1.3. Практическое применение
- •20.2. Люминесцентная спектроскопия
- •20.2.1 Классификация видов люминесценции
- •21.2.2 Механизм молекулярной фотолюминесценции. Флуоресценция и фосфоресценция
- •21.2.3 Основные характеристики и закономерности люминесценции
- •21.2.4. Влияние различных факторов на интенсивность флуоресценции растворов
- •21.2.5. Измерение аналитического сигнала
- •21.2.6. Практическое применение и основные приёмы люминесцентного анализа
- •Рибофлавин офлоксацин
- •Глава 22 общая характеристика и теоретические основы хроматографических методов анализа
- •22.1. Общая характеристика
- •22.2. Классификация хроматографических методов
- •Агрегатное состояние подвижной фазы
- •22.3. Хроматографические параметры
- •22.4. Теории хроматографического разделения
- •Глава 23
- •Сорбент помещают внутрь колонки
- •23.3. Особенности газотвёрдофазной хроматографии
- •23.4. Особенности газожидкостной хроматографии
- •23.5. Индексы удерживания Ковача
- •23.6. Практическое применение
- •Глава 24
- •Жидкостная хроматография
- •24.1. Общая характеристика
- •24.2. Плоскостная хроматография
- •Плоскостная хроматография
- •24.2.1. Методика получения плоскостной хроматограммы
- •24.2.2. Анализ плоскостной хроматограммы
- •24.2.3. Практическое применение
- •24.3. Колоночная жидкостная хроматография
- •24.3.1. Устройство жидкостного хроматографа
- •Ввод пробы
- •24.3.2. Практическое применение
- •24.4. Характеристика отдельных видов жидкостной хроматографии
- •24.4.1. Ионообменная хроматография
- •Сильнокислотные
- •24.4.2. Эксклюзионная хроматография
- •Глава 25 общая характеристика электрохимических методов анализа. Кондукгометрия
- •25.1. Основные понятия, связанные с электрохимическими методами анализа
- •25.2. Классификация электрохимических методов анализа
- •25.3. Кондуктометрия
- •25.3.1. Теоретические основы и классификация
- •25.3.2. Измерение аналитического сигнала
- •25.3.4. Практическое применение
- •25.3.5. Понятие о высокочастотной кондуктометрии
- •Глава 26 потенциометрический и кулонометрический методы анализа
- •26.1. Потенциометрический метод анализа
- •26.1.1. Общая характеристика и классификация
- •26.1.3. Индикаторные электроды
- •Первичные ионоселективные электроды
- •Электроды с подвижными носителями
- •Имеют жидкую мембрану -
- •26.1.4. Прямая потенциометрия
- •26.1.5. Потенциометрическое титрование
- •26.2. Кулонометрический метод анализа
- •26.2.1. Общая характеристика и классификация
- •26.2.2. Прямая кулонометрия
- •26.2.3. Кулонометрическое титрование
- •Глава 27 вольтамперометрический метод анализа
- •27.1. Принцип измерения аналитического сигнала.
- •27.2. Вольтамперограмма
- •Максимум второго рода
- •Максимум первого рода
- •27.3. Некоторые современные разновидности вольт- амперометрии
- •27.4. Практическое применение вольтамперометрии. Амперометрическое титрование
20.3. Атомно-абсорбционная спектроскопия
Атомно-абсорбционная спектроскопия(ААС) -спектроскопический метод анализа, основанный на измерении поглощения электромагнитного излучения оптического диапазона невозбуждёнными свободными атомами.
20.3.1. Процессы, приводящие к появлению аналитического сигнала
При
поглощении атомом кванта электромагнитного
излучения один из его электронов
переходит на более высокий энергетический
уровень - атом переходит из основного
в возбуждённое состояние. Атом способен
поглощать только такое электромагнитное
излучение, энергия которого точно равна
разности между энергией возбуждённого
и основного состояния (рис. 20.5). Например,
атом Na
может
поглощать электромагнитное излучение
с длинами волн 589,0 нм (3s
^
3p),
330,23
нм (3s
^
4p),
285,28
нм (3s
^
5p)
и
некоторыми другими.
3
E*
AE
=
hv
\
\
\
\
o
EoAE
=
E*
-
E
Рис. 20.5. Схема процесса, лежащего в основе ААС
Поскольку
энергии переходов между различными
энергетическими уровнями для атомов
разных элементов отличаются, то атом
каждого элемента будет иметь свой
собственный атомный спектр поглощения.
Поглощение электромагнитного излучения
атомами происходит при строго
определённых длинах волн, поэтому
атомные спектры поглощения являются
линейчатыми (рис. 20.6).
Рис.
20.7.
Принципиальная схема прибора для ААС
ввод
пробы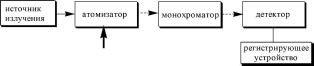
J I
X
Рис. 20.6. Условный атомный спектр поглощения
20.3.2. Измерение аналитического сигнала
Принцип
измерения аналитического сигнала в
ААС такой же, как и в других абсорбционных
спектроскопических методах анализа.
В ААС измеряют относительную интенсивность
двух потоков излучения, один из
которых проходит через атомный пар, а
другой является потоком сравнения.
Принципиальная схема атомно- абсорбционного
спектрометра приведена на рис. 20.7.
Атомы поглощают излучение в очень узком диапазоне, который с помощью монохроматора выделить из спектра испускания непрерывного источника невозможно. Если же пропускать через атомный пар немонохроматическое излучение, то факт поглощения невозможно практически зарегистрировать

Лампа
с полым катодом
представляет собой стеклянный или
кварцевый баллон, заполненный
находящимся под низким давлением
инертным газом (рис. 20.8). Внутри
баллона находятся катод и анод, к
которым Рис.
20.8.
Лампа с полым катодом
приложено высокое напряжение. Катод
изготовлен из такого металла, для
определения которого используется
данная лампа (легкоплавкий металл
наносится в виде тонкого слоя на
поверхность другого металла), и имеет
цилиндрическую форму. Под действием
высоковольтного разряда атомы инертного
газа ионизируются с образованием
положительно заряженных ионов,
бомбардируют катод и «выбивают» из
него атомы металла. Последние возбуждаются
и испускают излучение характерное
для свободных атомов данного металла.
Из полученного линейчатого спектра
выбирают с помощью обычного монохроматора
одну определённую линию и затем
используют её для определения
соответствующего элемента.
Для определения каждого элемента нужна
своя лампа.
Атомизатор
необходим для того, чтобы получить
свободные атомы. Молекулы имеют другое
строение электронных орбиталей и
совершенно другой вид спектров
поглощения.
Атомизация должна проводиться в таких
условиях, чтобы атомы оставались
невозбуждёнными.
Перед атомизацией анализируемый образец
переводят в раствор. В ААС используется
две группы атомизаторов: пламенные и
электротермические.
J
представляет собой горелку, в которой
пламя
имеет форму узкой вытянутой щели.
Такая форма пламени позволяет получить
большую длину поглощающего слоя, что
приво
дит
к повышению чувствительности определения.
Для создания пламени
используются горючие газовые смеси
различного состава, например,
ацетилен-воздух, ацетилен - кислород,
пропан - воздух и др.
Электротермический
атомизатор
представляет собой трубку длиной
несколько сантиметров и внутренним
диаметром до 1 см, изготовленную
обычно из плотных сортов графита. Трубка
нагревается до высокой температуры
электрическим током большой силы. Для
предотвращения сгорания графита трубка
заполнена инертным газом. Электротермическая
атомизация обладает рядом преимуществ
перед пламенной, например, более
эффективной атомизацией и более высокой
чувствительностью определения, меньшим
объёмом анализируемой пробы,
возможностью вести измерения в вакуумной
УФ-области и т. д.
В
качестве детектора в ААС
обычно используют фотоумножители.
Это связано с тем, что интенсивность
излучения источника невысокая.
Детектор связан через усилитель с
соответствующим регистрирующим
устройством.
20.3.3. Практическое применение
ААС
используется для
количественного определения
более 70 элементов, главным образом,
металлов.
Зависимость
между степенью поглощения электромагнитного
излучения и концентрацией поглощающего
вещества в ААС такая же, как и в других
абсорбционных методах анализа. Оптическая
плотность прямо пропорциональна
концентрации атомов соответствующего
элемента в атомизаторе и, следовательно,
в анализируемой пробе
A
=
k^C
Коэффициент
k
является
эмпирической величиной. Определение
концентрации в ААС проводят методом
градуировочного графика или методом
добавок.
В
Республике Беларусь ААС используется
для определения неорганических
токсикантов («металлических ядов») в
различных биологических объектах
при судебно-химическом и химико-
токсикологическом исследовании. Пределы
обнаружения большинства элементов
составляют при использовании пламени
1-100 мкг/л, при электротермической
атомизации на несколько порядков
меньше. Основные ограничения данного
метода анализа связаны с необходимостью
наличия большого набора соответствующих
ламп, а также необходимостью
переведения анализируемого объекта в
раствор.
