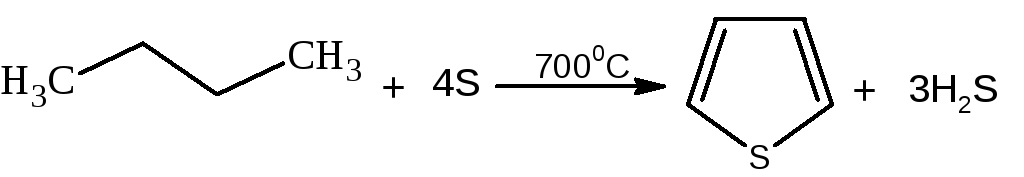- •176 Программа блока гетерофункциональные углеводороды.
- •Конспект лекций гетерофункциональные углеводороды
- •Углеводы
- •1.1 Моноуглеводы
- •Химическое строение моносахаридов
- •1. Реакции карбонильных форм моносахаридов
- •2.2 Реакции с участием всех гидроксильных групп
- •Олигосахариды
- •1.2.1 Дисахариды
- •1.2.3 Несахароподобные полисахариды
- •1.2.3.1 Гомополисахариды
- •1.2.3.2 Гетерополисахариды
- •2. Аминокислоты
- •(Nh2)m r(cooh)n,
- •2. Получение β-аминокислот
- •3.2.Перегруппировка оксимов (перегруппировка Бекмана):
- •1,1-Амидные группы
- •Оксикислоты
- •7. Синтез из альдегидов
- •1.3 Реакции нуклеофильного замещения α-галогенкарбоновых кислот.
- •4. Гетероциклические соединения
- •4.1 Пятичленные гетероциклы с одним гетероатомом
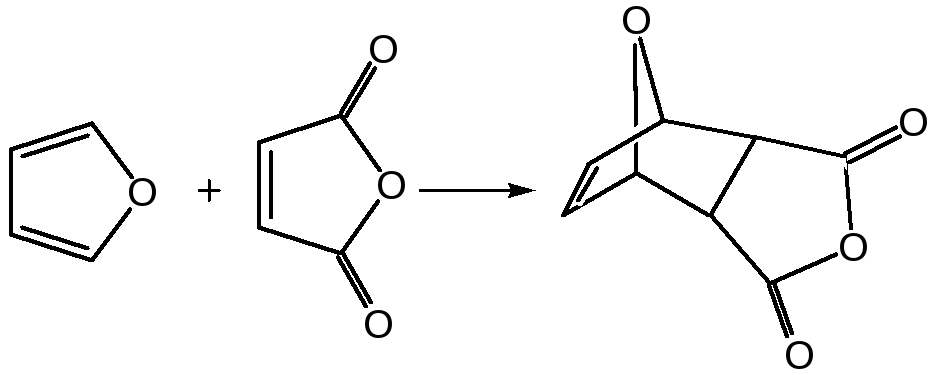
- •6. Реакция диенового синтеза с малеиновым ангидридом
- •2. Пиролизом:
- •1. Сухой перегонкой аммонийной соли слизевой кислоты или действием аммиака на фуран в присутствии оксида алюминия:
- •3. Получают при пропускании аммиака и паров бутиндиола-1,4 над катализатором при 300с:
- •4. При перегонке сукцинимида с цинковой пылью:
- •5. Восстановление смеси кетона с изонитрозокетона даёт гомологи или замещенные пирролы:
- •3. Реакция электрофильного замещения (механизм и ориентация замещения):
- •1. Индол обладает слабоосновными свойствами и в то же время слабокислыми, образует металлические производные – индол-калий, индол-натрий:
- •4.2 Пятичленные гетероциклы с несколькими гетероатомами
- •4.3 Шестичленные гетероциклы с одним гетероатомом
- •4.4 Шестичленные гетероциклы с несколькими гетероатомами
- •1. Основные свойства:
- •2. Свойства, обусловленные функциональными группами, в том числе групповые реакции:
- •4.4 Шестичленные гетероциклы с двумя разными гетероатомами
- •Нобелевские премии по органической химии
6. Реакция диенового синтеза с малеиновым ангидридом
Производные фурана
Тетрагидрофуран. Тетрагидрофуран получается гидрированием фурана в присутствии никелевого катализатора.

Другой метод получения тетрагидрофурана заключается в нагревании бутандиола-1,4 в присутствии дегидратирующих реагентов.
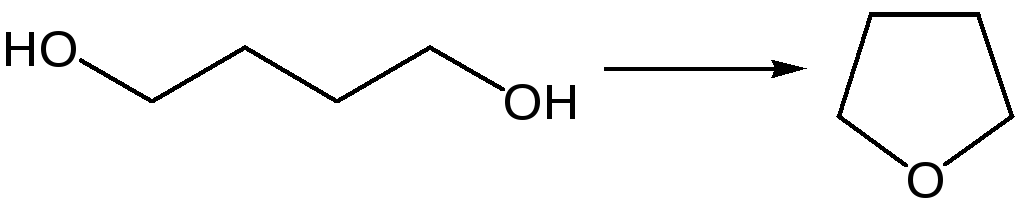
Кислородсодержащие предельные гетероциклы, не стабилизированные резонансом (энергией делокализации), ведут себя как простые циклические эфиры.
Фурфурол. Одним из важнейших производных фурана является фурановый альдегид фурфурол. Он же служит исходным веществом для получения самого фурана. Фурфурол получают дегидратацией пентоз, которые образуются в результате кислотного гидролиза полисахаридов – пентозанов, содержащихся в отходах сельско-хозяйственного производства: кукурузных початках, соломе, отрубях, шелухе подсолнечника и др.:
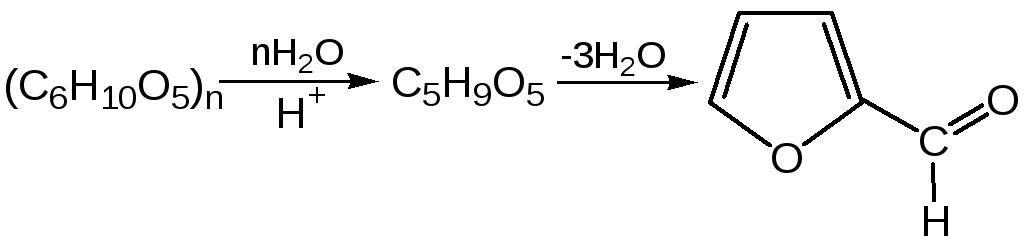
Физические свойства: фурфурол представляет собой бесцветную или слегка желтоватую жидкость с приятным запахом свежеиспеченного ржаного хлеба; температура кипения 162оС, умеренно растворим в воде.
Химические свойства. Химические свойства фурфурола напоминают химические свойства типичного ароматического альдегида – бензальдегида. Подобно бензальдегиду фурфурол вступает в реакцию самоокисления-самовосстановления (С. Канниццаро):
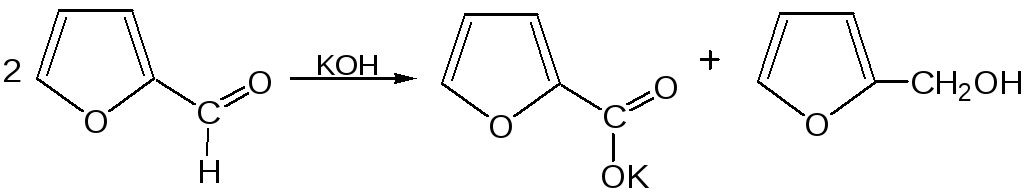
Химические свойства фурфурола можно отразить следующей схемой:
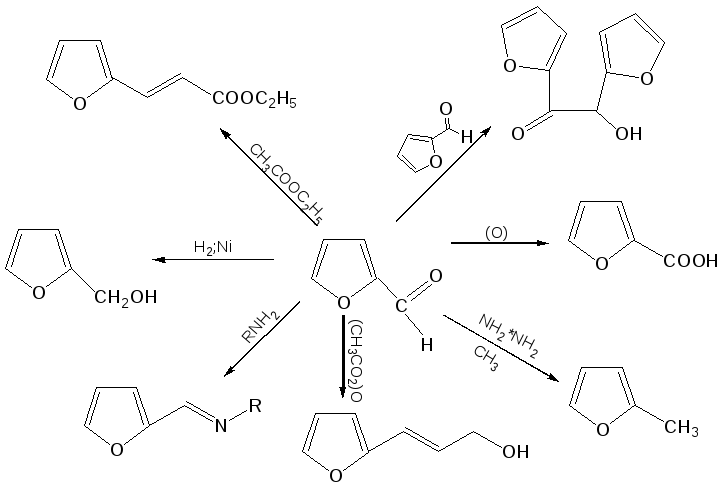
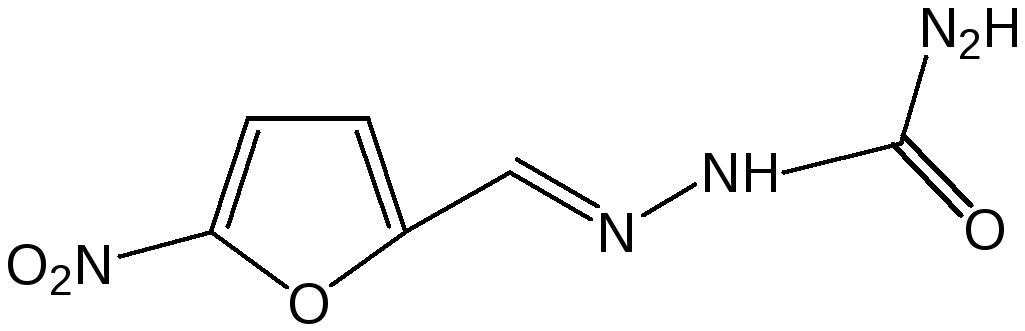
Применением фурфурола: Фурфурол широко используется в промышленности в качестве растворителя при очистке нефтяных фракций, для получения пластмасс (фенолфурфурольные смолы), фумаровой кислоты и многих соединений с фурановым кольцом, в частности, лекарственных препаратов. Например, семикарбазон 5-нитрофурфурола под названием «фурацилин» широко применяется в медицинской практике как противобактериальное средство:
Тиофен
История открытия. В. Мейер утверждал, что открытие им тиофена в 1883 г. было делом случая. В ходе лекции ему понадобилось показать образование индофенина – вещества темно-голубого цвета, которое образуется при смешивании бензола, выделенного из каменноугольной смолы, с изатином и концентрированной серной кислотой. До этого времени образование голубого вещества считалось характерной пробой на бензол. Мейер, который был осторожным и искусным экспериментатором, получил индофенин из каменноугольного бензола как раз перед началом лекции. Естественно, что он был весьма удивлен, когда оказался не в состоянии получить голубое вещество при демонстрации во время лекции. После того как его ассистент Зандмейер сообщил ему, что для лекционной демонстрации был взят другой образец бензола, а именно полученный декарбоксилированием бензойной кислоты. Мейер сразу же принялся за исследование обычного бензола, получаемого из каменноугольной смолы, и обнаружил, что он содержит небольшое количество органического сернистого соединения; оказалось, что индофенин образуется не из бензола, а из этого вещества. Было установлено, что оно является новым родоначальным соединением, которое хотя и весьма отличается от бензола по своему строению, однако поразительно сходно с ним по некоторым физическим и химическим свойствам, включая значительное число типичных реакций бензола, и во многих случаях дает производные, подобные производным бензола. Желая подчеркнуть это сходство, а также отразить наличие серы, Мейер назвал новое соединение тиофеном и немедленно начал изучение его свойств. В 1888 г. Мейер опубликовал монографию по тиофену и его производным, которая содержала огромное число сведений относительно химии этого уникального гетероциклического соединения.
Электронное строение. Электронная структура тиофена, как пиррола и фурана, основана на ароматическом секстете электронов, состоящем из 4 π-электронов, двух двойных углерод-углеродных связей и двух p-электронов атома серы. Однако в отличие от атомов азота и кислорода атом серы обладает еще и свободными d-орбиталями, которые, как показали исследования, также могут участвовать в образовании тиофенового кольца.
Современные электронные модели тиофена и строятся либо с учетом s-орбиталей, либо без учета их. В последнем случае тиофеновый цикл отличается по электронной структуре от фуранового или пиррольного цикла лишь меньшей электроотрицательностью атома серы по сравнению с атомами кислорода или азота.
Уменьшение электроотрицательности атома серы связано с увеличением электронной оболочки атома серы и появлением экранирующего электронного «пояса» между ядром атома и внешними электронами. Поэтому неподеленная электронная пара атома серы, входящая в кольцевую сопряженную систему тиофена, более делокализована, чем соответствующие неподеленные пары электронов у атомов кислорода или азота в фуране и пирроле. Этим обстоятельством объясняется большая ароматичность молекулы тиофена по сравнению с фураном и пирролом. По значению энергии делокализации 130,2 кДж/моль тиофен заметно приближается к бензолу.
Химические свойства
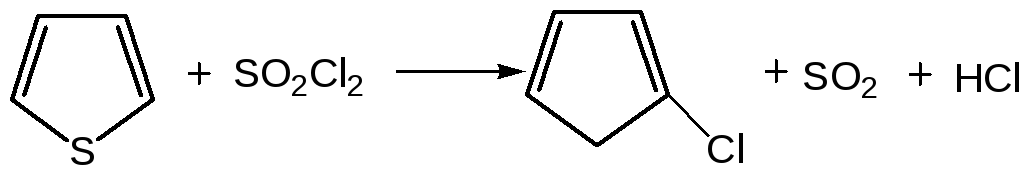
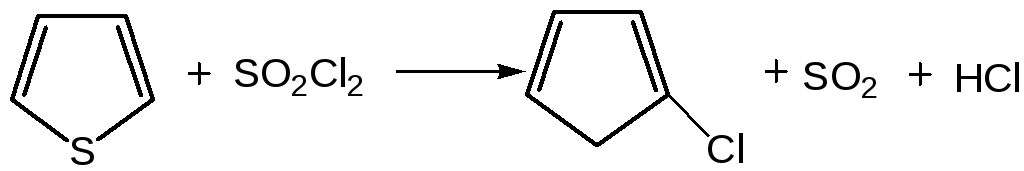
1. Реакция галогенирования. Для галогенирования тиофена можно использовать бром или хлор при низкой температуре, при этом могут образовываться как моно-, так и полигалогентиофены. Более избирательно действует сульфурилхлорид (SO2Cl2):
2. Реакция сульфирования. Повышенная устойчивость тиофена позволяет сульфировать его серной кислотой, причем, в отличие от бензола, тиофен сульфируется на холоде, что используется для очистки бензола от примесей тиофена:
3. Реакция нитрования. Хотя тиофен значительно устойчивее к действию минеральных кислот, чем фуран и пиррол, но и он окисляется азотной кислотой с разрушением молекулы. Поэтому для нитрования вышеназванных гетероциклов используют «мягкий» нитрующий агент – ацетилнитрит (смесь уксусного ангидрида с азотной кислотой) в пиридине, при этом образуются -нитропроизводные:
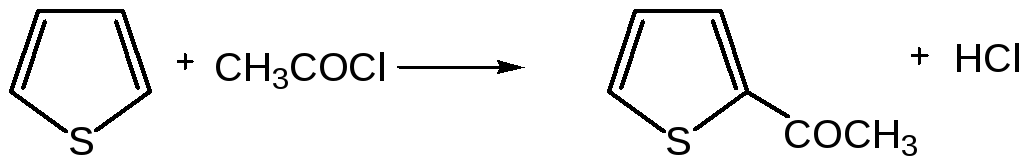
4. Реакция ацилирования. Реакцию ацилирования по Фриделю-Крафтсу проводят (подобно бензолу) в более жестких условиях:
5. Реакция гидрирования. Восстанавливается действием металлического натрия в спирте в присутствии аммиака, так как никелевые или платиновые катализаторы при гидрировании отравляются тиофеном и конечным продуктом гидрирования – тиофаном, который содержится в сернистых нефтях:

6. Реакция окисления. Тиофен в обычных условиях не окисляется. О термической устойчивости тиофена говорит сам факт его образования при температуре коксования угля (1000С).
Получение тиофена
1. В промышленности тиофен получают из бутана и паров серы или диоксида серы (SO2) при высокой температуре: