
- •Аминокислоты используются в качестве лекарств
- •Аминокислоты объединяют по разным признакам
- •Классификация аминокислот
- •Двадцать аминокислот необходимы для синтеза белка
- •Строение протеиногенных аминокислот
- •Право- и левовращающие формы аланина
- •Для аминокислот характерна амфотерность
- •Изменение заряда аминокислот при смещении рН раствора в кислую или щелочную сторону. Аминокислоты соединяются пептидной связью
- •Пути превращений аминокислот по боковой цепи
- •Серотонин
- •Реакции синтеза серотонина
- •Аминокислоты надо переносить через мембраны
- •Транспорт аминокислот через мембраны Вторичный активный транспорт
- •Вторичный активный транспорт аминокислот через мембраны
- •Глутатионовая система транспорта
- •Транспорт аминокислот при участии глутатиона
- •Аминокислоты могут давать энергию
- •Катаболизм аминокислот начинается с удаления аминогруппы
- •Прямое окислительное дезаминирование
- •Реакция, катализируемая оксидазами d- и l-аминокислот
- •Реакция прямого окислительного дезаминирования глутаминовой кислоты
- •Непрямое окислительное дезаминирование (трансдезаминирование)
- •Трансаминирование нуждается в витамине в6
- •Механизм реакции трансаминирования
- •Реакции полного цикла трансаминирования
- •Аминотрансферазы имеют клиническое значение
- •Реакции, катализируемые аланинаминотрансферазой и аспартатаминотрансферазой
- •Креатинфосфат - срочный резерв энергии
- •Использование креатинфосфата для ресинтеза атф
- •Образование креатинина из креатинфосфата
- •Реакции синтеза креатина в почках и печени
- •Синтез креатинфосфата
- •В мышце дезаминирование аминокислот идет особым образом
- •Реакции непрямого дезаминирования аминокислот в мышечной ткани
- •В клетках постоянно образуется аммиак
- •Основные источники аммиака
- •Связывание аммиака
- •Реакция синтеза глутаминовой кислоты
- •Реакция синтеза глутамина
- •Реакция синтеза аспарагина
- •Транспорт аммиака
- •Глюкозо-аланиновый цикл
- •Реакции глюкозо-аланинового цикла (выделен рамкой).
- •Накопление аммиака представляет проблему
- •Гипотезы токсичности аммиака
- •Наследственные и приобретенные формы гипераммониемий Приобретенные формы
- •Наследственные формы
- •Для удаления аммиака есть два способа
- •Реакция дезаминирования глутамина
- •Синтез мочевины
- •Реакция синтеза карбамоилфосфата и орнитиновый цикл Синтез аммонийных солей
- •Реакции синтеза аммонийных солей Пути использования аспартата и глутамата
- •Взаимосвязь обмена серина, глицина, метионина и цистеина Пути использования цистеина
- •Пути использования цистеина
- •Реакции синтеза таурина Обмен фенилаланина и тирозина
- •Нарушение обмена Аминокислот
- •Клиническая картина
- •Основы лечения
- •Клиническая картина
- •Цистиноз ранний нефропатический
- •Цистиноз нефропатический поздний
- •Цистиноз доброкачественный взрослых
- •Основы лечения
- •Клиническая картина
- •Основы лечения
- •Изовалератацидемия
- •Нарушение обмена триптофана
- •Основы лечения
Взаимосвязь обмена серина, глицина, метионина и цистеина Пути использования цистеина
Цистеин является чрезвычайно важной аминокислотой в связи с тем, что это единственный источник органической серы для клеток организма. В результате реакций метаболизма эта сера переходит в состав других серусодержащих веществ – фосфоаденозинфосфосерная кислота (ФАФС),коэнзим А, глутатион, сульфированные производные углеводов (хондроитинсульфат, кератансульфат, дерматансульфат) или выводится почками в виде сульфатов.
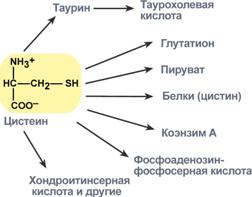
Пути использования цистеина
Одним из производных цистеина является таурин, обладающий следующими функциями:
является обязательным компонентом желчных кислот
играет роль внутриклеточного антиоксиданта,
есть данные о функции таурина как тормозного нейромедиатора.
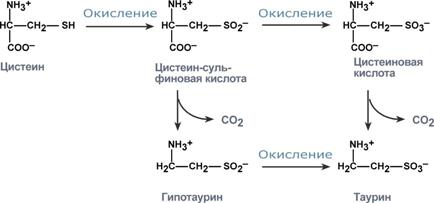
Реакции синтеза таурина Обмен фенилаланина и тирозина
В организме фенилаланин используется только в синтезе белков. Весь неиспользованный запас аминокислоты превращается в тирозин. В этом непосредственно участвует фермент фенилаланин-4-монооксигеназа, обеспечивающий окисление ароматического кольца. Коферменттетрагидробиоптерин в реакции окисляется до дигидроформы. Восстановление кофермента осуществляет дигидробиоптерин-редуктаза с своим коферментом НАДФН.
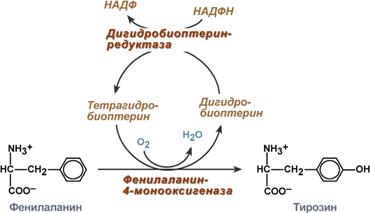
Реакция превращения фенилаланина в тирозин
Тирозин, помимо участия в синтезе белков, является предшественником гормона надпочечников адреналина, медиаторов норадреналина и дофамина, гормонов щитовидной железы тироксина и трийодтиронина и пигментов.

Пути превращения тирозина
Нарушение обмена Аминокислот
Нарушения обмена фенилаланина
Фенилаланин относится к незаменимым аминокислотам, поскольку ткани животных не обладают способностью синтезировать его бензольное кольцо. При любых нарушениях превращения его в тирозин развивается фенилкетонурия.
По Mc Kusick выделяется несколько типов фенилкетонурии: классическая (1 типа), вариантная (2 типа), 3 типа, материнская.
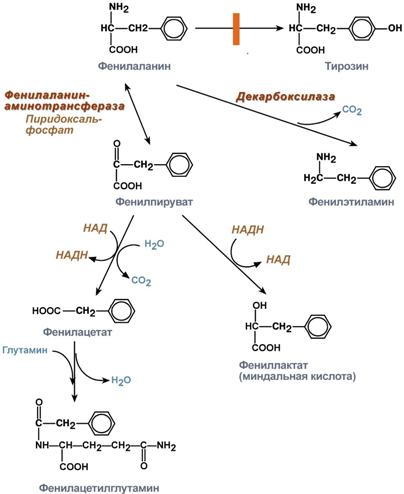
Превращение фенилаланина при фенилкетонурии
Фенилкетонурия 1 типа (классическая)
Фенилкетонурия 1 типа является наиболее распространенной аминоацидопатией. Частота ФКУ среди новорожденных по данным массового скрининга в различных странах составляет в среднем 1:10000, однако значительно варьирует в зависимости от популяции: от 1:4560 в Ирландии, до 1:100000 в Японии.
Этиология
Заболевание наследуется аутосомно-рецессивно и вызвано мутацией, которая вызывает снижение активности фермента фенилаланин-4-монооксигеназы, обеспечивающей превращение фенилаланина в тирозин. Фермент имеется только в печени, почках, поджелудочной железе.
Патогенез
В патогенезе ФКУ имеют значение многие обстоятельства, в частности:
значительное накопление в тканях и жидкостях больного организма фенилаланина и его производных (фенилпировиноградная, фенилмолочная (миндальная), фенилуксусная, гиппуровая кислоты, фенилэтиламин, фенилацетилглютамин) и вызванный ими ацидоз,
прямое токсическое действие указанных веществ на центральную нервную систему, которое заключается в торможении фенилаланиномактивности ряда ферментов, в том числе пируваткиназы (окисление глюкозы), тирозиназы (синтез меланина), тирозин-гидроксилазы (синтез катехоламинов) и нарушение синтеза моноаминовых нейромедиаторов – тирамина, октопамина,
нарушение синтеза серотонина, т.к. фенилаланин-4-монооксигеназа одновременно осуществляет гидроксилирование триптофана до 5-гидрокситриптофана, предшественника серотонина,
конкурентное снижение фенилаланином транспорта в клетки ароматических аминокислот – триптофана и тирозина,
нарушение синтеза простых и сложных белков в тканях, что вызывает тяжелые повреждения мозга и нарушение функции печени у большинства больных.
