- •Аминокислоты используются в качестве лекарств
- •Аминокислоты объединяют по разным признакам
- •Классификация аминокислот
- •Двадцать аминокислот необходимы для синтеза белка
- •Строение протеиногенных аминокислот
- •Право- и левовращающие формы аланина
- •Для аминокислот характерна амфотерность
- •Изменение заряда аминокислот при смещении рН раствора в кислую или щелочную сторону. Аминокислоты соединяются пептидной связью
- •Пути превращений аминокислот по боковой цепи
- •Серотонин
- •Реакции синтеза серотонина
- •Аминокислоты надо переносить через мембраны
- •Транспорт аминокислот через мембраны Вторичный активный транспорт
- •Вторичный активный транспорт аминокислот через мембраны
- •Глутатионовая система транспорта
- •Транспорт аминокислот при участии глутатиона
- •Аминокислоты могут давать энергию
- •Катаболизм аминокислот начинается с удаления аминогруппы
- •Прямое окислительное дезаминирование
- •Реакция, катализируемая оксидазами d- и l-аминокислот
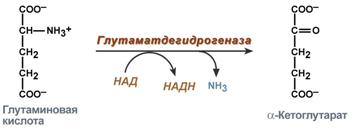
- •Реакция прямого окислительного дезаминирования глутаминовой кислоты
- •Непрямое окислительное дезаминирование (трансдезаминирование)
- •Трансаминирование нуждается в витамине в6
- •Механизм реакции трансаминирования
- •Реакции полного цикла трансаминирования
- •Аминотрансферазы имеют клиническое значение
- •Реакции, катализируемые аланинаминотрансферазой и аспартатаминотрансферазой
- •Креатинфосфат - срочный резерв энергии
- •Использование креатинфосфата для ресинтеза атф
- •Образование креатинина из креатинфосфата
- •Реакции синтеза креатина в почках и печени
- •Синтез креатинфосфата
- •В мышце дезаминирование аминокислот идет особым образом
- •Реакции непрямого дезаминирования аминокислот в мышечной ткани
- •В клетках постоянно образуется аммиак
- •Основные источники аммиака
- •Связывание аммиака
- •Реакция синтеза глутаминовой кислоты
- •Реакция синтеза глутамина
- •Реакция синтеза аспарагина
- •Транспорт аммиака
- •Глюкозо-аланиновый цикл
- •Реакции глюкозо-аланинового цикла (выделен рамкой).
- •Накопление аммиака представляет проблему
- •Гипотезы токсичности аммиака
- •Наследственные и приобретенные формы гипераммониемий Приобретенные формы
- •Наследственные формы
- •Для удаления аммиака есть два способа
- •Реакция дезаминирования глутамина
- •Синтез мочевины
- •Реакция синтеза карбамоилфосфата и орнитиновый цикл Синтез аммонийных солей
- •Реакции синтеза аммонийных солей Пути использования аспартата и глутамата
- •Взаимосвязь обмена серина, глицина, метионина и цистеина Пути использования цистеина
- •Пути использования цистеина
- •Реакции синтеза таурина Обмен фенилаланина и тирозина
- •Нарушение обмена Аминокислот
- •Клиническая картина
- •Основы лечения
- •Клиническая картина
- •Цистиноз ранний нефропатический
- •Цистиноз нефропатический поздний
- •Цистиноз доброкачественный взрослых
- •Основы лечения
- •Клиническая картина
- •Основы лечения
- •Изовалератацидемия
- •Нарушение обмена триптофана
- •Основы лечения
Аминокислоты надо переносить через мембраны
Перенос аминокислот через мембраны клеток, как при всасывании из полости кишечника в энтероциты, так и при переходе из крови в клетки различных тканей, осуществляется при помощи двух механизмов: вторичный активный транспорт и глутатионовая транспортная система.
Транспорт аминокислот через мембраны Вторичный активный транспорт
Вторичный активный транспорт – это перенос веществ, в данном случае аминокислот, с использованием градиента концентрации натрия между внутренней и наружной сторонами клеточной мембраны.
Вторичный активный транспорт основан на использовании низкой концентрации ионов натрия внутри клеток, создаваемой мембранным ферментом Na+,K+-АТФазой. Специфический белок-транспортер связывает на апикальной поверхности энтероцитов аминокислоту и ион натрия. Важно то, что в отсутствие натрия аминокислота не в состоянии связаться с белком-переносчиком.
Затем, изменив свое положение в мембране, белок отдает ион натрия в цитозоль по градиенту концентрации. Сразу после этого аминокислота теряет связь с белком и остается в цитоплазме.
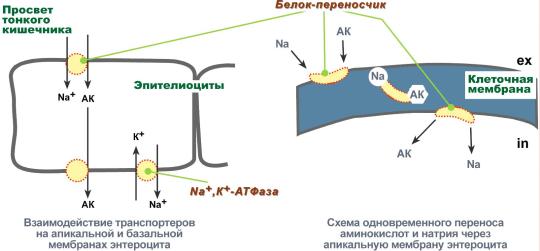
Вторичный активный транспорт аминокислот через мембраны
В настоящее время выделяют 5 транспортных систем:
для крупных нейтральных, в том числе алифатических и ароматических аминокислот,
для малых нейтральных – аланина, серина, треонина,
для основных аминокислот – аргинина и лизина,
для кислых аминокислот – аспартата и глутамата,
для малых аминокислот – глицина, пролина и оксипролина.
Глутатионовая система транспорта
Второй способ переноса аминокислот внутрь клетки происходит в комплексе с глутатионом при помощи фермента γ-глутамилтрансферазы.
.
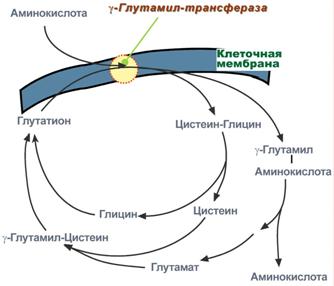
Транспорт аминокислот при участии глутатиона
Переносчиком некоторых аминокислот (обычно нейтральных) по этой схеме является трипептид глутатион (γ-глутамилцистеилглицин). При взаимодействии глутатиона с аминокислотой на внешней стороне клеточной мембраны при участии глутамилтрансферазы. γ-Глутамильный остаток связывает аминокислоту и происходит ее перемещение внутрь клетки. Глутатион при этом распадается на составляющие. После отделения аминокислоты происходит ресинтез глутатиона.
Аминокислоты могут давать энергию
(см. выше)
Нейромедиаторы образуются из аминокислот(см. выше)
Существуют 4 типа дезаминирования (см выше)
Катаболизм аминокислот начинается с удаления аминогруппы
У человека основным способом дезаминирования является окислительное дезаминирование. Выделяют два варианта окислительного дезаминирования: прямое и непрямое.
Прямое окислительное дезаминирование
Прямое дезаминирование катализируется одним ферментом, в результате образуется NH3 и кетокислота. Прямое окислительное дезаминирование может идти в присутствии кислорода (аэробное) и не нуждаться в кислороде (анаэробное).
1. Аэробное прямое окислительное дезаминирование катализируется оксидазами D-аминокислот (D-оксидазы) в качестве кофермента использующими ФАД, и оксидазами L-аминокислот (L-оксидазы) с коферментом ФМН. В организме человека эти ферменты присутствуют, но практически неактивны.

Реакция, катализируемая оксидазами d- и l-аминокислот
2. Анаэробное прямое окислительное дезаминирование существует только для глутаминовой кислоты, катализируется толькоглутаматдегидрогеназой, превращающей глутамат в α-кетоглутарат. Фермент глутаматдегидрогеназа имеется в митохондриях всех клеток организма (кроме мышечных). Этот тип дезаминирования теснейшим образом связан с трансаминированием аминокислот и формирует с ним процесстрансдезаминирования (см ниже).