
- •Билет 11
- •Зависимость скорости реакции от рН
- •Билет 13.
- •Билет 14.
- •Билет 17
- •Энзимопатии, возникающие при в6 дефиците.
- •Билет 22.
- •Билет 27.
- •Билет 28.
- •Билет 31.
- •Билет 32.
- •Билет 33.
- •Билет 34
- •Биологическая ценность белков.
- •Пути превращения аминокислот в печени.
- •Синтез аминокислот
- •Декарбоксилирование аминокислот.
- •Пути обезвреживания аммиака.
- •Энергетическая цена синтеза мочевины
- •Креатин Креатинфосфат
- •Обмен цистеина и метионина.
- •Функции цистеина:
- •Обмен фенилаланина и тирозина.
- •Синтез катехоламинов (адреналина, норадреналина)
- •Синтез тироксина
- •Обмен триптофана.
- •Биосинтез мелатонина.
- •Структура и свойства нуклеопротеидов.
- •Виды нуклеиновых кислот
- •Структура нуклеопротеидов.
- •Нуклеиновые кислоты.
- •Обмен нуклеотидов.
- •Распад пуриновых оснований.
- •Распад пиримидиновых оснований.
- •Распад пуриновых оснований.
- •Метаболизм белково-пептидных гормонов.
- •Пути экскреции гормонов и их метаболитов.
- •Биосинтез мелатонина.
- •Метаболизм аминокислотных гормонов.
- •Метаболизм тиреоидных гормонов.
- •Метаболизм мелатонина.
- •Пути экскреции гормонов и их метаболитов.
- •Регуляция обмена белков.
- •Этапы синтеза стероидных гормонов.
- •Транспорт гормонов.
- •Специфические транспортные белки плазмы крови.
- •Неспецифические белки.
- •Физиологическая роль связывания гормонов в крови.
- •Периферический метаболизм гормонов.
- •Виды метаболизма:
- •Регуляция обмена белков.
- •Этапы действия стг.
- •Этапы действия инсулина.
- •Половые гормоны.
- •Регуляция водно-солевого обмена.
- •Гормональная регуляция обмена кальция.
- •Функции кальция.
- •Билет 80. Витамины.
- •Функции витаминов.
- •Этапы нарушений обмена витаминов.
- •Диагностика гиповитаминозов
- •Причины возникновения и коррекция авитаминозов.
- •Причины нарушений обмена витаминов
- •Авитаминоз, гиповитаминоз.
- •Причины возникновения гиповитаминозов.
- •Клиническая картина гиповитаминозов.
- •Определение недостатка витаминов.
- •Биохимические принципы витаминотерапии
- •Нарушение обмена в1.
- •Витамин в5(рр).
- •Примеры реакций.
- •Патология обмена витамина в5.
- •Витамин в2 – рибофлавин.
- •Практической применение в2.
- •Обмен витамина в3 (пантотеновая кислота).
- •Витамин в6.
- •Витамин в6 участвует в обмене триптофана.
- •Энзимопатии, возникающие при в6 дефиците.
- •Обмен витамина н (биотин).
- •Врожденная пропионатацидемия.
- •Фолиевая кислота – витамин в9, Вс.
- •Нарушения обмена фолиевой кислоты.
- •Витамин в12-кобаламин.
- •Нарушения обмена витамина в12.
- •Аскорбиновая кислота (витамин с).
- •Нарушения обмена витамина с.
- •Функции витамина а.
- •Нарушения обмена витамина а.
- •Витамин е (токоферолы).
- •Витамин d.
- •Функции витамина d.
- •Механизм действия витамина d.
- •Нарушение обмена витамина d.
- •Врожденные нарушения обмена витамина d.
- •Витамин к.
- •Функции витамина к.
- •Белки плазмы крови.
- •Высаливание.
- •Функции белков плазмы крови.
- •Альбумины.
- •Строение гемоглобина.
- •Аномальные типы гемоглобина
- •Патология обмена гемоглобина.
- •Порфирии.
- •Синтез гема.
- •-Глобулины.
- •Билет 97. Биохимия печени
- •Билет 98
Билет 33.
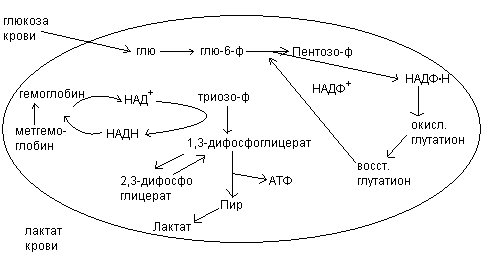
Обмен углеводов в эритроцитах.
Эритроциты не содержат ядра, митохондрий. В эритроците не идут реакции цикла лимонной кислоты, в них нет ферментов дыхательной цепи. Парадоксальным является тот факт, что эритроцит, перенося кислород для тканей, сам его не использует и получает энергию за счет аэробных процессов.
Основным процессом в эритроцитах, который дает энергию, является анаэробный гликолиз. При расщеплении фру-6-фф образуется НАДН, необходимый для восстановления избытка метгемоглобина (окисленной формы гемоглобина, не связывающей О2).
Побочным продуктом гликолиза в эритроцитах является 2,3-дифосфоглицерат. 2,3-дифосфоглицерат связывается с гемоглобином, уменьшает его сродство к О2 и, облегчает освобождение кислорода в тканях.
Фосфоглюконатный путь в норме составляет лишь небольшую долю в катаболизме глюкозы. В условиях повышенной потребности в НАДФ.Н этот процесс активизируется. НАДФ.Н необходим для того, чтобы поддерживать внутриклеточный восстановитель, глутатион, в его восстановленной SH-форме. Воздействие агентов, ускоряющих окисление глутатиона в S-S-форму, активирует реакции пентофосфотного пути, которые обеспечивают образование восстановленных эквивалентов в форме НАДФ.Н.
Обмен углеводов в эритроцитах.
Гемолитические анемии.
Гликолиз в эритроцитах и транспорт кислорода связаны участием в обеих процессах 2,3-дифосфоглицерата. 2,3-дифосфоглицерат снижает сродство гемоглобина к кислороду и облегчает освобождение О2 в тканях.
При дефекте гексокиназы снижается концентрация промежуточных продуктов гликолиза, в том числе снижается концентрация 2,3-дифосфоглицерата. В таких эритроцитах гемоглобин обладает очень высоким сродством с О2. Наступает гемолиз эритроцитов, когда гемоглобин плохо обдает О2.
При дефекте пируваткиназы нарушается энергетический обмен и мембрана не получает энергию, необходимую для ионного обмена и наряду с этим образуется избыток 2,3-дифосфоглицерата и связь с О2 становится слабой, сродство гемоглобина к О2 становится низким.
Глю Глю-6-ф Фру-6-ф Фру-1,6-дф 3ФГА
 1,3-ДФГК
3-ФГК
2-ФГК
ФЭП
Пир
Лак
1,3-ДФГК
3-ФГК
2-ФГК
ФЭП
Пир
Лак
![]()
2,3-ДФГК
2,3-ДФГК снижает сродство Hb к О2
Недостаточность глюкозо-6-фосфотдегидрогеназы – причина лекарственной гемолитической анемии.
У ряда больных малярией применение противомалярийного препарата памахина сопровождается гемолитической анемией. Через 30 лет после начала применения препарата была выяснена причина анемии. Было установлено, что возникновение анемии связано с недостаточностью глюкозо-6-фосфатдегидрогеназы в эритроцитах. В результате недостаточности фермента нарушается образование НАДФН в пентозофосфатном пути. Главная роль НАДФН в эритроцитах состоит в восстановлении дисульфидной формы глутатиона в сульфгидрильную форму.
Г-S-S-Г + НАДФН + Н+ Г-SH +НАДФ+
Восстановленная форма глутатиона обеспечивает обезвреживание перекиси и органических перекисей:
2 Г-SH + R-O-OH Г-S-S-Г + Н2О + ROH
Клетки со сниженным содержанием восстановленного глутатиона обладают повышенной чувствительностью к гемолизу. Возможно, что в отсутствие восстановленного глутатиона памахин и ряд других лекарственных препаратов, вызывают изменения поверхности мембраны эритроцитов за счет образования токсических перекисей.
Недостаточность глюкозо-6-фосфатдегидрогеназы в эритроцитах, по-видимому, обуславливает устойчивость к тропической малярии, т.к. для роста возбудителя необходим нормально функционирующий пентозный путь и восстановленный глутатион. Дефект фермента распространен в тех странах, где распространена малярия. Такая наследуемая недостаточность фермента может быть относительно безвредной, до тех пор, пока не вводятся определенные лекарства.
