
- •Методы исследования свойств и продуктов питания
- •Методы исследования свойств сырья и продуктов питания
- •ВвЕдение
- •1. Измерения и их классификация
- •1.1. Единицы измерения величин
- •1.2. Системы единиц
- •Кратные и дольные единицы по гост 1052-78
- •2. Статистический анализ измерений
- •2.1. Погрешности приближенных величин
- •2.2. Математическая статистика измерений
- •2.2.1. Параметры точности ряда измерений
- •Интегральная функция Лапласа
- •2.2.2. Анализ результатов экспериментов
- •2.3. Нахождение оптимальных параметров, применение методов планирования экспериментов
- •2.3.1. Схема Зайделя–Гаусса
- •2.3.2. Метод Бокса
- •2.3.3. Нахождение оптимальных параметров с помощью эвм
- •2.3.4. Пример оптимизации процесса приготовления пивного сусла
- •Матрица экспериментальных данных
- •2.3.5. Пример оптимизации использования питательной среды при культивировании пекарских дрожжей
- •Матрица экспериментальных данных
- •2.3.6. Аппроксимация экспериментальных данных
- •3. Отбор проб сырья, полуфабрикатов и пищевых продуктов для проведения исследований
- •3.1. Отбор проб сыпучих продуктов
- •3.1.1. Отбор проб из вагонов
- •3.1.2.Отбор проб из автомашин
- •3.1.3. Отбор проб из танкеров и барж
- •Размеры проб
- •3.1.4. Отбор проб от партии затаренных сыпучих продуктов
- •3.2. Отбор проб сыпучих продуктов при хранении
- •3.2.1. Отбор проб из бунтов
- •3.2.2. Отбор проб из силосов элеваторов
- •3.2.3. Отбор проб в производстве
- •4. Приемы подготовки проб к анализу
- •4.1. Подсушивание (высушивание)
- •4.2. Измельчение
- •4.2.1. Ступки
- •4.2.2. Терочные машины
- •4.2.3. Дисковые мельницы
- •4.2.4. Фрезерные измельчители
- •4.2.5. Комбинированные мельницы
- •4.2.6. Измельчители в жидкой среде
- •4.2.7. Выбор типа измельчительных устройств
- •4.3. Извлечение растворимых компонентов из твердых и пластичных материалов
- •4.3.1. Отжим
- •4.3.2. Извлечение растворителями
- •4.3.3. Специальные приемы извлечения растворимых компонентов
- •4.4. Разделение смеси различных веществ на компоненты
- •4.4.1. Простая перегонка
- •4.4.2. Ректификация
- •4.4.3. Молекулярная перегонка
- •4.4.4. Фракционирование кристаллизацией из растворов
- •5. Измерение кислотности и окислительно-восстановительного потенциала
- •5.1. Определение активной кислотности
- •5.2. Электрометрический метод определения рН
- •5.3. Определение рН при помощи рН-метра марки лпу-01
- •5.4. Колориметрический метод определения рН
- •Характеристика индикаторов для определения рН
- •5.5. Определение титруемой кислотности
- •5.5.1. Титрование с помощью индикаторов
- •5.5.2. Электрометрическое титрование
- •5.6. Определение окислительно-восстановительного потенциала
- •5.6.1. Электрометрический метод
- •5.6.2. Колориметрический метод
- •6. Рефрактометрия
- •6.1. Измерение показателя преломления
- •6.2. Измерения с помощью рефрактометров
- •6.3. Прецизионный рефрактометр
- •6.4. Погружаемый рефрактометр
- •7. Поляриметрия
- •7.1. Устройство поляриметров
- •Удельные вращения сахаров
- •7.2. Приготовление и осветление раствора анализируемого продукта
- •7.3. Методы поляриметрического определения
- •7.4. Определение крахмала методом Эверса
- •8. Колориметрия
- •8.1. Визуальные методы
- •8.2. Фотоэлектрический метод
- •Характеристика светофильтров спектрофотометров фэк-56
- •8.3. Люминесцентный анализ
- •8.3.1. Техника эксперимента и общие приемы анализа
- •8.3.2. Применение люминесцентного анализа в исследовании пищевых продуктов
- •8.4. Цвет и его измерение
- •8.4.1.Общие понятия и приемы измерения цвета
- •8.4.2. Методики определения цветности пищевых продуктов
- •Приготовление серии растворов йода
- •9. Хроматография
- •9.1. Адсорбционная молекулярная хроматография
- •9.2. Распределительная хроматография
- •9.2.1. Хроматография на бумаге
- •9.2.2. Хроматография на колонках
- •9.2.3. Газожидкостная хроматография
- •Характеристика неподвижной фазы
- •10. Электрофорез
- •11. Спектроскопия
- •11.1. Общие понятия и терминология
- •11.2. Эмиссионный спектральный анализ
- •11.3. Анализ элементов методом пламенной фотометрии
- •11.4. Анализ элементов в дуге
- •12. Молекулярный спектральный анализ
- •12.1. Общие сведения об электронных спектрах молекул
- •12.2. Приборы для регистрации электронных спектров поглощения и техника эксперимента
- •12.2.1. Ультрафиолетовая область
- •12.2.2. Видимая область
- •12.2.3. Использование инфракрасных спектров поглощения
- •12.3. Количественный анализ по спектрам поглощения в ультрафиолетовой, видимой и инфракрасной областях спектра
- •12.3.1. Анализ однокомпонентной смеси
- •12.3.2. Анализ двухкомпонентной смеси
- •13. Масс-спектРометрия
- •14. Спектроскопия электронного парамагнитного и ядерного магнитного резонанса
- •14.1. Электронный парамагнитный резонанс
- •14.2. Ядерный магнитный резонанс
- •Контрольные вопросы
- •Список рекомендуемой литературы
- •Содержание
- •Методы исследования свойств сырья и продуктов питания
8.3.1. Техника эксперимента и общие приемы анализа
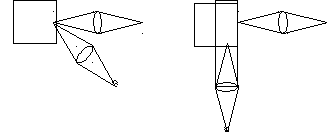
Рассмотрим принципиальные схемы для возбуждения и наблюдения флуоресценции (рис. 8.2). Источник света 1 проходит через светофильтр 2 и направляется кварцевым конденсором 3 на кварцевую кювету с образ- цом 4. Свет флуоресценции направляется стеклянным конденсором 5 на приемник 6. Приемником могут служить глаз (визуальный метод регистрации), фотопластинка или фотометр (объективные методы регистрации). При наблюдении спектров перед приемником ставят спектральный прибор. Наиболее часто используется схема, в которой возбуждающий свет направляется под углом 45° к поверхности кюветы. Если анализируемое вещество не сильно поглощает возбуждающий свет, то можно направлять луч вдоль передней стенки кюветы.
 4
5 6 4
5 6
4
5 6 4
5 6



3
3
2 1 2
1
Рис. 8.2. Принципиальная схема флуорометра:
1 – источник освещения; 2 – светофильтр; 3, 5 – конденсоры; 4 – кювета с исследуемым веществом; 6 – приемник
При количественном анализе измерения выхода флуоресценции обычно не производят, а пользуются методом сравнения интенсивности свечения анализируемого вещества с интенсивностью свечения стандартного раствора. Эти измерения удобнее производить при помощи флуорометров, построенных по двулучевой схеме.
Люминесцентный анализ можно проводить: по измерению интенсивности свечения и по изменению степени тушения флуоресценции вещества при добавлении определенного количества тушителя.
При количественном анализе в обоих случаях выбирают оптимальные условия для наблюдения флуоресценции, устанавливают интервал концентраций, в котором выход флуоресценции линейно зависит от концентрации, и составляют градировочную кривую на основании результатов измерения флуоресценции стандартных растворов анализируемого вещества.
8.3.2. Применение люминесцентного анализа в исследовании пищевых продуктов
Каротиноиды обладают флуоресценцией желто-зеленого цвета. Это свойство обычно используют при идентификации хроматограмм.
Пигменты группы хлорофилла обладают интенсивной флуоресценцией темно-красного цвета. В чистых и сухих органических растворителях они флуоресцируют слабо. Флуоресценция резко усиливается при наличии воды, спирта, аминов. По спектру флуоресценции можно определить присутствие ≈ 1 мкг/л хлорофилла. Водорастворимые производные по флуоресценции мало отличаются от хлорофилла.
Свободные формы токоферолов интенсивно флуоресцируют в ультрафиолетовой области при длине волны 340 нм под влиянием возбуждающего света с длиной волны 295 нм. Связанные формы токоферолов можно перевести в свободные обработкой пробы LiАlН4. Выход флуоресценции α-, β- и δ-токоферолов (в расчете на моль вещества) меняется так же, как и их молярные коэффициенты поглощения. Чувствительность метода около 0,005 мкг/мл. Присутствие витамина А не мешает определению токоферола.
Некоторые водорастворимые витамины обладают интенсивной флуоресценцией. Нейтральные растворы рибофлавина (В2) в воде и спирте флуоресцируют желто-зеленым светом (λmax = 535 нм). Выход флуоресценции падает при наличии кислот и щелочей. Эти свойства используются в различных вариантах люминесцентного метода определения витамина В2 в пищевых продуктах. Чувствительность метода составляет в среднем 0,05 мкг/мл.
Витамин В1 определяют по свечению продукта его окисления красной кровяной солью – тиохромом, имеющим интенсивную флуоресцен- цию голубого цвета (λ = 460…470 нм) при возбуждении светом около 260…277 нм.
Амид никотиновой кислоты имеет голубую флуоресценцию, так же, как и продукты окисления фолиевой кислоты.
Растворы аминокислот – фенилаланина, триозина, триптофана – обладают интенсивной флуоресценцией при 282, 303, 348…359 нм соответственно. Алифатические и серосодержащие кислоты и гистидин не люминесцируют.
Люминесценция белков обусловлена наличием в них ароматических кислот. Однако их спектры несколько отличаются от спектров флуоресценции свободных аминокислот. Положение полос может также меняться при изменении рН среды и степени денатурации белка.
Проведению анализа по спектрам флуоресценции предшествует сложная обработка пробы в целях концентрирования и выделения этого типа соединений, а также разделения их на группы.
В настоящее время уделяется очень большое внимание изучению этих соединений, так как полициклические соединения и, особенно, 3,4-бенз-пирен обладают канцерогенными свойствами. Чувствительность метода 10–3 мкг 3,4-бензпирена в 1 кг продукта.
Люминесцентный анализ широко применяется для идентификации компонентов, получающихся при хроматографии. Так, свечение продуктов реакции фосфолипидов с родамином используется для идентификации фосфатидных фракций при их бумажной и тонкослойной хроматографии. Высокая чувствительность люминесцентных индикаторов позволяет использовать их при титровании очень разбавленных растворов мутных или окрашенных сред. Титрование проводят в темном помещении при освещении пробы с помощью ультрафиолетового осветителя с фильтром, поглощающим видимый свет.
