
- •Вопрос 2. Кинематика вращательного движения. Угловая скорость, угловое ускорение. Связь линейных и угловых величин. Псевдовекторы.
- •Вопрос3. Масса, свойство массы. Сила. Инерция. Первый закон Ньютона.
- •Вопрос 6. Энергия. Кинетическая , потенциальная энергия. Закон сохранения энергии.
- •Вопрос 5. Работа силы в механике. Работа силы тяжести, работа силы упругости.
- •Вопрос 7. Идеальный газ. Уравнение Менделеева-Клаперона. Плотность, концентрация молекул. Закон Дальтона.
- •Вопрос 8. Основное уравнение молекулярно кинетической энергии. Следствие. Средняя энергия поступательного движения, средняя квадратичная скорость.
- •Вопрос 14.
- •Вопрос 12.
- •Вопрос 13. Закон Максвелла для распределения молекул идеального газа по скоростям. Анализ функции распределения.
- •Вопрос 9. Степени свободы молекул. Закон равномерного распределения энергии по степеням свободы. Внутренняя энергия газа – функция состояния.
- •Вопрос 10. Первое начало термодинамики. Работа газа в адиабатном и изопроцессах.
- •Вопрос 11. Адиабатный и политропный процессы. Уравнение Пуассона.
- •Вопрос 24. Обратимые и необратимые процессы. Круговой процесс (цикл). Термический кпд цикла. Цикл Карно. Кпд цикла Карно.
- •Вопрос 15. Взаимодействие электрических зарядов. Закон Кулона. Понятие напряженности электрического поля. Напряженность поли точечного заряда. Принцип суперпозиции для электрического поля.
- •Вопрос 16. Поток линий напряженности эл, поля. Теорема остроградского Гаусса. Расчет поля., созданного бесконечно протяженной равномернозаряженной плоскостью.
- •Вопрос 17. Напряженность плоского конденсатора, его электроемкость, энергия заряженного конденсатора.
- •Вопрос 18. Понятие потенциала электростатического поля. Работа по перемещению заряда в электростатическом поле. Понятие разности потенциалов.
- •Вопрос 19. Эквипотенциальные поверхности. Связь напряженности с разностью потенциалов. Расчет разности потенциалов в однородном поле.
- •Вопрос 21. Неоднородный участок цепи, понятие электродвижущей силы, действующей на участок цепи. Падение напряжения. Закон Ома для замкнутого контура.
- •Вопрос 22. Закон Джоуля-Ленца,. Работа тока. Кпд источника тока.
- •Вопрос 23. Расчет разветвленных цепей. Правило Киргофа.
- •1 Закон
- •2 Закон
- •Вопрос 24. Магнитное поле тока. Его характеристика. Изображение магнитных полей. Понятие потока линий магнитной индукции. Теорема Гаусса для магнитного поля.
- •Вопрос 25. Закон Био-Савара-Лапласо в вакууме. Расчет магнитного поля, созданого линейным отрезком проводника с током. Поле от бесконечно длинного проводника с током.
- •Вопрос 26. Индукция магнитного поля в центре кругового тока.
- •Вопрос 27. Циркуляция вектора индукции магнитного поля в вакууме. Магнитное поле бесконечно длинного соленоида.
- •Вопрос 28. Действие магнитного поля на проводник с током-сила Ампера. Взаимодействие бесконечно длинных проводников с током. Единица тока 1а.
- •Вопрос 29. Сила Лоренца. Действие частицы по окружности, радиус окружности, период вращения частицы.
- •Вопрос 30. Явление электро магнитной индукции. Закон Фарадея и Ленца. Принцип действия генератора пременного тока. Тока Фуко.
- •Вопрос 31. Явление самоиндукции. Полный магнитный поток. Индуктивность контуров. Эдс самоиндукции. Экстратоки замыкания и размыкания.
- •Вопрос 32. Гармонические колебания, их характеристики. Пружинный, физический маятники. Сложение колебаний.
- •Вопрос 33. Волновое движение. Уравнение плоской упругой волны. Длина волны. Фазовая скорость.
- •Вопрос 34. Электромагнитные волны. Свойства. Интенсивность волн.
- •Вопрос 35. Интерференция волн. Оптическая разность хода. Усломия максимумов и минимумов волн. Интерференция света в тонких пленках. Просветление оптики.
- •Вопрос 36. Дифракция света. Дифракционная решетка, дифракция от решетки.
- •Вопрос 37. Фотоны, их энергия, масса, импульс. Внешний фотоэффект. Его законы. Уравнение Эйнштейна. Объяснение законов внешнего фотоэффекта.
- •Вопрос 38. Тепловое излучение. Абсолютно чёрное тело. Законы теплового излучения абсолютно черного тела. Давление света
- •Вопрос 39. Строение атома. Постулаты Бора. Атом водорода по Бору. Квантование радиуса орбиты электрона в атоме. Квантование энергии. Сериальная формула.
- •Вопрос 40. Строение ядра. Ядерные силы. Энергия связи ядра, удельная энергия связи ядра.
- •Вопрос 41. Радиоактивность ядер. Законы распада ядер. Активность распада.
- •Вопрос 42. Ядерные реакции с выделением энергии. Ядерная энергетика.
Вопрос 9. Степени свободы молекул. Закон равномерного распределения энергии по степеням свободы. Внутренняя энергия газа – функция состояния.
Число степеней свободы тела называется наименьшее число независимых координат, которые необходимо задать для того чтобы полностью определить положение тела в пространстве.
Материальная точка, свободно движущаяся в пространстве, имеет три координаты (x,y,z) Одноатомную молекулу можно рассматривать как материальную точку и такая молекула имеет только три ст. св. поступательного движения. Двухатомную молекулу можно представить как гантель с невесомой ручкой, такая молекула имеет ещё 2 степени свободы (вращательное движение).
Таблица 1 – Степени свободы молекул газов
|
|
Поступательное движение |
Вращательное движение |
Всего |
|
Одноатомный газ |
3 |
- |
3 |
|
Двухатомный газ |
3 |
2 |
5 |
|
Трехатомный Многоатомный газ |
3 |
3 |
6 |
На
каждую степень свободы молекулы в
среднем приходится одинаковая
кинетическая энергия, равная
 .
Средняя кинетическая энергия молекулы
имеющей
.
Средняя кинетическая энергия молекулы
имеющей степеней свободы равна
степеней свободы равна

При колебательном движении учитывается две степени свободы с учётом потенциальной и кинетической энергии. Колебательные степени свободы учитываются только при T > 1000 K.
Внутренняя энергия состоит:
• Кинетическая энергия теплового, поступательного и вращательного движения молекул
• Кинетической и потенциальной энергии колебания атомов в молекулах
• Потенциальная энергия, обусловленная межмолекулярным взаимодействием
• Энергия электронных оболочек
• Энергия ядра
Внутренняя энергия – функция состояния. Изменение внутренней энергии идеального газа не зависит от процесса, по какому происходит это изменение. Изменение внутренней энергии равно разности внутренней энергии в конечном состоянии и начальном состоянии.


Если пройдя круговой процесс, мы вернем систему в первоначальное состояние, то изменение внутренней энергии равно 0. Поэтому внутренняя энергия является однозначной функцией состояния. Изменить состояние термодинамической системы, т.е. изменить внутреннюю энергию можно двумя способами: совершением работы или передачей теплоты.
Молекулы
воздуха всегда находятся в поле тяготения
Земли, если бы не было хаотического
теплового движения, то они упали бы на
Землю, а если бы не было тяготения –
атмосфера бы рассеялась в космос. Найдём
закон изменения давления идеального
газа в зависимости от высоты в однородном
поле тяготения ( ).
).
Давление
убывает с ростом высоты: p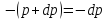











Распределение Больцмана - это распределение концентрации молекул в зависимости от высоты.

 –распределение
концентрации молекул в поле силы тяжести
Земли.
–распределение
концентрации молекул в поле силы тяжести
Земли.
 –потенциальная
энергия одной молекулы в поле тяжести.
–потенциальная
энергия одной молекулы в поле тяжести.
Больцман доказал, что эта формула справедлива в случае потенциального силового поля любой природы для совокупности любых одинаковых частиц, находящихся в состоянии хаотического движения.
Вопрос 10. Первое начало термодинамики. Работа газа в адиабатном и изопроцессах.
Первое начало термодинамики: количество теплоты, сообщенное системе, идет на изменение внутренней энергии системы и на совершение системой работы против внешних сил.

 >0,
если система нагревается.
>0,
если система нагревается.
Работа и теплота зависит от процесса. Работа совершается при изменении объема газа. Работа в термодинамике – обобщенная форма обмена энергией между системой и окружающей средой, в результате чего происходит изменение внешних параметров. Рассчитывает работу. Будем считать, что в сосуде под поршнем находится газ.
Будем считать, что газ двигает поршень очень медленно, что давление внутри газа постоянно. Тогда сила F=pS.
Работа




Работа в изопроцессах
Изотермический (T = const, δA = pdV (δA – элементарная работа))

Изобарный (p = const)
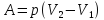
Изохорный
(V
= const,
∆V
= 0)

Адиабатный (∆Q = 0)
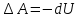


Во
всех процессах:

