
- •Основы составления баланса
- •1. Назначение материальных и энергетических балансов
- •2. Законы сохранения в закрытой системе
- •2.1. Законы сохранения массы в закрытой системе
- •2.2. Закон сохранения энергии в закрытой системе
- •3. Законы сохранения в поточной системе
- •3.1. Понятие поточной системы и виды потоков
- •3.3. Уравнение неразрывности потока
- •3.5. Выражение энергетического баланса в поточной системе
- •Свойства периодических процессов
- •Основные свойства
- •Достоинства непрерывных процессов
- •Причины существования периодических процессов
- •3. Стационарные системы
- •4. Нестационарные системы (процессы)
- •5. Открытые системы
- •Совместимые понятия
- •Несовместимые понятия
- •Классификация систем по фазовому состоянию реагента
- •2. Способы повышения скорости гомогенных процессов.
- •3. Гетерогенные системы
- •6. Методы увеличения скорости гетерогенных процессов
- •Химический катализ.
3.5. Выражение энергетического баланса в поточной системе
![]()
В случае адиабатического режима, то есть в отсутствии теплообмена с окружающей средой, то есть в закрытой системе, закон сохранения энергии записывается в таком выражении.
В левой части – сумма теплоты на входе
В правой части – сумма теплоты на выходе
Точка «●» - отнесено к единице времени.
В поточной системе в случае подвода теплоты из вне и совершения работы, уравнение энергетического баланса примет другой вид.
![]()
Q Q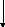

ΣNZhz
ΣNaha
ΣΔН


Q: «+» - приводится теплота
«-» - отводится теплота
L: «+» - над системой совершается работа
«-» - системой совершается работа
Закон сохранения энергии в конечном итоге выглядит так:
![]() -
уравнение энергетического баланса в
поточной системе ( и теплового баланса
так как учтены все источники тепла)
-
уравнение энергетического баланса в
поточной системе ( и теплового баланса
так как учтены все источники тепла)
ΣΔНi – суммарная теплота химических реакций.
Классификация систем и процессов по продолжительности операций
характеристика периодических процессов
характеристика непрерывных процессов
характеристика стационарных процессов
характеристика нестационарных процессов
характеристика открытых и закрытых систем или процессов
1. Периодический процесс – процесс, в котором порции сырья единовременно загружаются в реактор, проходят в нем все стадии обработки до заданной степени превращения, затем выгружаются все образовавшиеся продукты и непрореагировавшее исходное сырье.
Свойства периодических процессов
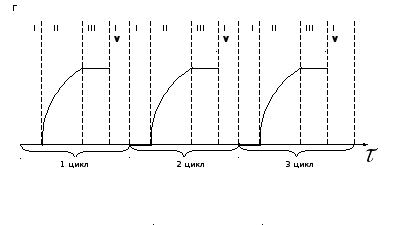
1) технологическая переменная Г (температура, давление, концентрация) являются функцией времени и не являются функцией пространства.
Г
Г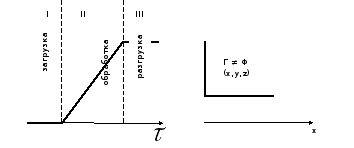

Г
= f
(![]() )
≠ Ф(х,y,z)
)
≠ Ф(х,y,z)
![]()
I – загрузка сырья в реактор
II – химическое превращение сырья конечный продукт
III – разгрузка, удаление конечных продуктов и непрореагировавшего сырья из реактора.
Периодический процесс является частным случаем нестационарного процесса.
Периодический процесс является циклическим

 IV
– простой оборудования, связанный с
чисткой, ремонтом и подготовкой реактора
к следующему циклу.
IV
– простой оборудования, связанный с
чисткой, ремонтом и подготовкой реактора
к следующему циклу.
II – основная стадия
I,III,IV – вспомогательные операции. Продолжительность стадий ≈ одинакова – особенность периодических процессов.
Химические предприятия, работающие в периодическом режиме:
- малотоннажные производства (органических и неорганических химических реактивов, производство лекарственных препаратов, катализаторов, пигментов)
- коксование
- мартеновский способ выплавки стали
2. Непрерывный процесс – процесс, в котором поступление сырья в реактор и выпуск продукции происходит непрерывным потоком в течение длительного времени.
Основные свойства
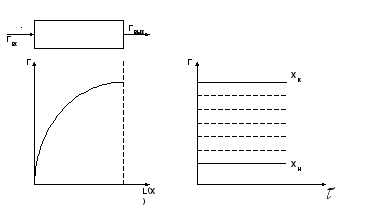
1) Технологическая переменная является функцией пространства и не является функцией времени.

Г
= f(L)
= f
(x,y,z)
![]()
![]()
Определение непрерывного процесса совпадает с определением стационарного процесса, но понятие непрерывного процесса шире, чем понятие стационарного, поскольку может быть непрерывным и нестационарный процесс. В непрерывном процессе стационарным является только установившийся режим. Если говорить о реальных непрерывных процессах в промышленных условиях от различных факторов (изменение состава сырья, изменение атмосферных условий, изменение активности катализатора) непрерывный процесс не всегда является установившимся стационарным процессом.
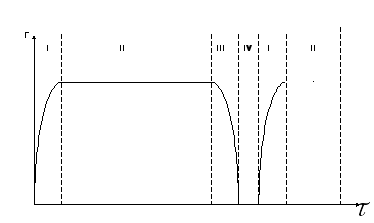

I – пуск установки или процесса
II – установившийся режим – стационарный режим
III – остановка процесса
В зависимости от производства I – стадия может проходить в течение 1-3ч.
Особенность: II – стадия протекает в десятки или сотни раз дольше, чем суммарно I,II и IV.
2) Отсутствие цикличности. Особенность непрерывного процесса является то, что для него характерен как стационарный, так и нестационарный процесс (периоды пуска, остановок, отклонений от установившегося режима за счет изменения внешних факторов).
Примеры непрерывных производств: Хлорирование углеводородов, хлорирование неорганических веществ в печах КИПЯЩЕГО СЛОЯ, крекинг нефтепродуктов, производства кислот, солей, удобрений.
В ряде случаев может быть специально задан непрерывный режим с изменяющимся потоком сырья во времени. Такой процесс является и нестационарным. Существуют полунепрерывные или полупериодические процессы. Это такие процессы, в которых одна из операций осуществляется непрерывно, а другая периодически. Такие процессы являются нестационарными.
Пример: доменный процесс, производство алюминия, магния и так далее.
