
- •1. История развития и современное состояние сталеплавильного производства
- •1.1. Этапы развития сталеплавильного производства
- •1.2. Современный этап сталеплавильного производства
- •2. Физико-химическая характеристика сталеплавильных процессов
- •3. Шлаки (см файл л_б1_шлаки)
- •Физико-химические константы элементов, наиболее часто встречающихся при выплавке стали
- •Основные химические реакции и их тепловые эффекты
- •1) Окисление фосфора в атмосфере:
- •2) Окисление монооксидом железа шлака во время плавки:
- •3.2. Шлакообразование
- •4. Шлаковые системы
- •5. Распределение компонентов между металлом и шлаком
- •6. Основные реакции сталеплавильного процесса
- •6.1. Окисление углерода
- •6.2. Окисление кремния
- •6.3. Окисление марганца
- •6.4. Окисление фосфора
- •7. Газы в сталях
6.3. Окисление марганца
Марганец растворяется в железе в любых соотношениях и образует с железом раствор, близкий к идеальному.
Окисляется марганец при сравнительно низких температурах с образованием оксидов — МnО2, Мn2О3, Мn2О4, МnО.
При высоких температурах устойчивым является только монооксид марганца МnО.
Окисление растворенного в металле марганца может происходить в результате его взаимодействия:
1) с кислородом, растворенным в металле: [Мn] +[О] = (МnО);
2) с кислородом газовой фазы: [Мn] +1/2{O2}= (МnО);
3) с оксидами железа шлака: [Мn] + (FеО) = (МnО) +[Fе].
Все эти реакции сопровождаются выделением тепла.
6.4. Окисление фосфора
Окисление растворенного в металле фосфора может происходить вследствие его взаимодействия:
1) с кислородом газовой фазы: 4/5[P] + {O2} = 2/5(P2O5);
2) с кислородом, растворенном в металле: 4/5[P] + 2[O] = 2/5(P2O5);
3) с кислородом, содержащимся в оксидах железа шлака:
4/5[P] +2(FеО) = 2/5(Р2O5) +2[Fе].
Все реакции сопровождаются выделением тепла.
Процессу окисления фосфора способствует повышение окислености шлака, а вот снижение активности оксидов железа в шлаке затрудняет протекание этого процесса.
7. Газы в сталях
В обычных условиях выплавки невозможно получить сталь, не содержащую газы – азот и водород.
Это связано с тем, что
во-первых, любой материал, применяемый для плавки стали, содержит газы;
во-вторых, по ходу обычной открытой плавки неизбежен контакт металла с газовой фазой, содержащей азот и водород или водяные пары, и может растворять их.
Растворение азота и водорода в железе подчиняется общей закономерности – закону квадратного корня: равновесное содержание газа в жидкой стали пропорционально корню квадратному из парциального давления его в газовой фазе.
Закон установлен немецким исследователем Сивертсом.
Математически этот закон выражается уравнением
![]()
где [Г] – содержание газа (азота или водорода) в железе;
 – парциальное
давление его в газовой фазе;
– парциальное
давление его в газовой фазе;
![]() – коэффициент
пропорциональности (константа
растворения), при 1600 оС
– коэффициент
пропорциональности (константа
растворения), при 1600 оС
![]() ,
,![]() .
.
Таким
образом получаем:
![]() ;
;
![]() .
.
На константу растворения оказывают влияние различные примеси. Эти примеси можно разделить на три группы:
повышающие
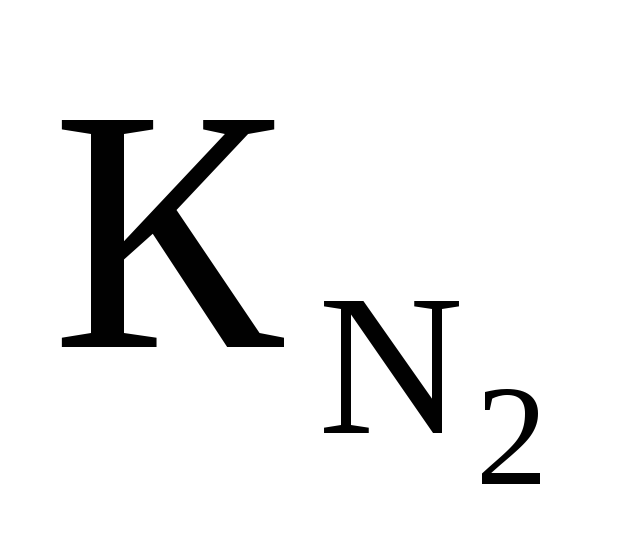 (V,
Nb,
Cr,
Ta)
;
(V,
Nb,
Cr,
Ta)
; (РЗМ,
Ti,
V,
Nb,
Cr);
(РЗМ,
Ti,
V,
Nb,
Cr);снижающие
 (С,
Si)
;
(С,
Si)
; (C,
B,
Si,
Al);
(C,
B,
Si,
Al);не изменяющие
 (Mn,
Mo, W, Cu, Ni, Co)
;
(Mn,
Mo, W, Cu, Ni, Co)
; (
Mn, Mo, Cu, Ni, Co);
(
Mn, Mo, Cu, Ni, Co);
Важной общей закономерностью поведения газов является следующая: растворимость газов в металле изменяется скачкообразно при переходе из жидкого состояния в твердое и при аллотропических превращениях в твердом состоянии, причем высокотемпературная модификация δ-Fe растворяет меньше газов, чем низкотемпературная γ-Fe.
[H], см3/100г [N], %

400 800 1200 1600 t, oC
Зависимость растворимости азота (1) и водорода (2)
от температуры при парциальном давлении 0,1 МПа.
0,003
0,002
0,001

Растворимость водорода в жидком железе

. [N],%
0,04
0,02
0
600 1000 1400 t °С
Растворимость азота в жидком железе

Растворимость кислорода в железе
