
ДЗ 1 Мт
.docДОМАШНЕЕ ЗАДАНИЕ № 1
ОБЩИЕ ЗАКОНОМЕРНОСТИ ХИМИЧЕСКИХ ПРОЦЕССОВ. РАСТВОРЫ
1.1. Для предложенной обратимой реакции рассчитайте
-
энтальпию химической реакции
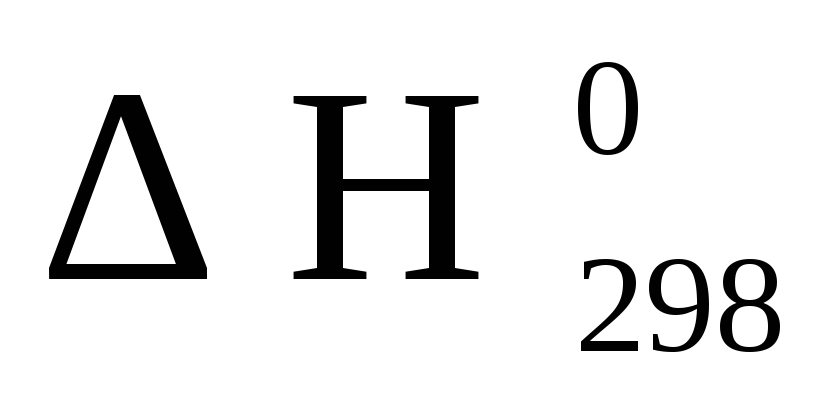 (кДж), Укажите,
эндо- или экзотермической является
прямая реакция;
(кДж), Укажите,
эндо- или экзотермической является
прямая реакция;
-
энтропию
 ,
энергию Гиббса
,
энергию Гиббса
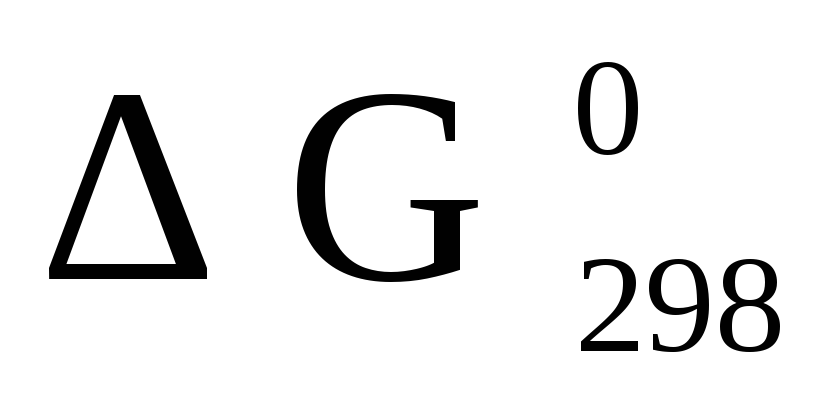 химической
реакции. Оцените термодинамическую
возможность протекания химической
реакции в стандартных условиях;
химической
реакции. Оцените термодинамическую
возможность протекания химической
реакции в стандартных условиях;
-
напишите математическое выражение константы химического
-
равновесия;
-
укажите направление смещения равновесия при изменении каждого из параметров. При рассмотрении влияния изменения концентраций запишите химические формулы исходных веществ и продуктов реакции.
|
вариант |
Уравнение реакции |
Изменение параметра |
|||
|
температуры |
давления |
концентрации |
|||
|
Исходного вещества |
Продукта реакции |
||||
|
1 |
2 |
3 |
4 |
5 |
6 |
|
1 |
СH4(г)+4Cl2(г) |
повышение |
понижение |
повышение |
понижение |
|
2 |
2N2O(г)
+ 3O2(г)
|
повышение |
повышение |
понижение |
понижение |
|
3 |
2Fe2O3(к)
+
3С(к) |
повышение |
понижение |
понижение |
повышение |
|
4 |
MnO2(к)
+
2C(к) |
понижение |
повышение |
повышение |
понижение |
|
5 |
CO(г)
+ H2O(г)
|
понижение |
понижение |
повышение |
повышение |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
6 |
2H2O
(г)+
2Cl2
(г) |
повышение |
понижение |
понижение |
понижение |
|
7 |
2Fe2O3(к)
+
3С(к) |
понижение |
повышение |
повышение |
повышение |
|
8 |
2ZnS(к)
+3O2(г) |
повышение |
понижение |
понижение |
повышение |
|
9 |
4Fe(к)
+
3O2(г) |
понижение |
повышение |
повышение |
понижение |
|
10 |
SO2(г)
+
2H2(г)
|
понижение |
понижение |
повышение |
повышение |
|
11 |
C(к)
+
CO2(г) |
повышение |
понижение |
повышение |
понижение |
|
12 |
Fe3O4(к)
+
C(т) |
повышение |
повышение |
понижение |
понижение |
|
13 |
Fe3O4(к).+
H2(г) |
повышение |
понижение |
понижение |
повышение |
|
14 |
Fe2O3(к)
+
3СO(г) |
понижение |
повышение |
повышение |
понижение |
|
15 |
C(к)
+ H2O(г) |
понижение |
понижение |
повышение |
повышение |
|
16 |
SO3(г)
+ H2(г) |
повышение |
понижение |
понижение |
понижение |
|
17 |
N2O(г)
+ NO(г) |
понижение |
повышение |
повышение |
повышение |
|
18 |
C(к)
+
2H2(г) |
повышение |
повышение |
понижение |
понижение |
|
19 |
2H2S(г)
+ 3O2(г.) |
повышение |
понижение |
понижение |
повышение |
|
20 |
4HCl(г)
+
O2(г) |
понижение |
повышение |
повышение |
понижение |
|
21 |
Fe3O4(к)
+4H2(г) |
понижение |
понижение |
повышение |
повышение |
|
22 |
С2H4(г)+3O2(г) |
понижение |
повышение |
повышение |
понижение |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
23 |
4HCl(г)
+
O2(г) |
понижение |
понижение |
повышение |
повышение |
|
24 |
CH4(г)
+
2O2(г) |
повышение |
понижение |
понижение |
понижение |
|
25 |
2NO(г)
+
O2(г) |
понижение |
повышение |
повышение |
повышение |
1.2. Напишите названия и укажите классы перечисленных соединений. Для электролитов запишите уравнения диссоциации
1.3. Выберите пары взаимодействующих веществ, запишите уравнения происходящих реакций.
1.4. Запишите молекулярные и ионные уравнения реакций, соответствующих превращениям.
1.5. Допишите ионные и молекулярные уравнения реакций.
|
вариант |
Номер задания |
|||
|
1.2 |
1.3 |
1.4 |
1.5 |
|
|
1 |
2 |
3 |
4 |
5 |
|
1 |
ZnO Вa(OH)2 SiO2 NH4NO3 KHSO3 |
Zn(OH)2 + KOH MgSO4 + Na3PO4 N2O5 + CaO Mn(OH)2 + Na2O |
CO2→BaCO3→BaCl2→BaSO4 SnOHCl →Sn(OH)2 → Na2SnO2 |
Cu2+ + S2− = |
|
2 |
Na2O MgOHCl Al2O3 HNO2 Ba(NO3)2 |
CaCO3 + HCl PbO2 + H2O SO2 + HCl CaO + Ba(OH)2 |
Na2S →H2S→NaHS→Na2S FeCl3→FeOHCl2→ FeCl3 |
HSO3− + OH− = |
|
1 |
2 |
3 |
4 |
5 |
|
3 |
PbO2 H3PO4 P2O5 Co(OH)2 CdSO4 |
Sn(OH)2 + NaOH CuSO4 + Na3PO4 SO3 + HCl Ni(OH)2 + Na2O |
Cr(NO3)3→Cr(OH)3→CrCl3→Cr(NO3)3 Ca(HCO3)2 → H2CO3 → CaCO3 |
CrOHSO4+H+= |
|
4 |
VO Sr(OH)2 Cr2O3 NH4Cl, H2SiO3 |
Cu(NO3)2 + K2S Na2CO3 + H2SO4 ZnO + H2O CO2 + CaO |
MgO→Mg(OH)2→MgCl2→Mg(NO3)2 CaHPO4→ H3PO4→Ca3(PO4)2 |
CO32−+2H+ = |
|
5 |
HClO Na2HPO4 P2O3 CaCl2 PbO2 |
Mg(OH)2 + Na2O CrCl3 + NaOH CdO + NaOH H2SeO3 + CO2 |
SO2→H2SO3→ Na2SO3→H2SO3 NiSO4→(NiOH)2SO4→NiSO4 |
Pb(OH)2+2OH− |
|
6 |
NiO BaHPO4 SnO Fe(NO3)3 Mg(OH)2 |
Mg(NO3)2 + KOH K2CO3 + HCl SiO2 + BaO Cr(OH)3 + KOH |
Sn(NO3)2→Sn(OH)2→SnSO4→SnCl2 Al(OH)3 → NaAlO2→ Al(OH)3 |
HPO42− + OH− = |
|
7 |
NaHCO3 Mn(OH)2 SO3 Cd(NO3)2 SnO2 |
Co(OH)2 + K2O P2O5 + HCl BaO + HCl Cr2O3 + H2O |
NiSO4→(NiOH)2SO4→NiSO4→NiS Mg(HCO3)2→ MgSO4 → MgCl2 |
Pb(OH)2+ 2OH− |
|
1 |
2 |
3 |
4 |
5 |
|
8 |
CrO3 Ba(NO2)2 BeO SnOHCl NaHSO3 |
H2SiO3 + N2O5 SnSO4 + NaOH Al(OH)3 + KOH N2O5 + HCl |
ZnSO4→Zn(OH)2→ZnCl2 →ZnS K3PO4→KH2PO4→K3PO4 |
3Mg2+ + 2PO43− |
|
9 |
Al2O3 Na2CO3 B2O3 FeOHCl2 K2HPO4 |
CaCl2 + H2SO4 P2O5 + HNO3 NiO + H2O Na2O + Ba(OH)2 Mn2O7 + H2SO4 |
Al2O3→ Al2(SO4)3→Al(OH)3→NaAlO2 Ca(OH)2 → Ca(HCO3)2→ Ca(NO3)2 |
HPO42− + 2H+ = |
|
10 |
MgO NH4NO3 BeO H2SiO3 Ca(OH)2 |
Cd(OH)2 + HC ZnSO4 + NaOH FeO + Ba(OH)2 I2O5 + HNO3 |
CaO→Ca(OH)2→CaCO3→Ca(NO3)2 NaHSO3→Na2SO3→ H2SO3 |
BeO22− + 2H+ = |
|
11 |
Cr2O3 Cu(OH)2 AlOHSO4 SnCl2 TeO2 |
AgNO3 + HCl MgSO4 + KOH ZnO + H2O CO2 + CaO |
H3PO4→ KH2PO4→K3PO4→AlPO4 Sn(OH)2→SnSO4→SnCl2 |
Cu2+ + PO43− = |
|
12 |
Al2O3 Mn(OH)2 SrO KHCO3 Pb(NO3)2 |
Ca(OH)2 + N2O5 CaCl2 + Na3PO4 MnO + Ca(OH)2 SnO2 + H2O |
FeCl3→Fe(OH)3→Fe2(SO4) 3→ FeCl3 Na2S→H2S→NaHS→Na2S |
HS− + OH− = |
|
1 |
2 |
3 |
4 |
5 |
|
13 |
MnO2 Cd(OH)2 Na3PO4 KHSO3 P2O3 |
HNO2 + NaOH Ga2O3 + H2O PbO + H2O Sr(OH)2 + HCl |
Fe(OH)3→Fe2(SO4)3→FeCl3→FeOHCl2 BaHPO4→Ba(NO3)2→BaCO3 |
PO4 3− + 2H+ = |
|
14 |
PbO2 HNO2 HgO K3PO4 NaHS |
NH4Cl + KOH H2SiO3 + P2O5 MgO + HNO3 CrO3 + HCl |
CaO→Ca3(PO4)2→H3PO4→CaHPO4 Al2O3→Al(NO3)3→Al(OH)2NO3 |
SeO32− + H+ = |
|
15 |
FeO H3PO4 TeO2 K2SO4 NaHS |
Cd(NO3)2 + K2S Na2CO3 + H2SO4 Mn2O7 + HCl Bi2O3 + H2O |
BeO2→BeCl2→Be(OH)2→K2BeO2 (CuOH)2SO4→ CuSO4→CuCl2 |
HPO42− + 2H+ = |
|
16 |
Rb2O H2SO3 Cl2O7 Sr(OH)2 NiOHNO3 |
H3PO4 + NiCl2 NH4NO3 + KOH SrO + H2SO4 AlCl3 + NaOH |
FeSO4→FeCl2→Fe(OH)2→Fe(NO3)2 Ca(OH)2→CaHPO4→Ca3(PO4)2 |
Cr + OH− + 2Cl− |
|
17 |
SO2 Ni(OH)2 BaCl2 FeOHSO4 Al2O3 |
Cl2O + H2SiO3 PbO + H2O N2O3 + HCl BeO + H2O |
CaO→CaCO3→Ca(HCO3)2→CaCO3 CrOHSO4→Cr2(SO4)3→Cr(OH)3 |
BeO2 2− + 2H+ = |
|
1 |
2 |
3 |
4 |
5 |
|
18 |
P2O5 Mn(OH)2 MgO NaHCO3 Fe(NO3)3 |
Fe2(SO4)3 + Na3PO4 CrO + H2O SrCl2 + H2SO4 Mn2O7 +HClO4 |
Co(OH)2→CoOHCl→CoCl2→Co(NO3)2 H3PO4→K3PO4→KH2PO4 |
Be(OH)2+2OH− |
|
19 |
TeO2 Cu(OH)2 SrO KHSO3 Na3PO4 |
K2SO3 + HCl CuO + H3PO4 SO3 + HCl Ni(OH)2 + Na2O |
Cr2O3→Cr2(SO4)3→Cr(OH)3→NaCrO2 BaCl2→BaCO3→Ba(HCO3)2 |
SO32− + Ba2+ = |
|
20 |
CO2 Ni(OH)2 CaO Cu(NO3)2 H2CO3 |
Sn(OH)2 + NaOH Cl2O + H3PO4 Sb2O3 + H2O MgO + H2SO4 |
NiSO4→(NiOH)2SO4→Ni(OH)2→NiCl2 Na2CO3 →NaHCO3 → H2CO3 |
HSe −+ OH− = |
|
21 |
CdO Mg(OH)2 Na2SiO3 HClO4 N2O5 |
Pb(NO3)2 + K2S CaO+ SO2 N2O3 + H2SO4 Fe2O3 + H2O |
CaO→Ca(HCO3)2 → H2CO3 → CaCO3 Zn(OH)2 →ZnOHCl→ ZnCl2 |
Cr3+ + 3OH− = |
|
22 |
Mn2O7 Pb(OH)2 Cl2O H2CO3 CoOHCl
|
Na2SiO3 + HCl Bi2O3 + H2O FeSO4 + NaOH NiO + KOH |
BeSO4→Be(OH)2→K2BeO2→Be(NO3)2 H3PO4→Ca3(PO4)2→CaCl2 |
HS− + H+ = |
|
1 |
2 |
3 |
4 |
5 |
|
23 |
ZnO KHS Na2SiO3 BaO Be(OH)2 |
Zn(OH)2 + KOH BeSO4 + NaOH P2O5 + HNO3 NiO + H2O |
ZnSO4→Zn(OH)2→ZnCl2→Zn(NO3)2 H3PO4→K3PO4→KH2PO4 |
PO43− + 3H+ = |
|
24 |
PbO2 SnOHCl P2O5 Al(NO3)3 H2SeO3 |
Sn(OH)2 + NaOH CuSO4 + Na3PO4 N2O5 + NaOH Mn(OH)2 + CaO |
CaO → Ca(OH)2 → CaCO3 → Ca(NO3)2 Cr2(SO4)3→CrOHSO4→Cr(OH)3 |
Al(OH)3 + OH− |
|
25 |
Co(OH)2 H2SO3 N2O3 Al2(SO)3 SnO2 |
CaCO3 + HCl PbO2 + H2O SO2 + HCl CaO+Ba(OH)2 |
Al2O3→ AlСl3→Al(OH)3 → NaAlO2 FeCl3→FeOHCl2→Fe(OH)3→Fe2(SO4)3 |
ZnO22−+2H+ = |
