
m20
.pdf
3.5.17. Коэффициент прозрачности прямоугольного прозрачного барьера:
|
|
2l |
|
|
|
|
2m(U E) |
||||
D D exp |
|
|
|
. |
|
|
|
|
|||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
61

4. ФИЗИКА КОНДЕНСИРОВАННОГО СОСТОЯНИЯ
Физика конденсированного состояния – раздел физики, изучающий поведение сложных систем (то есть систем с большим числом степеней свободы) с сильной связью. Принципиальная особенность эволюции таких систем заключается в том, что её (эволюцию всей системы) не удается «разделить» на эволюцию отдельных частиц. «Разбираться» приходится со всей системой в целом. Как результат, часто вместо движения отдельных частиц приходится рассматривать коллективные колебания. При квантовом описании, эти коллективные степени свободы становятся квазичастицами.
4.1.1. Молярная внутренняя энергия химически простых твер-
дых тел в классической теории теплоемкости:
Uμ 3RT .
4.1.2. Теплоемкость C системы (тела) при постоянном объеме определяется как производная от внутренней энергии U по температуре:
C ddUT .
4.1.3. Закон Дюлонга и Пти – эмпирический закон, согласно которому молярная теплоёмкость твёрдых тел при комнатной температуре близка к 3R:
Cμ 3R .
4.1.4. Закон Неймана – Коппа: молярная теплоемкость химически сложных тел (состоящих из различных атомов):
Cμ n3R ,
где n – общее число частиц в химической формуле соединения.
4.1.5. Среднее значение энергии E квантового осциллятора,
приходящейся на одну степень свободы, в квантовой теории Эйнштейна:
E E0 |
|
ω |
|
|
, |
|
|
|
|
|
|||
ω |
|
|||||
|
|
1 |
||||
|
|
exp |
|
|
||
|
|
|
||||
|
|
kT |
|
|
|
|
где E0 – нулевая энергия ( E0 1/ 2 ω); ω – круговая частота колеба-
ний осциллятора.
4.1.6. Молярная внутренняя энергия кристалла в квантовой теории теплоемкости Эйнштейна определяется по формуле:
Uμ Uμ |
|
3R |
|
θE |
|
, |
|
0 |
exp(θE / T ) 1 |
||||||
|
|
|
|||||
|
|
|
|
||||
|
|
62 |
|
|
|
||

где Uμ0 3 / 2RθE – молярная нулевая энергия по Эйнштейну;
θE ω / k – характеристическая температура Эйнштейна.
4.1.7.Молярная теплоемкость кристалла в квантовой теории теплоемкости Эйнштейна при низких температурах (T θE ):
C 3R |
θ |
E |
|
|
θ |
E |
|
|
exp |
|
. |
||||
|
|
|
|
||||
μ |
T |
|
|
T |
|||
|
|
||||||
4.1.8. Частотный спектр колебаний в квантовой теории тепло-
емкости Дебая:
dZ g(ω)dν ,
где g(ω) – функция распределения частот; dZ – число собственных час-
тот тела, приходящихся на интервал частот от ω до ω dω , определяется выражением (для трехмерного кристалла, содержащего N атомов)
dZ gN ω2dω ,
ω3max
где ωmax – максимальная частота, ограничивающая спектр колебаний.
4.1.9. Энергия U твердого тела связана со средней энергиейE квантового осциллятора и функцией распределения частот g(ω)
соотношением:
ωmax
U E g(ω)dω.
0
4.1.10. Молярная внутренняя энергия кристалла по Дебаю:
|
|
|
|
|
T |
|
3 |
θ |
D |
/T |
x |
3 |
|
|
|
|
|
|
|
|
|
|
|
||||||
U |
|
U |
|
3RT 3 |
|
|
|
|
|
|
dx , |
|||
μ |
μ0 |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
exp(x) 1 |
|
||||||
|
|
|
|
|
θD |
|
|
0 |
|
|||||
где Uμ0 9 / 8RθD – молярная нулевая энергия кристалла по Дебаю; θD ωmax – характеристическая температура Дебая.
4.1.11. Молярная теплоемкость кристалла по Дебаю, при низких температурах (T θD ):
|
|
3 |
|
|
|
3 |
|
12π |
|
T |
|
||
Cμ |
|
|
||||
|
|
R |
|
. |
||
5 |
|
|
||||
|
|
|
θD |
|
||
4.1.12. Теплоемкость электронного газа – количество теплоты,
которую необходимо передать электронному газу для того, чтобы повысить его температуру на 1 К. Она намного меньше по величине при высоких температурах, чем теплоёмкость кристаллической решётки:
63
C |
|
|
|
π 2 |
ZR |
T |
, |
μ |
э |
|
|
||||
|
2 |
|
θ F |
||||
|
|
|
|
|
|
|
|
где θ F EF – характеристическая температура Ферми. k
4.1.13. Энергия фонона E (фонон – квазичастица, являющаяся квантом поля колебаний кристаллической решетки):
Ekθ D .
4.1.14.Квазиимпульс фонона:
p2π / λ.
4.1.15.Скорость фонона – групповая скоростью звуковых волн в
кристалле:
u ddEp .
Скорость фонона при малых значениях энергии фонона, когда дисперсией волн можно пренебречь совпадает с групповой скоростью:
u υ E / p .
Скорости продольных υl и поперечных υτ волн в кристалле:
|
|
|
|
|
|
υl E / ρ и |
υτ G / ρ , |
||||
где E и G – модули соответственно продольной и поперечной упругости.
4.1.16. Усредненное значение скорости звука υ связано с υl и υ τ
соотношением:
2 1 .
υ3 υ3τ υ3l
4.1.17.Распределение Ферми – Дирака по энергиям для свобод-
ных электронов в металле:
f (ED ) |
|
|
|
1 |
|
|
|
, |
|
|
|
|
|
|
|
||
E |
|
E |
|
|
|
|||
|
i |
F |
1 |
|||||
|
exp |
|
|
|
||||
|
|
|
|
|
||||
|
|
|
kT |
|
|
|
|
|
где Ei – энергия электронов; EF – уровень (или энергия) Ферми.
4.1.18. Распределение Бозе – Эйнштейна – формула, описываю-
щая распределение по энергетическим уровням тождественных частиц с нулевым или целочисленным спином при условии, что взаимодействие частиц в системе слабо и им можно пренебречь:
64

f (EE ) |
|
|
|
1 |
|
|
|
. |
|
|
|
|
|
|
|
||
E |
|
E |
|
|
|
|||
|
i |
F |
1 |
|||||
|
exp |
|
|
|
||||
|
|
|
|
|
||||
|
|
|
kT |
|
|
|
|
|
4.1.19. Уровень Ферми в металле при Т = 0:
|
|
|
2 |
2 |
|
||
|
|
|
|
|
|
||
E |
F |
|
(3π2n) 3 . |
||||
2m |
|||||||
|
|
|
|
|
|||
|
|
|
|
|
|
||
4.1.20. Температура вырождения T – температура, ниже которой отчётливо проявляются квантовые свойства идеального газа, обусловленные тождественностью частиц:
|
2π 2 |
|
2 |
|
|
T |
n 3 . |
||||
km |
|||||
|
|
|
|
||
4.1.21. Удельное сопротивление собственных полупроводников:
ρ enb1 ,
где n – концентрация носителей заряда (электронов и дырок); b – подвижность носителей заряда.
4.1.22. Удельная проводимость собственных полупроводников:
γ en(bn bp ) ,
где bn и bp – подвижности электронов и дырок.
4.1.23. Зависимость электропроводности полупроводника от тем-
пературы:
σ σ0 exp( E / 2kT) .
4.1.24. Напряжение U H на гранях образца при эффекте Холла:
UH RH Bjh ,
где RH – постоянная Холла; В – индукция магнитного поля; h – ширина
пластины; j – плотность тока.
4.1.25. Уровень Ферми в собственном полупроводнике:
EF 2E .
4.1.26. Удельная проводимость собственных полупроводников:
|
|
E |
|
γ γ0 exp |
|
|
. |
|
|||
|
|
2kТ |
|
4.1.27. Правило Стокса для люминесцентного излучения – длина волны люминесценции дольше длины волны возбуждающего люминесценцию света:
hv hvлюм E .
65
4.1.28. Молярный объем кристалла:
Vμ M / ρ .
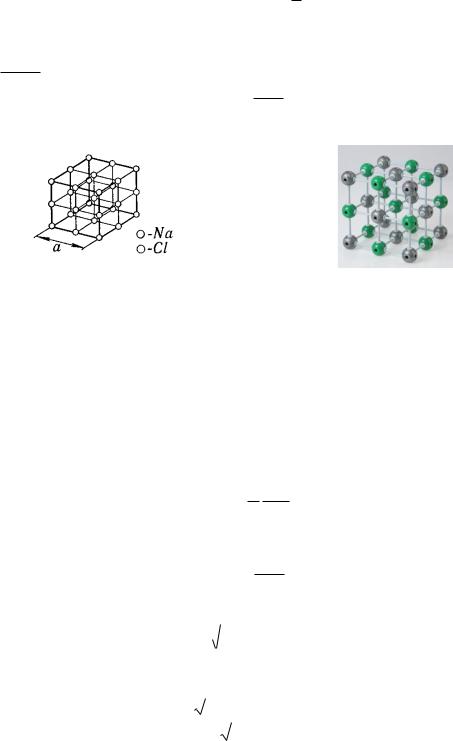
4.1.29.Объем V элементарной ячейки в кристаллах (рис. 4.1, 4.2):
при кубической сингонии: V a3 ;
при гексагональной сингонии V 
 3a2c / 2 , где а и с – параметры решетки.
3a2c / 2 , где а и с – параметры решетки.
для гексагональной решетки при теоретическом значении c 
 8 / 3a :
8 / 3a :
V 
 2a3 .
2a3 .
Рис. 4.1 |
Рис. 4.2 |
4.1.30. Число элементарных ячеек в одном моле кристалла:
Zμ Vμ /V , или |
Zμ kNA / n , |
где k – число одинаковых атомов в химической формуле соединения; n – число одинаковых атомов, приходящихся на элементарную ячейку.
4.1.31. Число Z элементарных ячеек в единице объема кристалла:
Z Zμ /Vμ ,
в общем случае:
Zρ kn NMA ;
для кристалла, состоящего из одинаковых атомов (k = 1):
Z ρ nMN A .
4.1.32. Параметр а кубической решетки:
|
|
|
|
|
|
|
|
|
a 3 nM /(kρN |
A |
) . |
||||
|
|
|
|
|
|
|
|
|
4.1.33. Расстояние d между соседними атомами в кубической ре- |
||||||
шетке: |
|
|
|||||
|
|
|
|
|
|
|
|
в гранецентричной: d a / 2 ; |
|
|
|||||
|
|
|
|
|
|||
в объемно-центрированной: d 3a / 2 . |
|
|
|||||
|
66 |
|
|
||||

5. АТОМНАЯ ФИЗИКА.
5.1. Модели атомов. Атом водорода по теории Бора
Развитие исследований радиоактивного излучения, с одной стороны, и квантовой теории – с другой, привели к созданию квантовой модели атома Резерфорда – Бора. Но созданию этой модели предшествовали попытки построить модель атома на основе представлений классической электродинамики и механики. В 1904 г. появились публикации о строении атома, принадлежащие одна японскому физику Х. Нагаока (1865–1950), другая – английскому физику Д. Д. Томсону.
5.1.1 Модели атомов, рассматриваемые в конце XX века Д. Д. Томпсоном, Х. Нагаока и Э. Резерфордом (рис. 5.1).
Рис. 5.1
5.1.2 Атом – сложная система, имеющая сложные атомные спек-
тры (рис.5.3, 5.4).
Рис. 5.2
5.1.3Обобщенная формула Бальмера:
|
1 |
|
1 |
|
1 |
1 |
|
1 |
|
|
v R |
|
|
|
или |
|
|
|
|
|
(k 1, 2, 3,... т k 1, k 2, k 3,...), |
|
|
|
|
|
||||||
|
n2 |
|
R |
n2 |
||||||
k 2 |
|
|
λ |
k 2 |
|
|
||||
где v – частота спектральных линий в спектре атома водорода; k определяет серию (т=1, 2, 3, ...); п определяет отдельные линии соответст-
67

|
|
m e4 |
|
15 |
|
1 |
|
7 |
1 |
|
|
e |
|
|
|||||
вующей серии (п=k+1, k+2, ...), R |
|
3,29 10 |
c |
|
; R |
1,1 10 м |
|
||
8ε02h3 |
|
|
|||||||
– постоянные Ридберга (рис. 5.1). |
|
|
|
|
|
|
|
|
|
|
Серия Лаймана k = 1. |
|
|
Серия Брэкета k = 4. |
|
||||
|
Серия Бальмера k = 2. |
|
|
Серия Пфунда k = 5. |
|
||||
|
Серия Пашена k = 3. |
|
|
Серия Хэмфри k = 6. |
|
||||
Рис. 5.3
5.1.4 Первый постулат Бора (правило квантования орбит или постулат стационарных состояний): электроны движутся только по определенным (разрешенным) орбитам. При этом, даже двигаясь с ускорением они не излучают энергию:
meυr n ,
где те – масса электрона; υ – скорость электрона по n-й орбите радиусом r, n 1, 2, 3, ...– главное квантовое число.
Боровский радиус – радиус первой орбиты водородоподобного атома (рис.3.17).
5.1.5 Второй постулат Бора (правило частот): излучение и поглощение энергии в виде кванта света (hv) происходит лишь при переходе электрона из одного стационарного состояния в другое. Величина светового кванта равна разности энергий тех стационарных состояний, между которыми совершается скачек электрона (рис.5.4):
hv En Em .
где En и Em – энергии электрона в двух стационарных состояниях, ν – частота фотона. При Em En происходит излучение фотона, при Em En
– его поглощение.
68
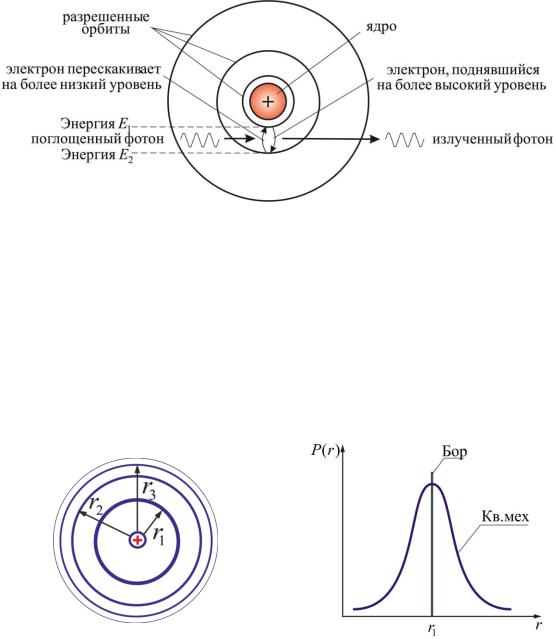
Рис. 5.4
5.1.6Уравнение Шредингера для электрона в атоме водорода:
|
2m |
e2 |
|
|
|
ΔΨ |
|
|
|
|
|
|
|
|
|||
|
E |
|
|
Ψ 0 . |
|
|
|
4πε |
0r |
||
5.1.7 Радиусы стационарных орбит (рис. 5.5, 5,6):
rn |
4πε |
0 |
2n2 |
, (n 1, 2, 3, ...). |
|||
|
|
|
|
||||
k |
0 |
m Ze2 |
|||||
|
|
||||||
|
|
|
e |
|
|||
Рис. 5.5 |
Рис. 5.6 |
5.1.8Энергия электрона в водородоподобном атоме:
En |
1 |
|
m Z 2e4 |
, (n 1, 2, 3, ...). |
|
|
|
e |
|
||
n2 |
|
8h2 |
ε02 |
||
|
|
|
|||
Энергетическое состояние, соответствующее значению n 1 называется основным или нормальным (невозбужденным) состоянием. Все состояния с n 1называются возбужденными.
5.1.9Энергия испускаемого кванта:
69

hv En E m |
mee4 |
|
1 |
|
1 |
|
|
|
|
|
. |
||
8h2ε02 |
|
m2 |
||||
|
n2 |
|
|
|||
5.1.10 Энергия ионизации атома водорода:
Ei E1 mee4 .
8h2ε02
5.2. Водородоподобные системы в квантовой механике
Атомные системы являются важнейшими объектами физики, для описания которых следует обязательно использовать законы квантовой механики. При этом существенно, что для такого описания квантовая механика не требует каких-либо дополнительных предположений, условий и постулатов, аналогичных постулатам в теории Бора.
5.2.1. Волновая функция положения электрона в атоме:
|
|
|
|
|
e |
r |
||
|
|
1 |
|
|
||||
|
|
|
|
. |
||||
Ψ(r) |
|
|
r1 |
|||||
πr |
3 |
|||||||
|
|
|
|
|
|
|||
|
|
1 |
|
|
|
|
||
Постоянная r1 совпадает с радиусом первой боровской орбиты. Следовательно, электронное облако в основном состоянии водорода сферически-симметрично, как показано на рис.5.7.
Рис. 5.7
5.2.2. Потенциальная энергия взаимодействия электрона с ядром, обладающим зарядом Ze (для атома водорода Z = 1):
U (r) k |
|
Ze2 |
, |
|
0 |
r |
|||
|
|
|||
|
|
|
где r – расстояние между электроном и ядром. Графически функция U(r) изображается на рис.5.8 жирной кривой. U(r) с уменьшением r (при приближении электрона к ядру) неограниченно убывает.
70
