
- •Масс- спектрометрия
- ••Масс-спектрометрия - это физический метод измерения отношения массы заряженных частиц материи (ионов) к
- ••Существенное отличие масс- спектрометрии от других аналитических физико-химических методов состоит в том, что
- ••Приборы, которые используются в этом методе, называются масс-спектрометры или масс-спектрометрические детекторы. Эти приборы
- ••Начало развитию масс-спектрометрии. положено опытами Дж. Томсона (1910), исследовавшего пучки заряженных частиц, разделение
- ••Первый серийный масс-спектрометр создан А. Ниром в 1940; его работы положили начало изотопной
- ••Macс-спектральные приборы.
- •Магнитный масс-спектрометр
- •Масс-спектр н-декана
- ••Первое, что надо сделать для того, чтобы получить масс-спектр, превратить нейтральные молекулы и
- •Методы ионизации
- ••Ионизация газообразной пробы может быть вызвана фотонами, ионами, электрическим полем, электронным ударом и
- ••Процесс ионизации и типы ионов
- ••Масс-анализаторы
- ••Все масс-анализаторы используют физические законы движения заряженных частиц. Исторически первым масс-анализатором, остающимся непревзойденным
- ••Именно это используется для анализа ионов по массам. Для того, чтобы увеличить разрешение,
- •Схема масс-анализатора с однородным магн. полем: S1 и S2 - щели
- •Схема масс-анализатора с двойной фокусировкой: S1 и S2 - щели источника
- ••Квадруполь
- •Схема квадрупольного масс-анализатора: 1 - высокочастотный генератор; 2 - генератор постоянного напряжения; 3
- •Квадрупольный масс-спектрометр
- ••Ионы, влетающие параллельно оси этих стержней, попадают в гиперболическое поле и оно, в
- •Схема спектрометра ион-циклотронного резонанаса
- •Ионно-циклотронный резонанс
- •Циклотронно-резонансный масс-анализатор -ячейка в виде прямоугольного параллелепипеда или куба, помещенная в однородное магн.
- •Дальнейшее развитие квадрупольных анализаторов привело к созданию "ионной ловушки". Одна пара стержней была
- •В последнее время все большую популярность приобрели "времяпролетные" (Time Of Flight, TOF) масс-анализаторы.
- •(V - напряжение)
- •Распространенность изотопов некоторых элементов
- •Некоторые масс-спектрометрические правила
- •Одна из важнейших задач - нахождение зависимости между характером масс-спектра и строением исследуемой
- •Примером установленных закономерностей фрагментации являются следующие схемы разрыва связей:
- •Определение парциального давления паров веществ
- •Определение константы равновесия химической реакции и теплоты реакции
- •Масс-спектромерия в химической кинетике

(V - напряжение)
Схема время-пролетного масс- анализатора: 1 - сетка; 2 - детектор.
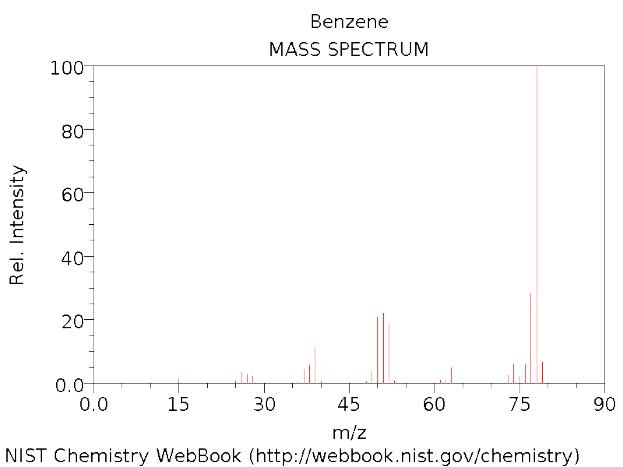
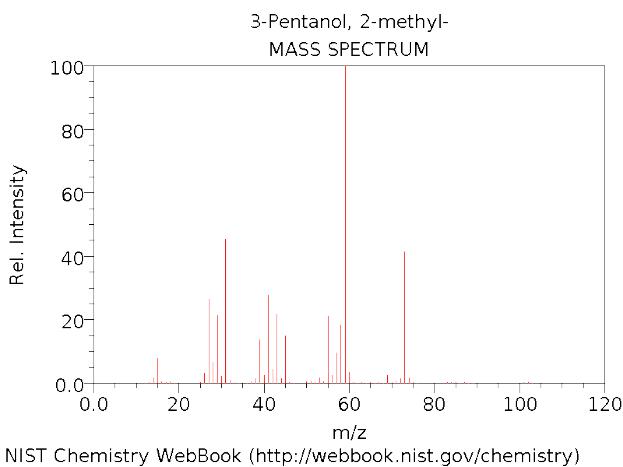


Распространенность изотопов некоторых элементов
 Элемент
Элемент
Водород
 Углерод
Углерод
Азот
 Кислород
Кислород
Фтор
 Кремний
Кремний
Фосфор
 Сера
Сера
Хлор Мышьяк
Селен
Бром
Теллур
Иод
Изотоп (распространенность в природе, %)
 1Н (99,985); 2H (0,015)
1Н (99,985); 2H (0,015)
(98,893); (1,107)
 14N (99,634); 15N (0,366)
14N (99,634); 15N (0,366)
16O (99,759); 17O (0,037); 18O (0,204)
 (100)
(100)
28Si (92,21); 29Si (4,70); 30Si (3,09)
 31P (100)
31P (100)
32S (95,0); 33S (0,75); 34S(4,22); 36S (0,02)  35Cl (75,77); 37Cl (24,23)
35Cl (75,77); 37Cl (24,23)
75As (100)
74Se (0,87); 76Se (9,02); 77Se (7,58); 78Se (23,52); 80Se (49,82); 82Se (9,19)
79Br (50,537); 81Br (49,463)
120Te (0,089); 122Te (2,46); 123Te (0,89); 124Te (4,74); 125Te (7,03); 126Te (18,72); 128Te (31,759); 130Te(34,27) 127I (100)
Некоторые масс-спектрометрические правила
•1. "Азотное правило". Большинство встречающихся в органических соединениях элементов имеют либо четную массу основных изотопов и четные валентности (C, O, S, Si, Ge, Pb и др.), либо нечетную массу и нечетные валентности (H, F, Cl, Br, I, As, Sb и др.). Поэтому М+. соединений, составленных из любых комбинаций этих элементов, имеют четную массу. Азот имеет четную массу и нечетную валентность.
•2. "Четно-электронное" правило. Ион-радикалы (нечетное число электронов) могут элиминировать или радикалы, или четно-электронные нейтральные молекулы, тогда как ионы (четное число электронов) могут терять лишь нейтральные четно-электронные частицы.
•Следует отметить, что это правило имеет довольно много исключений.
•3. Правило Стивенсона-Одье. При распаде молекул под действием электронного удара положительный заряд локализуется на фрагменте, который обладает наименьшей энергией ионизации.
•4. Затрудненный разрыв связей, принадлежащих к ненасыщенным системам.
Разрыв связей, прилежащих к винильной, этинильной или арильной группе, обычно затруднен вследствие очень низкой стабильности образующихся ненасыщенных ионов или радикалов (часто за подобные ионы принимают фрагменты продуктов перегруппировки молекулярных ионов).
Одна из важнейших задач - нахождение зависимости между характером масс-спектра и строением исследуемой орг. молекулы. При ионизации орг. молекулы образуется молекулярный ион, в котором далее происходят процессы гетеро- и гомолитического. разрыва связей или разрыва связей с перегруппировкой молекулы и образование осколочных ионов, которые в свою очередь могут подвергаться дальнейшему распаду. Последовательные распады ионов, устанавливаемые из масс-спектра, называются направлениями или путями распада. Направления распада - важная характеристика каждого класса соединений. Совокупность всех направлений распада составляет характерную для каждого органического соединения схему фрагментации. Если масс-спектр прост, схема фрагментации сводится к одному пути распада, например, при распаде молекулярного иона СН3ОН+
последовательно образуются ионы СН2=ОН+ и Н—С=О+. В случае сложных масс-спектров схема фрагментации отвечает
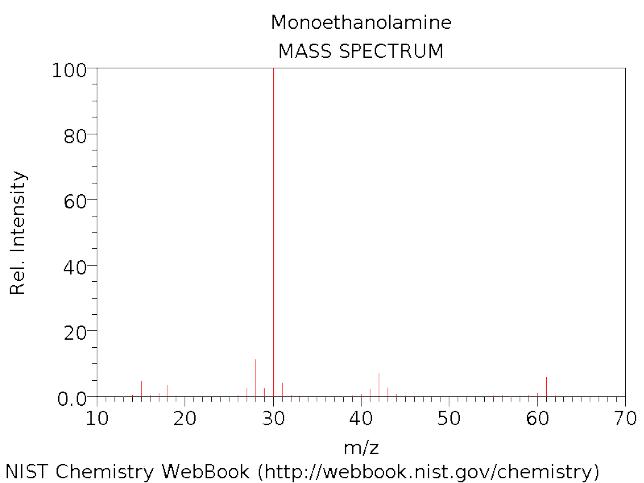
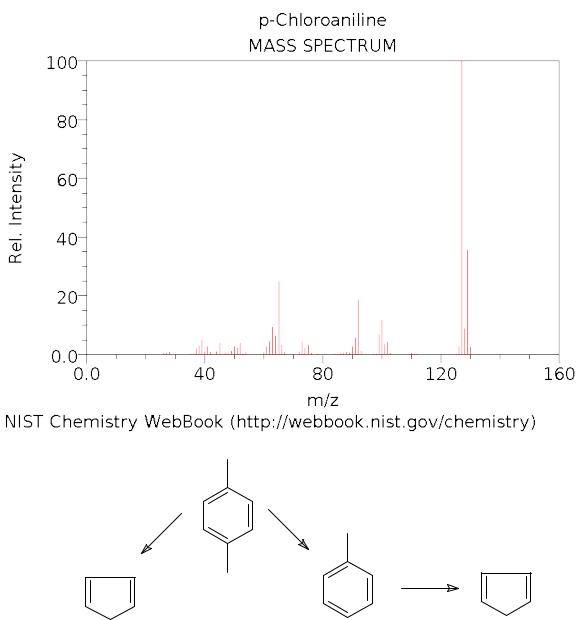
|
NH2 +* |
|
|
|
-HCN |
-Cl |
NH2 |
|
|
m*66.5 |
|
|
||
m*78.8 |
|
|
|
|
+* |
Cl |
+ |
-HCN |
+ |
|
||||
|
|
m*46 |
||
|
M=127 |
|
|
|
Cl |
|
|
|
|
|
M=92 |
|
M=65 |
|
|
|
|
M=100
Примером установленных закономерностей фрагментации являются следующие схемы разрыва связей:
•1. В разветвленных углеводородах наиболее вероятен разрыв связей у места ветвления
C |
|
|
C |
|
C |
|
C |
|
+* |
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
C |
|
C |
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
* C |
|
C |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
•2. Вероятность разрыва связи С-Н уменьшается с увеличением длины цепи углеводорода
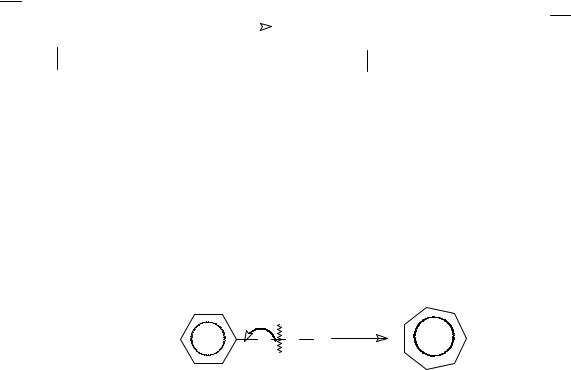
•3. В ароматических производных наиболее вероятен разрыв β-связей с образованием перегруппировочного тропилиевого иона С7Н7+
|
|
|
|
+* |
C |
C C |
+ |
•4. В масс-спектрах спиртов характерными осколочными ионами являются ионы с массами 31(СН2=ОН+) и М-1 (RCH=OH+), которые соответствуют следующей схеме разрыва связей:
•5. Для аминов H2N-CH2-R характерен разрыв α-связи
•с образованием иона NH2=CH2 (30). Значительным также является пик H2N=CHR (M-1).
R CH OH
CH OH
H
H2N CH2  C C
C C
R1 C=O
R2

• 6. Масс-спектр кетонов содержит ионы R1-C=O+ и R2-C=O+. Если алкильная цепь содержит три и более атомов углерода, то происходит отрыв β-связи и далее перегруппировка с участием атома водорода:
•7. Алифатические фториды, хлориды и бромиды дают малую интенсивность молекулярного ионного тока, но иодиды имеют значительный пик молекулярного иона.
•8. Металлорганические соединения обладают крайне низкой энергией связи металл-углерод, что приводит к резкому уменьшению интенсивности молекулярного иона в масс-спектре.
R3 |
R4 |
R3 |
CH |
CH |
R4 |
|
CH |
CH |
|||||
|
|
|
|
|||
R2CH |
H |
|
|
|
+ |
|
|
R2 |
CH |
C |
OH |
||
C |
O+* |
|||||
|
|
R1 |
|
|||
R1 |
|
|
|
|

I
А
В
|
|
|
Е, эВ |
|
ПИ(А) |
ПИ(В) |
|||
|
||||
ПП(R+1)=D(R1 - R2)+ПИ(R1)+Т(R+1, R2)+Е (R+1, R2) |
(1) |
|
• |
D(R1 - R2) ≈ ПП(R+1) - ПИ(R1) |
(2) |
• |
ПИ(R1) ≈ ПП(R+1) - D(R1 - R2) |
(3) |
