
- •Глава 21
- •21.1. Дыхательные движения
- •21.2. Легочная вентиляция
- •21.3. Механика дыхания
- •21.4. Газообмен Содержание газов в альвеолах
- •Влияние вентиляционно–перфузионного отношения
- •21.5. Легочная перфузия и оксигенация крови в легких
- •21.6. Центральный генез дыхательного ритма и регуляция дыхания
- •21.7. Литература
21.5. Легочная перфузия и оксигенация крови в легких
Легочная перфузия
Сосудистое сопротивление. Величина легочного кровотока (перфузии) в покое составляет 5–6 л/мин, а движущей силой для него служит разница средних давлений всего около 8 мм рт. ст. (1 кПа) между легочной артерией и левым предсердием. Следовательно, сопротивление легочных сосудов по сравнению с общим периферическим чрезвычайно мало. При тяжелой физической работе легочный кровоток увеличивается в четыре раза, а давление в легочной артерии – всего в два раза. Таким образом, с повышением скорости кровотока снижается сопротивление легочных сосудов.
Это уменьшение сосудистого сопротивления происходит пассивно в результате расширения легочных сосудов и раскрытия резервных капилляров. В покое кровь протекает примерно лишь через 50% всех легочных капилляров, а по мере возрастания нагрузки доля перфузируемых капилляров возрастает. Параллельно увеличивается и площадь газообменной поверхности (т.е. диффузионной способности легких), и благодаря этому достигается соответствие поглощения O2 и выделения СO2 метаболическим потребностям организма.
На сопротивление легочных сосудов кровотоку в известной мере влияют дыхательные экскурсии грудной клетки. При вдохе артерии и вены расширяются, что связано с увеличением степени растяжения эластических волокон, крепящихся к их наружным стенкам. Однако одновременно повышается сопротивление капилляров, так как они растягиваются в длину и, следовательно, сужаются. Поскольку эффект повышения капиллярного сопротивления преобладает, сопротивление легочных сосудов в целом по мере расширения легких возрастает [32].
Местные различия в легочном кровотоке. Легочный кровоток отличается выраженной региональной неравномерностью, степень которой зависит в основном от положения тела. При его вертикальном положении основания легких снабжаются кровью значительно лучше, чем верхушки. Это связано с разницей в гидростатическом давлении: верхушки легких располагаются на 30 см выше оснований, и вследствие этого между сосудами этих отделов создается перепад гидростатического давления
примерно 23 мм рт. ст. (3 кПа). Это означает, что артериальное давление в верхних отделах легких ниже, чем альвеолярное, поэтому капилляры здесь почти спавшиеся. В нижних же отделах капилляры более расширены, так как внутрисосудистое давление больше альвеолярного. Вследствие таких местных различий в сосудистом сопротивлении кровоток в пересчете на единицу объема легких почти линейно снижается в направлении от основания легких к их верхушкам [31, 32]. При физической нагрузке и при горизонтальном положении тела легочный кровоток более равномерен.
Гипоксическая вазоконстрикция. Еще один фактор, влияющий на местный кровоток в легких,–это состав газовой смеси в альвеолах того или иного отдела. Так, снижение парциального давления O2 в альвеолах приводит к сужению артериол и, следовательно, к уменьшению кровотока (феномен Эйлера–Лилиестранда). В результате такого повышения сосудистого сопротивления, вызванного гипоксией, количество крови, протекающей через плохо вентилируемые участки легких, снижается, и кровоток перераспределяется в пользу хорошо вентилируемых отделов. Тем самым местная перфузия Q’ в известной мере приспосабливается к местной альвеолярной вентиляции V’a. Однако этот механизм не может предупредить возникновение местных неравномерностей соотношения V’a/Q’, в частности в патологических условиях.
Венозно–артериальные шунты. Большая часть выбрасываемой правым сердцем крови имеет диффузионный контакт с поверхностью альвеол, однако небольшой объем этой крови не участвует в газообмене. Эта часть крови смешивается с оксигенированной кровью перед тем, как попадает в системное кровообращение (так называемый шунтовой кровоток). Существуют естественные анатомические шунты малые сердечные вены Тебезия, открывающиеся в левый желудочек, и бронхиальные вены. Сосуды перфузируемых, но не вентилируемых альвеол представляют собой функциональные шунты. По любым из этих шунтов кровь из системных вен поступает в артерии большого круга, минуя участки, в которых происходит газообмен, поэтому состав ее не изменяется. Несмотря на то что у здорового человека на долю такого шунтового кровотока приходится всего около 2% общего сердечного выброса, напряжение O2 в артериях после перемешивания с этой кровью снижается на 5–10 мм рт. ст. по сравнению со средним напряжением O2 в конечных отделах капилляров легких. При врожденных пороках сердца (например, незаращении межжелудочковой перегородки) или сосудов (например, незаращении артериального протока) через шунты сбрасывается значительно больший объем крови, что приводит к гипоксии (пониженное напряжение O2) и гиперкапнии (повышенное содержание СO2 ).
Факторы, влияющие на газообмен. Основные факторы, от которых зависят насыщение крови
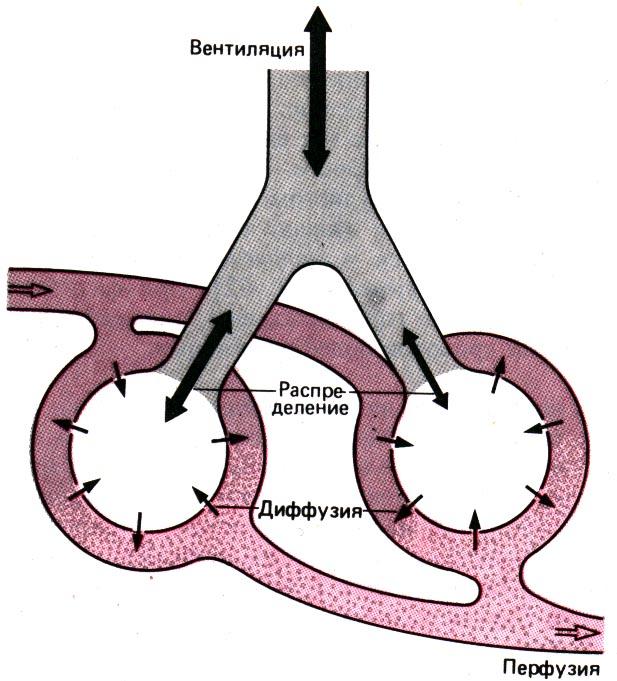
Рис. 21.24. Схема действия факторов, влияющих на газообмен в легких [8]
в легких кислородом и удаление из нее углекислого газа,–это альвеолярная вентиляция V’a, перфузия легких Q’ и диффузионная способность легких Dл (рис. 21.24). Мы убедились в том, что эффективность дыхания определяется не столько этими тремя факторами как таковыми, сколько их соотношениями, в частности V’а/Q’ и Dл/Q’ [31, 46]. Еще один фактор, влияющий на газообмен,–это местная неравномерность вентиляции, перфузии и диффузии в различных отделах легких [12, 18, 46]. Вследствие этой неравномерности газообмен происходит менее эффективно: напряжение O2 в крови артерий большого круга снижается, а напряжение СO2 слегка повышается.
Неравномерность вентиляционно–перфузионного соотношения. Неравномерное распределение соотношения V’a/Q’ в различных отделах легких имеет особое значение как при нормальной, так и при патологической физиологии. Для того чтобы оценить это распределение, были разработаны различные методики. Региональное распределение альвеолярной вентиляции исследуют с помощью радиоактивного газа (например, 133Хе), добавляя его во вдыхаемый испытуемым воздух, а затем измеряя радиоактивность над разными участками грудной клетки. Таким же образом изучают и распределение перфузии: вводят внутривенно раствор, содержащий радиоактивный газ; при прохождении крови через легкие этот газ диффундирует в альвеолы; об
объеме локальной перфузии легких судят по величине радиоактивности над разными участками грудной клетки. В сочетании оба этих метода позволяют количественно оценивать региональное распределение V’a/Q’ [31, 32].
На рис. 21.25 приведены результаты подобного исследования у здорового человека при горизонтальном положении тела. Вверху изображены точки, в которых производили измерения. Кривая внизу дает значения РO2 (по оси абсцисс) и РCO2 (по оси ординат) в альвеолах для различных значений V’a/Q’, т.е. величины парциального давления дыхательных газов, которые определяются условиями газообмена в различных участках легких. В области верхушек легких V’a/Q’ составляет 3,0; парциальные давления дыхательных газов при этом равны: РO2 =131 мм рт. ст., РCO2 = 29 мм рт. ст. В области же основания легкихVa’/Q’ = 0,65; в этом случае РO2 = 89 мм рт. ст. и РCO2 = 42 мм рт. ст. В других участках легких имеются соответствующие промежуточные значения. Эти местные различия в вентиляционно–перфузионном соотношении обусловлены главным образом неравномерным распределением легочного кровотока; альвеолярная вентиляция также увеличивается в направлении от верхушек легких к основаниям, но значительно меньше, чем перфузия.
На рис. 21.26 изображены физиологические последствия неравномерности соотношения вентиляции и перфузии в легких. Для простоты альвеолярное пространство представлено лишь двумя участками, расположенными один над другим. Указанные величины альвеолярной вентиляции и перфузии относятся к обоим легким. При таких значениях
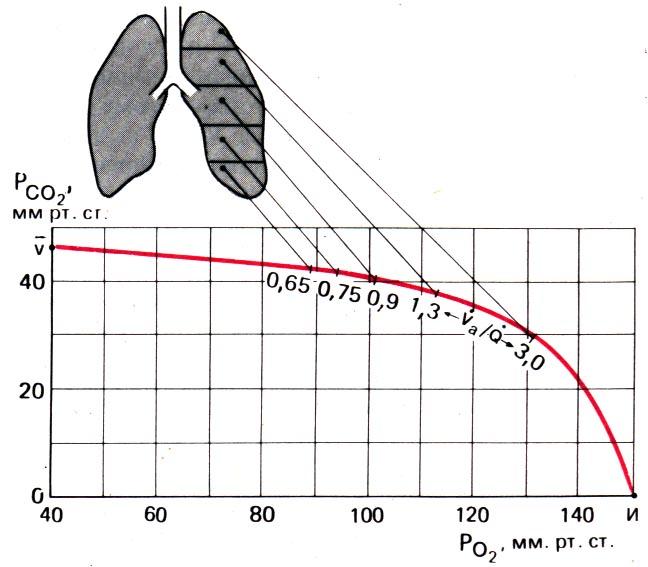
Рис. 21.25. Местные различия в вентиляционно–перфузионном соотношении V’a/Q’ (по [31] с изменениями). Красная кривая: значения РO2 (по оси абсцисс) и РCO2 (по оси ординат) для разных величин V’a/Q’ в различных участках легких. И–парциальное давление во вдыхаемом воздухе; v’ парциальное давление в смешанной венозной крови
этим важно установить «норму» для этих показателей: однако они, как и многие другие биологические параметры, колеблются в довольно широких пределах. Кроме того, напряжения дыхательных газов в крови претерпевают характерные возрастные изменения. Напряжение O2 в артериальной крови у здоровых молодых людей в среднем составляет около 95 мм рт. ст. (12,6 кПа); к 40 годам оно снижается примерно до 80 мм рт. ст. (10,6 кПа), а к 70 годам – приблизительно до 70 мм рт. ст. (9,3 кПа) [39]. Возможно, эти изменения связаны с тем, что с возрастом увеличивается неравномерность функционирования различных участков легких. Напряжение СO2 в артериальной крови, равное у молодых людей примерно 40 мм рт. ст. (5,3 кПа), с возрастом изменяется незначительно.
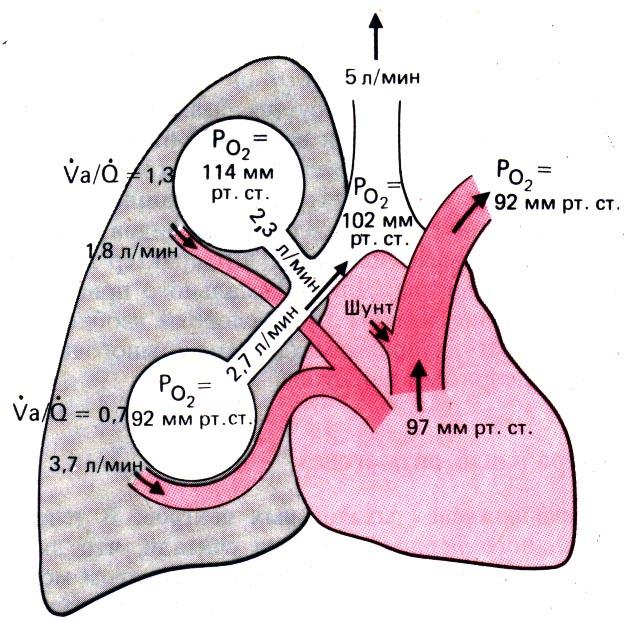
Рис. 21.26. Влияние региональной неравномерности вентиляции и перфузии на газообменную функцию легких в целом. Для простоты приведены лишь два участка с различными уровнями вентиляции и перфузии; допускается, что аналогичные условия создаются в обоих легких. Вследствие региональной неравномерности и наличия венозно–артериальных шунтов разница в РO2 между альвеолярным воздухом и артериальной кровью составляет 10 мм рт. ст.
этих показателей в верхнем участке альвеолярное PO2 должно составлять 114 мм рт. ст., а в нижнем–92 мм рт. ст. С учетом распределения альвеолярной вентиляции среднее альвеолярное РO2 =102 мм рт. ст. Когда же происходит смешивание крови, оттекающей от того и другого участков и по–разному насыщенной кислородом, РO2 в ней становится равным 97 мм рт. ст. Это означает, что в нижнем участке (более близком к основаниям) преобладает перфузия. За счет шунтового кровотока PO2 дополнительно снижается на 5 мм рт. ст., и в результате в артериальной крови становится равным 92 мм рт. ст. Таким образом, хотя во всех участках легких РO2 в капиллярах полностью уравновешено с РO2 в альвеолах, среднее артериальное PO2 на 10 мм рт. cm. меньше среднего альвеолярного PO2 из–за функциональной неравномерности V’a/Q’ и венозно–артериальных шунтов. По тем же причинам РCO2 в артериальной крови выше, чем в альвеолах, однако эта разница очень невелика и ее можно не учитывать.
Средние значения напряжений газов в артериальной крови. Конечный эффект внешнего дыхания отражает величины напряжения O2 и СO2 в крови системных артерий. По этим двум показателям можно судить о функции легких в целом. В связи с
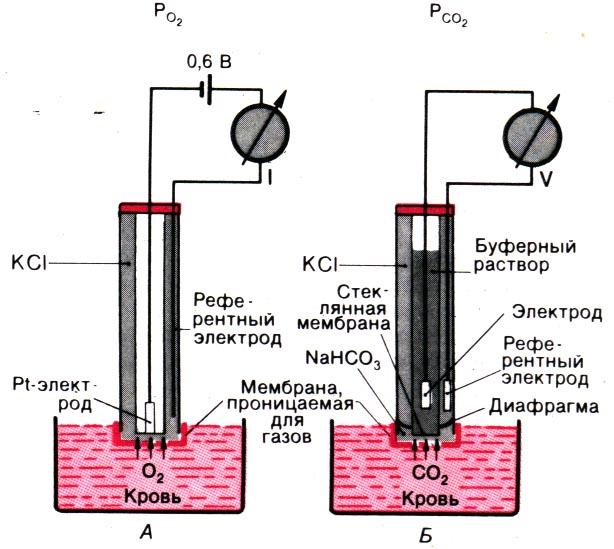
Рис. 21.27. Упрощенная схема прибора для измерения PO2 и РСO2 крови. А. Измерение PO2. В замкнутой цепи, включающей платиновый электрод и электрод сравнения, создается напряжение 0,6 В; электроды отделены от крови мембраной, проницаемой для газов (изображена красным). Молекулы O2 диффундируют через эту мембрану, и кислород восстанавливается на поверхности платинового электрода: в результате возникает электрический ток I, величина которого пропорциональна напряжению O2 между двумя поверхностями стеклянной мембраны, проницаемой для ионов H+, создается напряжение, величина которого пропорциональна рН. Это напряжение измеряется при помощи гальванометра; вся система отделена от крови мембраной, проницаемой для газов (изображена красным); через эту мембрану диффундируют молекулы СO2, и в результате рН раствора, окружающего стеклянную мембрану, изменяется. Таким образом, величина напряжения в цепи пропорциональна РCO2 в крови
Измерение напряжения и содержания газов в артериальной крови [35, 50]. Напряжение кислорода чаще всего измеряют полярографически (рис. 21.27, А). При этом используются два электрода – измеряющий (из платины или золота) и электрод сравнения. Оба их погружают в раствор электролита и поляризуют от источника напряжения (поляризующее напряжение = 0,6 В). При контакте с поверхностью благородного металла молекулы O2 восстанавливаются. В результате в замкнутой электрической цепи возникает ток, который можно измерить при помощи амперметра: величина этого тока при определенном значении приложенного напряжения прямо пропорциональна числу молекул O2, диффундирующих к поверхности электрода, т.е. напряжению O2 в растворе. Обычно раствор электролита, в который погружены электроды, отделен от исследуемой крови мембраной, проницаемой для кислорода. Измерительную аппаратуру можно сделать настолько миниатюрной, что для анализа напряжения O2 в артериальной крови потребуется всего несколько капель крови. Кровь при этом обычно берут из мочки уха, предварительно добившись того, чтобы кровоток в ней был максимальным. Необходимо, чтобы кровь не контактировала с воздухом при переносе ее в измерительную ячейку [44].
Напряжение СO2 также можно измерять в очень небольших порциях артериальной крови (рис. 21.27,5). В данном случае применяют электрод, который служит для измерения рН. Как и при определении напряжения кислорода, между жидкостью, окружающей электрод, и кровью помещают мембрану, проницаемую для газов, но не для ионов. Вследствие этого на рН раствора электролита (NaHC03) могут влиять только изменения напряжения СO2 в крови, и об этом напряжении можно судить по показаниям амперметра после его соответствующей калибровки. Измерять напряжение СO2 в небольшом количестве крови можно также при помощи метода Аструпа.
Если требуется измерить не напряжение, а содержание газов в крови, используют методы, при которых сначала полностью извлекают газы из крови, а затем измеряют их давление или объем. Чаще всего для этого используют манометрический аппарат Ван–Слайка (см. [3]). При работе с первыми образцами таких приборов требовались значительные количества крови (0,5– 2 мл), которые можно было получить лишь путем пункции артерии. В дальнейшем эта методика была усовершенствована, и теперь она позволяет измерять содержание O2 и СO2 в небольшом объеме крови.
