
OBSchAYa_KhIMIYa
.pdfРаспространенность, мас.% |
86,81 |
0,01 |
0,05 |
12,68 |
1,0 |
|
|
|
|
|
|
В качестве примера можно привести весьма характерную распространенность изотопов стронция и свинца (мас.%):
84Sr – |
0,56; |
86Sr – 9,86; |
87Sr – 7,02; |
88Sr – |
82,56; |
204Pb – |
1,4; |
206Pb – 24,7; |
207Pb – 21,16; |
208Pb |
– 52,74 |
Изотопный состав химических элементов в земной коре отражает многие геохимические процессы образования пород и руд. Одной из причин различного распределения изотопов в природных объектах служат геологические процессы. Расшифровка этих явлений на основании анализа возникшей изотопной смеси - одна из задач геохимии. Например, экспериментально определено соотношение изотопов кислорода - 18О (0,204 %) и 16О (99,759 %), однако в природных объектах их соотношение может изменяться на 10 %. Вариации изотопного состава кислорода в горных породах определяются в первую очередь температурой, при которой протекал процесс их формирования. Так изменение изотопного состава кислорода в карбонатах скелетов различных моллюсков свидетельствует о температуре древнего моря, в котором происходил их рост. Другой пример касается изотопного состава серы. К настоящему времени произошло разделение серы земной коры на две группы: серу биогенного происхождения (сульфиды, образование которых в природе осуществляется бактериальным путем), обогащенную изотопом 32S, и серу сульфатов, входящую в солевой остаток океанической воды, с большим содержанием изотопа 34S.
В состав земной коры входят 88 элементов, практически отсутствуют короткоживущие технеций, прометий, астат, франций и трансурановые элементы. Основу земной коры составляют всего восемь элементов: кислород, кремний, алюминий, натрий, железо, кальций, магний, калий – суммарный кларк которых составляет 98,5 мас.%. Далее по распространенности следует четыре элемента: титан, фосфор, водород и марганец. Распространенность всех других элементов меньше 0,6 масс.%.
Согласно геохимической классификации химических элементов В.М. Гольдшмидта
выделено четыре группы химических элементов, их названия отражают ту область Земли, где преимущественно встречаются входящие в нее элементы. Для ядра Земли характерна группа сидерофильных элементов, для земной коры – литофильных, для промежуточного слоя – мантии – группа халькофильных элементов и, наконец, атмосфера представлена группой атмофильных элементов.
Группа литофильных элементов характерна для горных пород земной коры и включает кислород, кремний, алюминий, кальций, магний, хлор, натрий, калий и другие. Железо, никель, кобальт, фосфор, платиновые металлы и другие элементы составляют группу сидерофильных элементов. Группа халькофильных элементов, имеющих высокое сродство к сере и встречающихся в рудных жилах, – сера, селен, теллур, мышьяк, медь, серебро, золото, цинк, свинец, ртуть и др. Элементы атмофильные: водород, азот и инертные газы.
Между химическими свойствами и распространенностью элементов имеется тесная зависимость. Специфика Земли заключается в преимущественной роли кислорода в составе земной коры (кларк кислорода составляет 49,13 масс.%), тогда как на Солнце он занимает скромное место. Причина этого заключается в прочной химической связи кислорода со многими элементами земной коры, что препятствует его удалению. Следующие по распространенности элементы земной коры – кремний и алюминий – отличаются способностью образовывать легкоплавкие соединения, а потому сравнительно легко накапливаются в шлаковой корке - земной коре. Таким образом, в земной коре преобладают кислородные соединения, из которых наиболее распространены силикаты, слагающие все главнейшие горные породы. Заметно менее распространены карбонаты, еще меньше – сульфидные и сульфатные минералы.
Преимущественно в виде оксидов в земной коре находятся такие металлы как железо, хром, марганец, никель, ванадий, вольфрам, в виде сульфидов – медь, олово, цинк, ртуть,
161
свинец, а также железо, никель и кобальт. Натрий, калий, рубидий чаще встречаются в виде хлоридов и сульфатов. Литий, бериллий и цезий входят в состав силикатов. Магний и щелочноземельные металлы образуют карбонатные и сульфатные минералы. Ряд металлов встречается в природе в виде простых веществ в самородном состоянии: палладий, платина, осмий, иридий, золото, серебро.
В зависимости от химической природы элемент может либо иметь свои минералы, либо сопутствовать другим элементам. Геохимики выделяют обширную группу элементов, для которых характерно равномерное распределение в земной коре, такие элементы называются рассеянными. Распространенность в земной коре и число разновидностей минералов не находятся в прямой зависимости. Так рубидий практически не имеет собственных минералов и является рассеянным элементом, тогда как менее распространенная медь образует собственные минералы, а потому к рассеянным элементам не относится.
В.И. Вернадский классифицировал химические элементы по способности образовывать химические соединения, концентрироваться, участвовать в циклических процессах, а также по радиоактивности и выделил шесть групп:
благородные газы;
благородные металлы - золото и платиновые металлы (Ru, Rh, Pd, Os, Ir, Pt);
циклические элементы - водород, углерод, кислород, азот, калий, магний, алюминий и др;
рассеянные элементы - литий, скандий, галлий, бром, рубидий и др.;
радиоактивные элементы;
редкоземельные элементы - иттрий, лантан, лантаниды.
162

ТЕМАТИЧЕСКИЙ СЛОВАРЬ Атомно-молекулярное учение
Атом - наименьшая электронейтральная частица химического элемента, являющаяся носителем его химических свойств и состоящая из положительно заряженного ядра и электронной оболочки.
Бертоллиды – вещества переменного состава.
Валентность – мера способности атома присоединять или замещать другие атомы или группы атомов при образовании химических связей. За единицу принята валентность атома водорода.
Дальтониды – вещества постоянного состава.
Закон Авогадро: в равных объемах различных газов при одинаковых температуре и давлении содержится одинаковое число молекул.
Закон постоянства состава: индивидуальное химическое вещество молекулярного строения имеет постоянный качественный и количественный состав, не зависящий от способа его получения.
Закон сохранения массы вещества: сумма масс продуктов реакции равна сумме масс веществ, вступивших во взаимодействие.
Закон эквивалентов: массы реагирующих веществ прямопропорциональны их эквивалентным массам.
m A Э А
m B Э В
Молекулярная частица - наименьшая устойчивая совокупность взаимосвязанных атомных частиц, являющаяся носителем химических свойств вещества.
Относительная атомная масса - отношение массы атома к 1/12 массы атома углерода изотопа 12С.
Относительная молекулярная масса - отношение среднеизотопической массы молекулы, вычисленной с учетом естественного природного содержания изотопов, к 1/12 массы атома углерода изотопа 12C.
Моль - количество вещества, содержащее столько структурных или формульных единиц, сколько атомов содержится в 12 г углерода изотопа 12С.
Молярная масса – масса одного моля вещества.
Уравнение состояния идеального газа: pV Mm RT ,
где m - масса газа, М – его молярная масса, р – давление, V – объем, Т – абсолютная температура, R – универсальная газовая постоянная (8,314 Дж/моль К).
Формульная единица вещества - простейшее соотношение между составляющими его элементами (брутто-формула).
Формульная масса – масса моля формульных единиц. Химический элемент – совокупность атомов с одинаковым заряда ядра.
Число Авогадро – это число структурных или формульных единиц в моле вещества
(NA = 6,022 1023 моль-1).
Эквивалент - это реальная или условная частица, отдающая или присоединяющая один катион водорода в реакциях кислотно-основного взаимодействия, один электрон в окислительно-восстановительных реакциях или взаимодействующая с одним эквивалентом любого другого вещества в реакциях обмена.
Эквивалентная масса вещества - это молярная масса его эквивалента.
Строение атома Уравнение Эйнштейна: E = m c2.
163
Волновая функция ( ) – это функция, определяющая вероятностные характеристики микрочастицы. Вероятность нахождения частицы в бесконечно малом объеме (dV) прямопропорциональна величине 2.
Главное квантовое число (n) принимает значения 0, 1, 2, … ∞ и обеспечивает квантование энергии электрона и средней его удаленности от ядра.
Граничная поверхность орбитали – поверхность, ограничивающая область пространства с заданной вероятностью нахождения в ней электрона.
Квантовые числа - это целочисленные параметры, входящие в выражение волновой функции и изменяющиеся на единицу. Каждое квантовое число обеспечивает квантование (дискретность) определенной физической величины.
Магнитное орбитальное (азимутальное) квантовое число (ml) принимает значения
0, 1 … l и обеспечивает квантование проекции орбитального момента количества движения электрона на одну из осей.
Магнитное спиновое квантовое число (mS) принимает значения от –S до +S и
определяет проекцию собственного вращательного момента количества движения микрочастицы на одну из осей; для электрона mS = 1/2.
Орбитальное квантовое число (l) принимает значения 0, 1 … (n-1) и обеспечивает квантование орбитального момента количества движения электрона, связанного с формой его орбитали.
Правило Клечковского: энергетические подуровни многоэлектронного атома заполняются электронами в порядке возрастания суммы главного и орбитального квантовых
чисел; при равных значениях суммы (n + ) сначала заполняется подуровень с меньшим значением главного квантового числа.
Правило Хунда: при заполнении энергетического подуровня электроны стремятся занять максимальное число орбиталей, ориентируя спин параллельно.
Принцип корпускулярно-волнового дуализма: любому движущемуся материаль-
ному объекту можно поставить в соответствие волновой процесс.
Принцип неопределѐнности: невозможно одновременно с высокой точностью определить положение электрона в пространстве (координаты) и его импульс.
Принцип Паули: для многоэлектронных систем невозможно существование двух электронов с одинаковым набором всех квантовых чисел.
Уравнение Шрѐдингера – основное уравнение квантовой механики
|
|
|
2 |
|
2 |
|
2 |
|
2 |
||
H = E |
|
|
|
|
|
|
|
|
|
|
|
или |
|
2m |
( x 2 |
y2 |
z2 )ψ Uψ = Eψ , |
||||||
|
|||||||||||
где H - оператор полной энергии (оператор Гамильтона, гамильтониан), Е - полная энергия системы.
Спиновое квантовое число (S) обеспечивает квантование собственного вращательного момента количества движения микрочастицы; для электрона S = ½.
Уравнение Планка: E = h , где h - постоянная Планка (6,625 10-34 Дж с), - частота излучения.
Электронная орбиталь – область околоядерного пространства¸ вероятность нахождения электрона в котором существенно отличается от нуля.
Электронная конфигурация – распределение электронов по орбиталям.
Химическая связь Валентный угол - это угол, образуемый условными прямыми, проведенными через
ядра центрального и присоединенных к нему атомов.
Внутренняя и внешняя гибридизация. Гибридизация с привлечением d-орбиталей предвнешнего энергетического уровня называется внутренней. Внешней гибридизацией называется гибридизация с использованием d-орбиталей внешнего уровня.
164

|
(n - 1)d |
|
|
ns |
|
np |
|
|
nd |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
sp3d2 |
внешняя гибридизация |
|
d2sp3
внутренняя гибридизация
Водородная связь – это связь атома водорода, связанного с сильно электроотрицательным партнером, с атомами других элементов.
Гибридизация – выравнивание энергии и симметрии атомных орбиталей за счет комбинирования их волновых функций при образовании химических связей.
Длина связи – среднее расстояние между ядрами взаимодействующих атомов. Дисперсионное взаимодействие – электростатическое притяжение мгновенных
микродиполей вещества.
Донорно-акцепторный механизм образования связи. Двухэлектронная связь обра-
зуется за счет свободной (вакантной) орбитали одного из атомов и неподеленной электронной пары другого атома по следующей схеме:
A  + B
+ B
 A
A B
B
Индукционное взаимодействие – электростатическое притяжение постоянных и наведенных (индуцированных) диполей вещества.
Ионная связь – химическая связь, реализованная за счет образования и электростатического притяжения разноименно заряженных ионов.
Ковалентность - мера способности атома к образованию связи, количественным выражением которой является число двуэлектронных связей, образуемых им по обменному и донорно-акцепторному механизму.
Металлическая связь – химическая связь, обусловленная взаимодействием электронного газа, образованного валентными электронами, с остовом положительно заряженных ионов кристаллической решетки.
Обменный механизм образования связи. Связывающие электронные пары форми-
руются из неспаренных электронов взаимодействующих атомов по следующей схеме:
A  + B
+ B
 A
A B
B
Ориентационное взаимодействие – электростатическое притяжение постоянных диполей вещества.
Полярная связь – асимметричная ковалентная связь между атомами с разной электроотрицательностью.
Принцип метода МО-ЛКАО: волновая функция молекулярной орбитали конструируется как линейная комбинация волновых функций атомных орбиталей.
Связывающие, несвязывающие и разрыхляющие молекулярные орбитали. Свя-
зывающая МО имеет энергию меньше энергии исходных атомных орбиталей, разрыхляющая МО имеет энергию больше энергии исходных атомных орбиталей. Несвязываюшие МО – это АО, перешедшие в молекулу без изменения.
Сигма-, пи- и дельта-связь. Сигма-связь ( -связь): перекрывание валентных орбиталей происходит вдоль линии связи, т.е. линии, соединяющей ядра взаимодействующих атомов. Пи-связь ( -связь): перекрывание орбиталей происходит в направлении, перпендикулярном линии связи (боковое перекрывание). Дельта-связь ( -связь): перекрывающиеся орбитали расположены в двух параллельных плоскостях, перпендикулярных линии связи.
Электронная конфигурация молекулы - распределение электронов по молекулярным орбиталям.
Энергия связи - энергия, которую необходимо затратить на ее разрушение.
165

Химическая термодинамика Внутренняя энергия - совокупность всех видов энергии термодинамической систе-
мы, кроме кинетической энергии ее движения как целого и потенциальной энергии ее положения во внешнем поле.
Второй закон термодинамики: в изолированной системе самопроизвольно протекаю процессы, приводящие к повышению энтропии.
Закон Гесса: тепловой эффект химической реакции определяется начальным и конечным состоянием системы и не зависит от пути проведения процесса и числа промежуточных стадий.
Компоненты системы – вещества, необходимые и достаточные для образования системы.
Первый закон термодинамики: увеличение внутренней энергии системы равно количеству теплоты, сообщенной системе, минус количество работы, совершенной системой против внешних сил.
Свободная энергия Гиббса – термодинамическая функция, определяемая соотноше-
нием: G = H - TS
Составная часть – индивидуальное химическое вещество, которое может быть выделено из термодинамической системы.
Стандартная теплота (энтальпия) образования - изменение энтальпии системы при синтезе одного моля вещества из простых веществ в стандартных условиях.
Термодинамическая вероятность – число микросостояний, которыми может быть реализовано данное макросостояние системы.
Термодинамическая система - тело или совокупность тел в объеме, ограниченном от окружающей среды реальными или условными перегородками.
Третий закон термодинамики: при температуре абсолютного нуля энтропия идеального кристалла равна нулю.
Уравнение Больцмана: S = RlnW
Фаза - совокупность частей системы, одинаковых по составу, физическим и химическим свойствам и отделенных от других частей системы поверхностями раздела.
Энтальпия – термодинамическая функция, определяемая соотношением: H = U + pV. Энтропия – термодинамическая функция, являющаяся мерой неупорядоченности си-
стемы.
Химическая кинетика и химическое равновесие Активированный комплекс - ассоциат частиц, участвующих в химической реакции,
в котором синхронно происходит разрыв старых и образование новых связей.
Закон действующих масс: для одностадийной реакции при постоянной температуре скорость прямопропорциональна произведению концентраций реагирующих веществ.
Катализ – изменение скорости реакции под действием катализатора.
Катализатор - вещество, изменяющие скорость химической реакции, но остающееся в результате реакции химически неизмененными и в неизменном количестве.
Константа скорости химической реакции – скорость химической реакции при еди-
ничных концентрациях реагирующих веществ.
Константа химического равновесия – отношение констант скоростей прямой и обратной реакции.
Порядок реакции – сумма показателей степеней при концентрациях реагентов в кинетическом уравнении реакции.
Правило Вант-Гоффа: при повышении температуры на каждые 10 градусов скорость гомогенной реакции возрастает в 2-4 раза.
T2 T1
k 2 k1 γ |
10 |
|
Принцип Ле Шателье: если на систему, находящуюся в состоянии динамического равновесия, оказано внешнее воздействие, то равновесие смещается в сторону процесса,
166

ослабляющего оказанное воздействие.
Скорость химической реакции - это число актов химического взаимодействия за единицу времени в единице реакционного пространства.
Ea
Уравнение Аррениуса: k A e RT , где А - предэкспоненциальный множитель, е - основание натурального логарифма, Еа - энергия активации процесса.
Энергия активации – минимальное количество энергии, которое необходимо сообщить системе, чтобы взаимодействие стало возможным.
Энтропия активации – функция, отражающая вероятность надлежащей ориентации взаимодействующих молекул. Изменение этой характеристики в процессе реакции определяется следующим соотношением:
ΔSa Rln W2 , W1
где W1 - число возможных ориентаций молекул, W2 - число благоприятных ориентаций.
Координационные соединения Внутренняя (координационная) сфера – совокупность центрального атома и свя-
занных с ним лигандов.
Внешняя сфера – совокупность атомных и молекулярных частиц, непосредственно не связанных с центральным атомом.
Дентатность - число мест, занимаемых лигандом в координационной сфере. Определяется числом -связей, которыми лиганд связан с центральным атомом.
Донорно-акцепторная и дативная связь в координационных соединениях.
Донорно-акцепторная связь реализуется по следующей схеме: М :L. Дативная связь ( -дативное взаимодействие) реализуется по схеме:
..  M
M  : L
: L
Координационные (комплексные) соединения. Координационными называются со-
единения, содержащие в своем составе многоатомные молекулы или ионы, имеющие центр координации, связанный с частицами, способными к самостоятельному существованию.
Координационное число – число мест в координационной сфере, которое определяется суммарным числом -связей, образованных центральным атомом с лигандами.
Параметр расщепления - разность энергий орбиталей d-подуровня центрального атома в поле лигандов.
Снятие вырождения d-орбиталей в октаэдрическом поле.
dz2, dx2-y2
+0,6 oкт
oкт
-0,4 oкт
|
|
dxy, dxz, dxz |
Свободный |
Поле |
Октаэдрическое |
ион |
сферической |
поле |
|
симметрии |
|
167
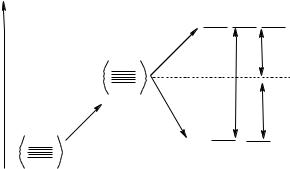
Снятие вырождения d–орбиталей в тетраэдрическом поле.
|
|
dxy, dxz, dxz |
|
|
+0,4 т |
|
|
т |
|
|
-0,6 т |
|
|
dz2, dx2-y2 |
Свободный |
Поле |
Тетраэдрическое |
ион |
сферической |
поле |
|
симметрии |
|
Хелаты - координационные соединения, содержащие во внутренней сфере циклы, включающие центральный атом.
Центральный атом и лиганды. Атом или ион, занимающий центральное положение в комплексе, называется центральным атомом. Молекулы или ионы, непосредственно связанные с центральным атомом, называются лигандами.
Теория растворов Активность и коэффициент активности. Активность – это эффективная концен-
трация, с которой частица проявляет себя в растворе. Рассчитывается по уравнению а = f С, где – f – коэффициент активности.
Водородный показатель – отрицательный десятичный логарифм концентрации катионов водорода, pH = -lg[H+].
Гидролиз солей – обменное взаимодействие ионов соли с водой. Диаграмма состояния отражает зависимость между температурой и давлением
насыщенного пара вещества.
Закон Вант-Гоффа: осмотическое давление раствора равно давлению, которое оказывало бы растворенное вещество, находящееся в газообразном состоянии и занимающее объем, равный объему раствора.
Ионная сила раствора – полусумма произведений концентраций всех ионов, присутствующих в растворе, на квадрат их заряда: μ = 0,5ΣСizi2
Ионизация – образование ионов при взаимодействии молекул растворенного вещества с растворителем.
Ионное произведение воды – произведение равновесных концентраций катионов водорода и гидроксид-анионов в водных растворах: Kw = [H+][OH-] при 25 С Кw = 1 10-14.
Кислоты и основания Бренстеда-Лоури. Кислота Бренстеда – это донор протонов, основание Бренстеда – это акцептор протонов.
Кислоты и основания Льюиса. Кислота Льюиса – акцептор неподеленной электронной пары, основание Льюиса – донор неподеленной электронной пары.
Кислоты и основания в теории сольвосистем. Кислота - это вещество, отщепляю-
щее в растворе тот же катион, что и растворитель. Основание - это вещество, отщепляющее в растворе тот же анион, что и растворитель.
Константа ионизации – константа равновесия в растворе слабого электролита.
Константа кислотности и константа основности – константа равновесия, устано-
вившегося в растворе результате ионизации (диссоциации) кислоты или основания.
Константа устойчивости комплексного иона – константа равновесия, которое устанавливается в растворе при образовании комплексной частицы из центрального иона и лигандов.
Концентрация раствора – количественное соотношение между растворителем и растворенными веществами в растворе.
168

Коэффициент растворимости - масса растворенного вещества, образующего насыщенный раствор со 100 г растворителя.
Массовая доля - отношение массы растворенного вещества к массе раствора
ω m1 m
Мольная доля - отношение количества данного компонента к суммарному количеству всех компонентов раствора
1 |
|
|
|
1 |
|
0 |
1 ... |
||||
|
|
||||
Моляльность - отношение количества растворенного вещества к массе растворителя, выраженной в кг
|
1000 |
1 |
|
1000m |
|
Cm |
|
|
1 |
, |
|
m0 |
|
M1m0 |
|||
|
|
|
|
где m1 и m0 - массы растворенного вещества и растворителя в г, М1 - молярная масса растворенного вещества.
Молярность - отношение количества растворенного вещества к объему раствора
С |
ν1 |
|
m1 |
, |
|
|
|||
1 |
V |
|
M1 V |
|
|
|
|||
где m1, M1 и ν1 - масса, молярная масса и количество растворенного вещества. Нормальность - отношение количества эквивалента растворенного вещества к объ-
ему раствора
N |
ν1 |
|
m1 |
, |
|
|
|||
1 |
V |
|
MЭV |
|
|
|
|||
где МЭ - эквивалентная масса растворенного вещества.
Осмос – односторонняя диффузия растворителя через полупроницаемую мембрану. Осмотическое давление - осмотическое давление раствора равно давлению, которое
оказывало бы растворенное вещество, находящееся в газообразном состоянии и занимающее объем, равный объему раствора.
Правило фаз: С + Ф = К + 2, где С - число степеней свободы, Ф - число фаз, К - число компонентов.
Первый закон Рауля: относительное понижение давления насыщенного пара над раствором равно мольной доле растворенного вещества:
p0 p1 |
|
ν1 |
или p p |
|
ν0 |
|
, |
p0 |
|
ν0 ν1 |
1 |
0 ν0 |
ν1 |
||
где р0 и р1 - давление насыщенного пара над растворителем и раствором, ν0 и ν1 - количество растворителя и растворенного вещества.
Произведение растворимости – произведение равновесных концентраций ионов малорастворимого электролита в насыщенном растворе.
Растворы - это однородные (гомогенные системы), состоящие из двух и более компонентов.
Растворимость - способность вещества переходить в раствор. Количественной мерой растворимости является концентрация насыщенного раствора. Насыщенным называется раствор, находящийся в динамическом равновесии с избытком растворяемого вещества.
Степень диссоциации (ионизации) – отношение количества электролита, распавшегося на ионы, к общему его количеству в растворе.
Уравнение Дебая – Хюккеля: lgf 0,5z2 
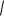 μ , где f – коэффициент активности, z –
μ , где f – коэффициент активности, z –
1 
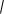 μ
μ
заряд иона, - ионная сила раствора.
Электролитическая диссоциация – распад электролита на ионы под действием растворителя или высокой температуры при плавлении.
Энтальпия растворения – тепловой эффект растворения одного моля вещества в
169

бесконечно большом объеме растворителя.
Окислительно-восстановительные реакции Анод – электрод, на котором идет процесс окисления.
Восстановление – процесс понижения степени окисления, который можно рассматривать как присоединение атомом электронов.
Восстановитель – элемент, отдающий электроны и повышающий степень окисления.
Гальванический элемент - устройство, в котором энергия окислительно-восстано- вительной реакции преобразуется в энергию электрического тока.
Диспропорционирование и сопропорционирование – окислительно-восстанови-
тельные реакции, сопровождающиеся изменением степени окисления одного и того же элемента.
Закон Фарадея: масса выделившегося на электроде вещества пропорциональна количеству электричества, прошедшего через раствор или расплав.
m MЭ IFτ ,
где m - масса продукта электролиза, I - сила тока, - время пропускания тока, F – постоянная Фарадея (96485 Кл.моль-1), Мэ - эквивалентная масса вещества.
Катод – электрод, на котором идет процесс восстановления.
Направление окислительно-восстановительной реакции. В процессе ОВР из двух окисленных форм восстанавливается та, для которой электродный потенциал больше, а из двух восстановленных форм окисляется та, для которой электродный потенциал меньше.
Окисление – процесс повышения степени окисления, который можно рассматривать как потерю атомом электронов.
Окислитель – элемент, присоединяющий электроны и понижающий степень окисления.
Окислительно-восстановительные реакции – это реакции, сопровождающиеся из-
менением степеней окисления элементов.
Стандартный окислительно-восстановительный потенциал - разность потенциа-
лов, возникающая на поверхности инертного электрода, погруженного в раствор, содержащий окисленную и восстановленную форму вещества в стандартных условиях.
Стандартный электродный потенциал - разность потенциалов, возникающая на поверхности металлического электрода, погруженного в раствор, содержащий ионы данного металла в стандартных условиях.
Степень окисления - формальный заряд, рассчитанный в предположении, что электроны, участвующие в образовании химических связей, полностью смещены к партнеру с большей электроотрицательностью, т.е. все химические связи рассматриваются как ионные.
Уравнение Нернста: E E |
RT |
ln |
Coxx |
, при 298 К E E |
0,059 |
lg |
Coxx |
, |
|
nF |
y |
||||||||
|
|
|
n |
y |
|||||
|
|
|
Cred |
|
Cred |
||||
где R - универсальная газовая постоянная, Т - абсолютная температура, n - число электронов, соответствующее переходу окисленной формы в восстановленную, F – постоянная Фарадея (96485 Кл·моль-1), Cox и Cred - концентрации окисленной и восстановленной формы, x и y - коэффициенты в уравнении полуреакции, Е˚ - стандартный электродный потенциал.
Электролиз – совокупность окислительно-воссстановительных реакций, протекающих на электродах при пропускании электрического тока через раствор или расплав электролита.
Периодический закон и периодическая система химических элементов Группа - совокупность элементов с одинаковым числом валентных электронов, т.е.
170
