
КХ часть 1
.pdf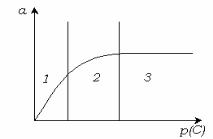
Энергия притяжения при адсорбции зависит от расстояния в третьей степени вместо шестой, как это имеет место при взаимодействии двух атомов. Такая зависимость указывает на более медленное уменьшение энергии притяжения при адсорбции и на дальнодействие адсорбционых сил. Полная потенциальная энергия взаимодействия при адсорбции выражается уравнением
U |
B |
|
C n |
(3.6) |
|
r12 |
6r3 |
||||
|
|
|
где n - число атомов в единице объема адсорбента. Важными практическим выводом при рассмотрении природы адсорбционных сил является вывод о том, что, когда преобладают дисперсионные силы,
наблюдается лучшая адсорбция в трещинах и порах, т.к. вблизи адсорбированной молекулы находится большое число атомов твердого тела. Если преобладают электростатические силы, то в трещинах и порах заряды компенсируют друг друга, и наибольший потенциал оказывается на выступах, где и будет преобладать адсорбция, особенно при образовании водородных связей.
3.8. Изотермы адсорбции
Вид изотермы адсорбции изображен на рис. 3.10.
Рис. 3.10. Изотерма адсорбции 1 типа.
68
агрегируют, что хорошо известно из теории устойчивости коллоидных систем.
Агрегация коллоидных частиц (УДЧ) характеризуется особенностями роста и геометрического строения. Эти частицы участвуют в броуновском движении, двигаясь по траектории случайного блуждания. Слипание частиц друг с другом (агрегация)
наиболее интенсивно протекает на значительном удалении от места зарождения коллоидного агрегата, т. е. на его периферии. Поэтому агрегат имеет сильно разветвленную структуру. С увеличением размера агрегата ( r ) его плотность ( ) уменьшается, и при r ,
0. Были получены агрегаты оксидных частиц необычайно низкой плотности, когда только 2% объема материала заняты веществом, а
98% приходится на пустоты. Такие материалы называются
фрактальным агрегатом или фрактальным кластером. Последний внешне выглядит как неупорядоченная система, но характеризуется внутренним порядком, определяемым фрактальной размерностью df . Фрактальная размерность - это дробная величина,
характеризующая структуру и степень открытости коллоидного агрегата. Размерность фрактального кластера, являясь дробной величиной, не совпадает с размерностью пространства, в котором существует кластер (размерность пространства - целая величина).
Фрактальную размерность можно рассматривать также, как характеристику рыхлости агрегата. Чем меньше фрактальная размерность, тем более рыхлым является фрактальный кластер.
21
www.mitht.ru/e-library

1.7. Влияние дисперсности на свойства вещества
Основными критериями ультрадисперсного (коллоидного)
состояния являются следующие:
Малая кинетическая подвижность частиц вследствие высокой массы частицы по сравнению с молекулой.
Гетерофазность.
Адсорбционные явления на поверхности.
Стабилизация системы за счет снижения поверхностной энергии третьим компонентом.
Высокая чувствительность к малым добавкам электролитов.
Высокодисперсные системы характеризуются особыми
свойствами. Вследствие малого размера частицы в них не оседают.
Рассеяние света такими системами приводит к их мутности.
Высокая удельная поверхность таких систем приводит к возрастанию роли поверхностных слоев. По мере дробления в системе происходят качественные изменения. При переходе от грубо дисперсных систем к высокодисперсным системы приобретают седиментационную устойчивость, возрастает прочность и растворимость, растет взрывоопасность. Из-за увеличения кривизны поверхности увеличивается химическая активность.
Ультрадисперсные частицы могут на воздухе воспламеняться. С
увеличением степени дисперсности изменяются все свойства вещества.
С изменением дисперсности изменяются условия протекания многих химических реакций. Так, реакция обжига известняка с повышением дисперсности сдвигается вправо:
CaCO3 CaCO CO2
22
На очень близких расстояниях при перекрывании электронных оболочек атомов, возникает отталкивание, называемое борновским
отталкиванием и описываемое эмпирическим соотношением:
U от |
В |
(3.5) |
|
r12 |
|||
|
|||
Полная энергия межмолекулярного взаимодействия определяется |
|||
уравнением Леннард-Джонса U |
C |
|
B |
|
|
|
, где C - константа |
||
r6 |
r12 |
|||
межмолекулярного притяжения, B - константа борновского отталкивания, происходящего при перекрывании электронных орбит,
C B
r6 - энергия межмолекулярного (дисперсионного) притяжения, r12 -
энергия борновского отталкивания, которое происходит при малых r и
обусловлено запретом Паули. Потенциал притяжения всегда отрицателен, а потенциал отталкивания - положителен.
Межмолекулярные силы действуют на малых расстояниях порядка 10-9 м. При адсорбции дисперсионные силы действуют одновременно между молекулами адсорбата и поверхностью, т.е.
многими атомами адсорбента. Дисперсионные силы обладают свойством аддитивности, происходит суммирование адсорбционных сил, и суммарный потенциал адсорбции определяется выражением
U U |
i |
C |
1 |
B |
1 |
. |
r6 |
|
|||||
|
|
|
r12 |
|||
В результате суммирования парных взаимодействий, т. е.
тройного интегрирования по объему адсорбента, степень r
уменьшается, и межмолекулярное взаимодействие увеличивается.
Поэтому адсорбционные силы значительны, и действуют на больших
расстояниях по сравнению с межмолекулярными силами rАД 10 7 м.
67
www.mitht.ru/e-library

Адсорбент |
Адсорбат |
Силы |
|
взаимодействия |
|||
|
|
||
полярный |
полярный |
Ориентационные |
|
полярный |
неполярный |
индукционные |
|
неполярный |
полярный |
||
|
|||
неполярный |
неполярный |
дисперсионные |
|
|
|
|
Дисперсионные силы проявляются между мгновенными диполями,
возникающими при сближении молекул за счет флуктуаций электронной плотности. Резонанс таких флуктуаций приводит к уменьшению общей энергии системы, обусловленному притяжением атомов. Потенциал межмолекулярного взаимодействия определяется
выражением:Uмежмол.взаим. Uор Uинд Uдисп .
Если оценить вклад каждого из трех типов взаимодействий -
ориентационного, индукционного и дисперсионного в общую энергию притяжения молекул, то оказывается, что доля индукционного эффекта составляет не более 5%. Доля ориентационного эффекта зависит от дипольных моментов взаимодействующих молекул. Для таких сильно полярных молекул, как аммиак и вода, ориентационный эффект равен дисперсионному. Следовательно, для неполярных и слабополярных молекул основным типом межмолекулярного
взаимодействия является дисперсионное.
Различные виды межмолекулярного взаимодействия характеризуются одним и тем же законом изменения энергии
притяжения от расстояния между молекулами U |
пр |
С |
r - |
|
|
, где |
|||
r6 |
||||
расстояние между центрами атомов или молекул, C - константа, в
которую входят электрические и магнитные характеристики молекул или атомов, соответствующие для каждого эффекта.
66
Удаление кристаллизационной воды из грубодисперсного оксида алюминия Al2O3 3H2O происходит при 473K , а из коллоидного
оксида - на 100 ниже, т. е. при 373K . Коллоидное золото растворяется в соляной кислоте.
Ещё одним примером влияния дисперсности на свойства является изменение свойств воды при дроблении. С уменьшением размера капель воды давление пара над каплей увеличивается. При диаметре капель, равном 1 10 8 м, отношение давления пара над каплей при данной температуре p к давлению над плоской поверхностью воды
p
pO, pO 1,108. Повышенному давлению пара отвечает пониженная
температура замерзания капель воды. Это явление имеет большое значение в живой природе, обеспечивая жизнеспособность растений при низкой температуре.
В ультрадисперсных твердых частицах размером 10 7 м может происходить коренная перестройка расположения атомов. Из-за большой кривизны поверхности возникают значительные внутренние напряжения, что приводит к изменению физических свойств веществ.
Так, температура плавления серебра сильно зависит от размера частиц и равна: при размере частиц 5 10 8 м - 973K , 2 10 8 м -
593K , тогда как крупные частицы серебра плавятся при 1233K .
Ввысокодисперсных системах повышается температура перехода
всверхпроводящее состояние. Возникает возможность получения высокотемпературных сверхпроводников.
Явление сверхпроводимости было открыто в 1911 году голландским физиком Камерлинг-Онессом. Он обнаружил, что при температуре, близкой к абсолютному нулю, ртуть почти полностью
23
www.mitht.ru/e-library
теряет электрическое сопротивление, т.е. переходит в сверхпроводящее состояние. Для практического использования явления сверхпроводимости, например с целью передачи электроэнергии без потерь на большие расстояния, необходимо получать сверхпроводники при более высокой температуре. В 1986-87
годах в Швейцарии, США, Японии, СССР был открыт класс новых керамических материалов, сверхпроводящих при температуре жидкого азота. Эти материалы изготовлены на основе иттрия и являются дисперсными системами.
В последнее время обнаружены неустойчивые фазы новых керамических материалов, в которых наблюдаются переходы,
начинающиеся при . Чтобы сделать их практически доступными, нужно изучить их фазовую структуру и свойства. Уже в настоящее время возможно применение этих материалов в сверхпроводниковой электронике и вычислительной технике.
Таким образом, в высокодисперсном состоянии вещество обладает особыми свойствами. Это состояние является промежуточным между свободными атомами или молекулами и массивными образцами.
1.8. Значение коллоидной химии в природе и технике
Дисперсные системы и поверхностные явления имеют громадное значение в природе и технике. Без преувеличения можно сказать, что весь реальный окружающий нас мир состоит из дисперсных систем.
Законы коллоидной химии управляют жизнью крошечной клетки живого организма. Свойства реальных тел и материалов определяются не только их составом, но и коллоидно-химической структурой, т.е. фазовой структурой, размером частиц, их
24
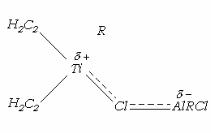
Циглера-Натта входит титан. Активный центр комплексного катализатора имеет вид:
Рис.3.9.
На атоме Ti происходит предварительная координация молекул мономера.
Развитие химической промышленности, в том числе промышленности синтетических каучуков, идет с учетом экологических проблем. Так на заводах СК бутадиеновый каучук СКД получается на катализаторах Циглера-Натта. При этом образуется сильно пахнущие,
летучие и токсичные олигомеры бутадиена, загрязняющие атмосферу в производственной и жилой зоне. Поэтому на в последние годы осваивается производство каучука на редкоземельном неодимовом катализаторе. В этом процессе олигомеры бутадиена, загрязняющие атмосферу, не образуются.
3.7. Природа адсорбционных сил
Физическая адсорбция происходит под действием Ван-дер Ваальсовых сил межмолекулярного взаимодействия, которое складывается из ориентационных, индукционных и дисперсионных сил.
Ниже показана природа взаимодействия в зависимости от характера адсорбента и адсорбата. Полярным веществом называется
вещество, обладающее интенсивным полем межмолекулярных сил.
65
www.mitht.ru/e-library

3.6. Значение координационных связей при
хемосорбции
Хемосорбция может быть обусловлена образованием как ковалентных, так и координационных связей. Это показано при изучении адсорбции различных адсорбатов на поверхности металлов.
Во всех случаях, независимо от природы адсорбата, наблюдаются определенные закономерности адсорбции. Первая закономерность заключается в том, что интенсивность хемосорбции велика для переходных металлов. Вторая закономерность состоит в том, что, с
увеличением атомного номера металла в одной группе интенсивность хемосорбции снижается, т. к. уменьшается возможность образования координационных связей.
В качестве примера на рис. 4.8 показано изменение теплоты адсорбции Qa на поверхности металлов первой переходной группы, с
увеличением атомного номера металла.
Рис. 3.8. Зависимость теплоты адсорбции Qa на поверхности металлов от
атомного номера металла
Эти закономерности важны для понимания механизма катализа.
Так в состав катализатора стереоспецифической полимеризации
64
относительным расположением и взаимодействием друг с другом и дисперсионной средой.
Примерами дисперсных систем в природе являются почва, горные породы, облака, дымы, туманы; а в живой природе - биоколлоиды,
биомембраны, клетки и ткани, кровь, размер частиц которой 7 10 6 м.
Такие продукты питания как молоко, мясо, хлеб, а также лекарственные вещества тоже являются дисперсными системами.
Основу научно-технического прогресса составляют три направления: новые источники энергии, новые материалы и новые информационные системы. Коллоидная химия в настоящее время определяет развитие каждого направления. Ультрадисперсные катализаторы позволяют осуществлять фотохимическое восстановление воды до водорода, что создает реальные предпосылки для развития экологически чистой солнечно-
водородной энергетики. Новые композиционные материалы,
называемые нанокомпозитами, включающие металлы, полимеры и керамику, получаются из ультрадисперсных порошков или с использованием ультрадисперсных наполнителей. Компьютеры нового поколения создаются с использованием моно- и мультислоев ПАВ
(пленок Ленгмюра-Блоджетт).
Высокая прочность всех трех основных классов конструкционных материалов (металлических сплавов, керамики и полимерных композитов) определяется их фазовой структурой, например,
соответствующей образованию игольчатых кристаллов одной фазы в матрице другой фазы. Такие игольчатые кристаллы образуются в металлических сплавах, цементном камне, кристаллических полимерах. Эти кристаллы оказывают упрочняющее действие благодаря тому, что микротрещина, зарождающаяся в матрице, при встрече с кристаллом прекращает свой рост. Происходит
25
www.mitht.ru/e-library
перераспределение напряжения по многим связям, микротрещина разряжается, и для дальнейшей деформации материала требуется новое напряжение. Так реализуется общий принцип прочности и усиления материалов - равномерное распределение напряжений по нагруженным связям.
Коллоидная химия имеет большое значение в химической технологии. Такие процессы и явления, как дробление, растворение,
кристаллизация, флотация, гетерогенный катализ основаны на глубоком изучении поверхностных явлений.
В последнее время большое значение в технике и технологии получили мембранные методы разделения сложных смесей: обратный осмос, ультрафильтрация, испарение через мембрану, диализ.
Движущими силами, вызывающими перенос вещества в этих процессах, являются разность концентраций, давлений, химических или электрических потенциалов. Этими методами разделению подвергаются как газовые, так и жидкие смеси. В химической и нефтехимической промышленности мембранные методы используются для разделения смесей высоко- и низкомолекулярных соединений, эмульсий, выделения гелия и водорода из природных газов, кислорода из воздуха. В электронной промышленности,
потребляющей большоеколичество ультрачистой воды, мембранным методом получают воду, по чистоте превосходящую бидистиллат.
В пищевой промышленности мембранные методы применяются для получения высококачественного сахара, стабилизации пива и виноградных вин, очистки воды методом обратного осмоса для приготовления высококачественной водки, концентрирования фруктовых и овощных соков.
26
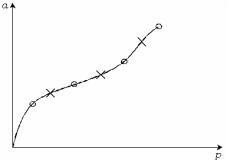
одинаковы. совпадают и изотермы адсорбции одного газа на разных адсорбентах. В качестве примера на рис. 3.7 приведена изотерма
адсорбции азота на TiO2 и BaSO4 .
Рис. 3.7. Изотерма адсорбции N2 на TiO2 (0) и BaSO4 (x).
Адсорбция зависит от величины поверхности адсорбента и от энергии взаимодействия между поверхностью и газом. Энергия взаимодействия характеризуется теплотой физической адсорбции,
которая примерно равна теплоте конденсации газа и не зависит от адсорбента. Решающим фактором в физической адсорбции является не природа адсорбента, а величина его поверхности.
В отличие от физической адсорбции хемосорбция специфична,
т.е. данное вещество хемосорбируется только на определенных адсорбентах. В хемосорбции более важен энергетический фактор, а
не величина поверхности.
При хемосорбции адсорбция возможна вследствие самопроизвольного уменьшения энергии Гиббса всей системы, что может привести даже к увеличению поверхностной энергии. Это
возможно в том случае, если Gхим GS .
63
www.mitht.ru/e-library

Рис. 3.6. Изобары физической адсорбции ( a) и хемосорбции ( в)
При низкой температуре протекает только физическая адсорбция,
а хемосорбция не протекает. При высокой температуре протекает хемосорбция, а физическая адсорбция пренебрежимо мала.
Кривая (a) соответствует равновесной физической адсорбции, (b) - хемосорбции. На обоих этих участках адсорбция обратима и равновесна. На участке (c) протекают оба процесса: физическая адсорбция и хемосорбция. Для хемосорбции на этом участке значения равновесной адсорбции велики, но скорость установления равновесия мала.
Степень равновесной адсорбции при температуре, при которой скорость хемосорбции низка, но не пренебрежимо мала, представлена неравновесной кривой (с), расположение которой зависит от времени,
необходимого для достижения равновесия.
Четвертое отличие физической адсорбции от хемосорбции состоит в том, что физическая адсорбция неспецифична, а
хемосорбция специфична. Неспецифичность физической адсорбции означает, что данное вещество примерно одинаково адсорбируется на разных адсорбентах. Это проявляется в том, что теплоты физической адсорбции данного газа на различных адсорбентах
62
В микробиологической и медицинской промышленности эти методы применяются для очистки и выделения биологически активных веществ, лекарственных веществ, для очистки крови.
Мембранные методы имеют большое значение для охраны окружающей среды. Они позволяют создавать безотходные производства путем организации замкнутого водооборота и утилизации ценных вредных веществ. Из сточных вод сыроваренных заводов извлекаются белок, лактоза и витамины. Мембранные методы широко применяются для опреснения соленой воды. В 1970 году этими методами получали всего 1% пресной воды, в 1980 году –
50%, а в настоящее время почти вся опресненная вода получается мембранными методами.
Особое значение коллоидно-химические явления имеют в переработке полимеров. Примерами типично коллоидных полимерных систем являются кристаллические полимеры, дисперсии, латексы,
наполненные полимеры, смеси полимеров, блок-сополимеры,
пластизоли, нетканые материалы и другие.
Кристаллические полимеры имеют ряд существенных отличий по сравнению с низкомолекулярными кристаллами. Эти отличия проявляются уже на стадии образования кристаллов. Если низкомолекулярные жидкости кристаллизуются только при охлаждении ниже температуры кристаллизации, то полимеры кристаллизуются также при растяжении. Кристаллизация полимеров при растяжении -
причина высокой прочности резин из кристаллизующихся каучуков:
натурального, синтетического полиизопренового, цис-
полибутадиенового, полихлоропренового, которая достигает
150 160кг см. Каучуки, не способные кристаллизоваться, например бутадиен-стирольный, позволяют получать резины с прочностью всего
см. Каучуки, не способные кристаллизоваться, например бутадиен-стирольный, позволяют получать резины с прочностью всего
27
www.mitht.ru/e-library

23 30 кг см. Гигантские молекулы полимеров состоят из
см. Гигантские молекулы полимеров состоят из
кинетических единиц, называемых сегментами. Кристаллические полимеры однофазны по отношению к макромолекуле. В то же время кристаллические полимеры по отношению к сегменту представляют собой двухфазную систему, в которой нельзя отделить кристаллическую фазу от аморфной, в отличие от низкомолекулярных систем. Это является следствием того, что отдельные полимерные молекулы большого размера находятся одновременно в кристаллической и аморфной фазе. Таким образом, можно говорить о том, что в полимерах молекулы больше, чем кристалл, по своему размеру. Кристаллическая фаза переходит в аморфную непрерывно, в
кристаллическом полимере отсутствуют четкие границы раздела между фазами.
Кристаллизация в полимере протекает во времени. Вначале кристаллизуются наиболее подвижные участки макромолекул, затем -
менее подвижные. Это приводит к двум важным следствиям. Во-
первых, полимерные кристаллы плавятся не при одной температуре,
как низкомолекулярные, а в интервале температур. Вспомним, что в органической химии четкая температура плавления является критерием чистоты вещества. Во-вторых, интервал плавления зависит от возраста кристалла. Чем дольше хранился кристалл, чет выше его интервал плавления. Так, натуральный каучук, пролежавший в течение
30 лет на дне Атлантического океана, имел температуру плавления
60 С по сравнению с 10 С для кристаллов каучука, хранившегося
в течение одного года.
Большой интерес с коллоидно-химической точки зрения представляют наполненные полимеры. Наполнение - это сочетание полимера с твердыми, жидкими и газообразными веществами,
которые относительно равномерно распределяются в объеме
28
Эти кривые объясняют наблюдающуюся обычно быструю сорбцию в начале процесса и медленную в дальнейшей стадии.
Кривая (2) отвечает хемосорбции, идущей для первых порций адсорбата ( 0) с выделением значительной энергии,
уменьшающейся по мере заполнения поверхностного слоя (кривая (3)
для 0,8). При приближении молекулы к поверхности в области больших расстояний процесс идет по кривой (1) (скорость велика,
EQ 0), и переход на кривую (2) происходит без барьера. В
дальнейшем, при значительной степени заполнения поверхности, для перехода от кривой (1) к кривой (3) требуется преодолеть активационный барьер, равный энергии активации хемосорбции. Такая хемосорбция называется активированной. Величина энергии активации зависит от формы кривых физической адсорбции и хемосорбции и сильно отличается для разных систем. Она является очень низкой для хемосорбции водорода на металлических поверхностях. Энергия активации входит в выражение для скорости
E q
хемосорбции типа уравнения Аррениуса: V V0 e RT .
Если энергия активации хемосорбции велика, то скорость хемосорбции при низкой температуре настолько мала, что протекает только физическая адсорбция.
На рис. 3.6 показано изменение степени адсорбции газа на твердой поверхности в зависимости от изменения температуры при постоянном давлении (изобара адсорбции).
61
www.mitht.ru/e-library
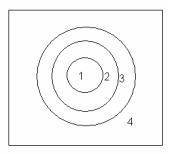
физической адсорбции, а теплота хемосорбции значительно превышает теплоту физической адсорбции.
Пересечение кривой 1 с 2 и 3 отражает переход от физической адсорбции к химической. Правый и левый верхние участки кривых 2 и
3 и левый верхний участок кривой 1 не реализуются.
Результирующая кривая хемосорбции имеет максимум,
образующийся при пересечении кривых 1 и 3 и соответствующий энергии активации адсорбции. При пересечении кривых 1 и 2
максимум отсутствует, что соответствует протеканию процесса без
энергии активации.
Таким образом кривая (1) описывает изменение энергии
физического взаимодействия между металлом M и газом X2 . Она
включает в себя Вандер-Ваальсовы (диполь-дипольные и лондоновские) силы притяжения и борновские силы отталкивания.
Кривые (2) и (3) описывают хемосорбцию, в которой молекула адсорбата вначале диссоциирует на 2 атома X . Поэтому для протекания хемосорбции необходимо затратить энергию, равную энергии диссоциации. Величина этой энергии показана на больших расстояниях от поверхности. Кривые (2) и (3) характеризуются относительно глубоким минимумом, соответствующим теплоте хемосорбции и находящемся на более близком расстоянии от твердой поверхности, чем относительно мелкий минимум на кривой физической адсорбции.
Как правило, начальной стадией хемосорбции является физическая адсорбция. При отсутствии физической адсорбции энергия активации равна высокой энергии диссоциации молекул адсорбируемого газа. Если молекула газа вначале физически адсорбируется, то она приближается к поверхности по пути с низкой затратой энергии.
60
образующейся композиции и имеют четкую границу раздела с непрерывной полимерной фазой (матрицей). Газонаполненные полимеры представляют собой пенорезины или пенопласты.
Твердые наполнители бывают зернистые, такие как технический углерод (сажа), диоксид кремния, мел; пластинчатые - тальк, слюда,
графит; волокнистые. На границе раздела фаз в наполненных полимерах большое значение имеют поверхностные явления:
смачивание, адгезия, адсорбция, полимеризация на поверхности наполнителя. При этом адсорбируется несколько молекул полимера и образуется поверхностный слой значительной толщины. Если толщина поверхностного слоя на границе раствора соли с воздухом равна 5 10 10 м, кварца с полисилоксаном - 10 8 м, то межфазные слои в полимерах имеют толщину свыше 10 7 м . В полимерах проявляется подвижность макромолекул в целом и ее отдельных участков - сегментов, т. е. полимеры имеют двойственную природу.
Вследствие этого в межфазных слоях на поверхности наполнителя следует различать сегментальный слой небольшой толщины и значительный по размерам граничный слой (рис. 1.6).
Рис. 1.6. Межфазный и переходный слой в полимерах.
!-Наполнитель, 2-сегментальный слой, 3-переходный слой, 4-полимер.
29
www.mitht.ru/e-library
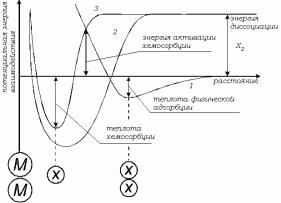
На поверхности частицы наполнителя вследствие ограничения подвижности макромолекул изменяется их конформация. Это в свою очередь влияет на близлежащие макромолекулы, расположенные в объеме матрицы. В случае кристаллического полимера небольшое количество твердых частиц (доли % по объему) изменяет кристаллическую структуру всего полимера, что указывает на сильное дальнодействие поверхности.
Наполнители, сильно повышающие прочность, называются
усиливающими. Наибольшее значение имеет усиление каучука техническим углеродом (сажей). Сажа образует в матрице каучука цепочечные и фрактальные структуры, которые способствуют ориентации молекул каучука, вследствие чего повышается прочность.
Другой причиной повышения прочности является притупление вершины разрастания трещины, повышение энергии, рассеиваемой в объеме, по линии разрыва. Поэтому происходит выравнивание напряжения при деформации.
Особый класс коллоидных систем типа полимер в полимере образуют смеси полимеров. Они имеют двухфазную структуру,
высокую устойчивость вследствие огромной вязкости и малого межфазного натяжения, развитый межфазный слой. Свойства смесей зависят от следующих коллоидно-химических параметров:
соотношения объемов дисперсной фазы и дисперсионной среды,
природы дисперсной фазы и матрицы, размера и формы частиц дисперсной фазы, интенсивности взаимодействия полимеров на границе раздела фаз.
Для двухфазных смесей каучуков характерен эффект взаимоусиления, заключающийся в увеличении динамической выносливости (N-число циклов до разрыва) (рис. 1.7).
30
Рис. 3.5. Кривые потенциальной энергии для физической адсорбции (1) и
хемосорбции при 0(2), 0,8(3)
Рассмотрим в качестве примера изменение потенциальной энергии молекулы газа X2 с изменением расстояния от поверхности металла, на которой она адсорбируется физически (кривая 1) и
химически (кривые 2 и 3) при разной степени заполнения поверхности адсорбента .
При сближении молекулы с поверхностью, потенциальная энергия уменьшается вследствие действия Ван-дер-Ваальсовых сил притяжения. По положению минимума на кривой можно определить минимальное расстояние от поверхности, а по величине этого минимума – теплоту физической адсорбции. При дальнейшем уменьшении расстояния потенциальная энергия увеличивается вследствие проявления сил отталкивания (борновских сил). При хемосорбции молекула предварительно диссоциирует на атомы X .
Положение минимумов на кривых 2 и 3 соответствует оптимальному расстоянию адсорбированных атомов от поверхности, а
величины этих минимумов – теплоте хемосорбции. Как видно, при хемосорбции молекула ближе подходит к поверхности, чем при
59
www.mitht.ru/e-library
