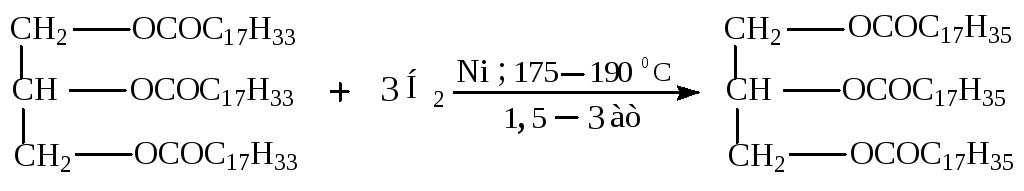- •2.2. Функциональные производные углеводородов. Галогенпроизводные углеводородов
- •Строение и номенклатура
- •Химические свойства
- •Особенности реакций ароматических галогенопроизводных с галогеном в ароматическом ядре
- •II. Реакции отщепления.
- •Физические свойства галогенопроизводных, их применение
- •Способы получения галогенопроизводных
- •Задания для выполнения кр № 2 по теме «функциональные производные углеводородов. Галогенопроизводные углеводородов» Галогенпроизводные углеводородов
- •2.3. Функциональные производные углеводородов. Кислородсодержащие производные углеводородов
- •2.3.1.Спирты
- •Химические свойства одноатомных спиртов
- •Способы получения одноатомных спиртов
- •Особенности многоатомных спиртов
- •Химические свойства
- •Физические и пожароопасные свойства многоатомных спиртов, их применение
- •Способы получения
- •Строение фенола
- •Химические свойства
- •Физические свойства и применение
- •Способы получения
- •Простые эфиры
- •Химические свойства
- •Физические и пожароопасные свойства простых эфиров
- •Способы получения простых эфиров
- •2.3.2. Альдегиды и кетоны
- •Номенклатура альдегидов и кетонов
- •Химические свойства
- •Физические и пожароопасные свойства альдегидов и кетонов, их применение
- •Способы получения альдегидов и кетонов
- •2.3.3. Карбоновые кислоты
- •Физические свойства.
- •Химические свойства
- •Особенности ненасыщенных карбоновых кислот.
- •Важнейшие представители карбоновых кислот и их производных.
Особенности ненасыщенных карбоновых кислот.
Непредельные карбоновые кислоты содержат кратные углерод-углеродные связи.
Примеры ненасыщенных карбоновых кислот:
СН2=СН-СООН акриловая кислота; пропеновая кислота
СН2=С(СН3)-СООН метакриловая кислота; метилпропеновая кислота
СН3-(СН2)7-СН=СН(СН2)7-СООН олеиновая кислота
СН3-(СН2)4-СН=СН-СН2-СН=СН-(СН2)7-СООН линолевая кислота
Для этих кислот характерны реакции предельных (насыщенных) карбоновых кислот по карбоксильной группе, а также реакции по кратным связям (реакции присоединения и полимеризации).
Непредельные карбоновые кислоты являются более сильными кислотами , чем соответствующие предельные карбоновые кислоты.
Способы получения одноосновных карбоновых кислот
Реакции окисления.
Конечным продуктом окисления многих органических соединений являются карбоновые кислоты. Для окисления используют как кислород (воздух) в присутствии катализаторов (соли Со, Mn), так и другие неорганические (H2O2, CrO3, KMnO4, HNO3) и органические окислители.
Реакции гидролиза.
Примеры:
CH3CH2СCl3 + 3H2O CH3CH2COOH + 3HCl
CH3C N + 2H2O CH3COOH + NH3
Нитрил
Оксосинтез.

Важнейшие представители карбоновых кислот и их производных.
Муравьиная кислота. Это бесцветная едкая жидкость с острым запахом, смешивающаяся с водой. Впервые выделена из красных муравьев. В природе встречается также в крапиве.
Синтез муравьиной кислоты:

Уксусная кислота – бесцветная жидкость с острым запахом и кислым вкусом, неограниченно смешивается с водой. Безводную уксусную кислоту называют «ледяной», так как при 160С она замерзает и образует кристаллы, подобные льду.
Разбавленные водные растворы уксусной кислоты образуются при брожении вина. При перегонке водных растворов получаютс приблизительно 80%-ную кислоту, которую применяют для пищевых целей. Синтетическую уксусную кислоту получают различными методами: окислением этилового спирта специальными бактериями уксуснокислого брожения, из этилена, ацетилена.
Уксусную кислоту используют в качестве растворителя и как исходное вещество для синтеза производных уксусной кислоты. Соли уксусной кислоты применяют в текстильной промышленности в качестве протравителей. Уксусная кислота применяется в пищевой промышленности, в производстве искусственных волокон, пластических масс, лекарственных веществ и душистых веществ.
Уксусная кислота самовозгорается при контакте с хромовым ангидридом, перекисью натрия и другими сильными окислителями.
Этилацетат – жидкость с приятным ароматным запахом, плохо растворяется в воде. С воздухом этилацетат образует взрывчатые смеси. Концентрационные пределы воспламенения: НПВ – 3,55%, ВПВ – 16,8%. Эфир самовозгорается в контакте с хромовым ангидридом CrO3, с перекисью натрия Na2O2 в присутствии воды, с перманганатом калия KMnO4, хлоратом калия KClO3 в присутствии серной кислоты. На воздухе горит светящимся пламенем с выделением значительного количества тепла.
При нагревании этилацетата с водой в присутствии минеральной кислоты или щелочи происходит гидролиз эфира:
СН3СООС2Н5 + Н2О СН3СООН + С2Н5ОН
Акриловая кислота - бесцветная жидкость с острым запахом, хорошо растворима в воде. Она легко полимеризуется, поэтому ее используют в промышленности полимерных материалов.
Метакриловая кислота - бесцветная жидкость, легко полимеризуется. В промышленности полимеров используют ее метиловый эфир.
Жиры. Жиры – это сложные эфиры трехатомного спирта глицерина и высших карбоновых кислот.
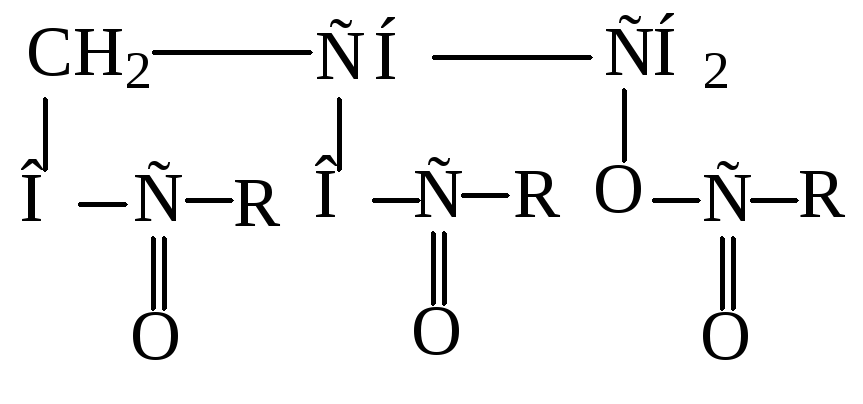
Жиры бывают животного и растительного происхождения. Если в составе эфира глицерина насыщенные кислоты, это твердые жиры (сливочное масло, животный жир). Если же в составе эфира ненасыщенные жирные кислоты, это растительные масла (подсолнечное, оливковое, льняное и др.). Все жиры нерастворимы в воде, легче воды. Жиры растворяются во многих органических растворителях (бензине, четыреххлористом углероде, серном эфире и др.). Все жиры являются горючими веществами. Масла и некоторые животные жиры склонны к самовозгоранию при определенных условиях. Для оценки способности масел к самовозгоранию необходимо знать количество ненасыщенных связей, что оценивают по величине иодного числа. Чем больше иодное число, тем больше в масле ненасыщенных связей, следовательно это масло более склонно к самовозгоранию. Практика показывает, к самовозгоранию способны масла с иодным числом более 50.
Омыление жиров.
При нагревании с водным раствором щелочи жиры гидролизуются

Гидрирование растительного масла.
Пример: