
- •Оптика и квантовая физика
- •Лабораторный практикум для студентов специальности 010100 (010101.65) - Математика
- •Определение показателя преломления жидкостей при помощи рефрактометра аббе
- •Описание прибора
- •Измерения
- •Контрольные вопросы
- •Определение радиуса кривизны линзы и длины световой волны с помощью колец ньютона
- •Краткие теоретические сведения
- •Описание прибора
- •Измерения и вычисления
- •Контрольные вопросы
- •Изучение поляризованного света
- •Естественный и поляризованный свет
- •Методы получения линейно-поляризованного света
- •Способы получения плоскополяризованного света
- •Описание установки
- •Измерения
- •Контрольные вопросы
- •Изучение линейчатых спектров испускания при помощи спектроскопа
- •Теория метода и описание установки
- •Описание ртутной лампы
- •Длины волн некоторых линий спектра ртути
- •Длины волн некоторых линий в спектре неона
- •Контрольные вопросы
- •Изучение явления внешнего фотоэффекта
- •Теоретическая часть
- •Приборы и оборудование
- •Порядок выполнения работы
- •Контрольные вопросы
- •Соотношение неопределенностей для фотонов
- •Теоретическая часть
- •Измерения
- •Контрольные вопросы
- •Исследование температурной зависимости металлов и полупроводников
- •Содержание работы
- •Приборы и оборудование
- •Порядок выполнения работы
- •Обработка результатов измерений
- •Контрольные вопросы
- •Изучение закона радиоактивного распада
- •Введение
- •Измерения
- •Контрольные вопросы
Контрольные вопросы
1. Объяснить с точки зрения зонной теории различное поведение электропроводности металлов и полупроводников при изменениях температуры.
2. Что такое температурный коэффициент сопротивления металла.
Лабораторная работа № 8
Изучение закона радиоактивного распада
Цель работы: ознакомление с основными закономерностями радиоактивного распада.
Приборы и принадлежности: счетчик β - излучения УИМ 2-1е, пылесос, ватно-марлевый фильтр, секундомер.
Введение
Естественная радиоактивность представляет собой процесс самопроизвольного превращения атомных ядер, сопровождающийся испусканием различных частиц и лучей. γ-лучи не являются видом радиоактивности и, обычно, сопровождаются α- и β- распадами. Испуская γ-фотоны, возбужденное ядро переходит в основное состояние.
П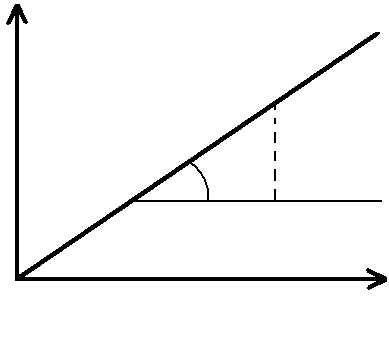 ри
α- распаде ядро лишается группы из
четырех нуклонов и его массовое число
уменьшается на четыре единицы, а заряд
ядра уменьшается на две единицы. При
естественно β- радиоактивности массовое
число остается постоянным, заряд
увеличивается на единицу. Как α- так и
β- распад описываются одним и тем же
статистическим законом, носящим названиезакон
радиоактивного распада.
ри
α- распаде ядро лишается группы из
четырех нуклонов и его массовое число
уменьшается на четыре единицы, а заряд
ядра уменьшается на две единицы. При
естественно β- радиоактивности массовое
число остается постоянным, заряд
увеличивается на единицу. Как α- так и
β- распад описываются одним и тем же
статистическим законом, носящим названиезакон
радиоактивного распада.
К
Рис.
8.1
dN = -Ndt (8.1)
Знак “-” появляется в связи с тем, что количество не распавшихся ядер уменьшается в процессе распада. Постоянная распада представляет собой относительную убыль числа ядер в единицу времени. Интегрируя (8.1) с учетом начальных условий N = N0 при t = 0, получим закон радиоактивного распада в интегральной форме:
![]() , (8.2)
, (8.2)
где
N0-количество
не распавшихся ядер (атомов) в начальный
момент времени t.
Зависимость (8.2) удобно изображать в
полулогарифмических координатах,
откладывая по оси абсцисс время, а по
оси ординат
![]() .
По такому графику легко определить
постоянную распада
как тангенс угла наклона (Рис.8.1).
.
По такому графику легко определить
постоянную распада
как тангенс угла наклона (Рис.8.1).
Значение постоянных распада для различных радиоактивных изотопов изменяется в очень широких пределах. Опытная проверка законов радиоактивного распада должна состоять в изучении зависимости числа наличных ядер от времени. Зависимость можно установить, наблюдая за изменением активности препарата во времени.
Активностью препарата «n» называется число распадов в единицу времени:
![]() (8.3)
(8.3)
Дифференцирование уравнения (8.2) приводит к следующему выражению для активности:
![]() , (8.4)
, (8.4)
где
n0
= N0
– начальная
активность. Таким образом, действительно,
часть распада в единицу времени
пропорциональна интересующей нас
величине N
(числу наличных радиоактивных ядер), а
в каждом акте распада рождается одна
частица. Измеряя число частиц, испускаемых
препаратом в единицу времени, можно
получить требуемую зависимость. -
радиоактивный препарат легко изготовить,
воспользовавшись естественной
радиоактивностью воздуха. Дело в том,
что в атмосферном воздухе всегда
содержится радиоактивный газ радон и
продукты его распада: радиоактивные
изотопы висмута, свинца и полония.
Пропустив значительный объем воздуха
через пористый (ватный) фильтр,
задерживающий радиоактивный аэрозоль,
можно получить препарат, обладающий
значительной радиоактивностью. Активность
фильтра зависит от изотопов
![]() и
и![]() .
Периоды радиоактивных изотопов полония
.
Периоды радиоактивных изотопов полония![]() ,
свинца
,
свинца![]() и
висмута
и
висмута![]() соответственно равны~
3,05 мин., 26,8 мин. и 19,7 мин. Периоды последних
двух радиоактивных изотопов таковы,
что время, отводимое на выполнение
лабораторной работы достаточно для
исследования закона радиоактивного
распада и установления его основных
характеристик: постоянной распада
и периода полураспада Т. Зависимость
(8.4) для активности радиоактивного
препарата, так же как и зависимость
(8.2), выражающая изменение числа наличных
радиоактивных ядер со временем, в
полулогарифмических координатах
изображается прямой линией, тангенс
угла наклона которой будет равен
постоянной распада.
соответственно равны~
3,05 мин., 26,8 мин. и 19,7 мин. Периоды последних
двух радиоактивных изотопов таковы,
что время, отводимое на выполнение
лабораторной работы достаточно для
исследования закона радиоактивного
распада и установления его основных
характеристик: постоянной распада
и периода полураспада Т. Зависимость
(8.4) для активности радиоактивного
препарата, так же как и зависимость
(8.2), выражающая изменение числа наличных
радиоактивных ядер со временем, в
полулогарифмических координатах
изображается прямой линией, тангенс
угла наклона которой будет равен
постоянной распада.
Однако
если активность препарата убывает не
по экспоненциальному закону, то препарат
содержит несколько радиоактивных
компонентов, каждый из которых в
наблюдаемый промежуток времени вносит
определенный вклад. Пусть, например, в
момент времени t=0
препарат содержит
![]() ядер радиоактивных элементов А, В и С,
превращающиеся в стабильные ядра с
постоянными распада1,
2,
3.
Число ядер каждого элемента в произвольный
момент времени будет равно:
ядер радиоактивных элементов А, В и С,
превращающиеся в стабильные ядра с
постоянными распада1,
2,
3.
Число ядер каждого элемента в произвольный
момент времени будет равно:

тогда регистрируемая на опыте активность препарата:
![]()
График такой зависимости в полулогарифмических координатах ln n = f(t) будет, вообще говоря, криволинейным. Но при определенных условиях активность препарата может обусловливаться только активностью одного радиоактивного изотопа, тогда зависимость ln n = f(t) будет приблизительно прямолинейной.
