
- •Тема 1. Введение………………………………………………………………….4
- •Тема 1. Введение.
- •Тема 2. Физические основы горения.
- •2.1. Свойства газов.
- •2.2. Свойства газовых смесей.
- •3. Парциальные давление и объем.
- •2.3. Свойства жидкостей.
- •2.4. Свойства сжиженных газов.
- •2.5. Свойства твердых веществ.
- •Тема 3. Химические основы горения.
- •3.1. Химизм реакций горения.
- •3.2.Теплосодержание веществ.
- •3.3. Тепловой эффект реакции.
- •3.4. Кинетические основы газовых реакций.
- •3.5. Энергия активации реакции.
- •3.6. Катализ.
- •3.7. Адсорбция.
- •Тема 4. Виды горения.
- •4.1. Горение газообразных, жидких и твердых веществ.
- •4.2. Гомогенное и гетерогенное горение.
- •4.3. Диффузионное и кинетическое горение.
- •4.4. Нормальное горение.
- •4.5. Дефлаграционное (взрывное) горение.
- •4.6. Детонационное горение.
- •Тема 5. Показатели пожаровзрывоопасности веществ.
- •5.1. Общие показатели для горючих веществ и видов горения.
- •5.2. Показатели взрывопожароопасности газо-, паро- и пылевоздушных смесей.
- •5.3. Показатели пожароопасности твердых компактных и пыле- видных веществ.
- •Тема 6. Возникновение горения.
- •6.1. Тепловое самовоспламенение (тепловой взрыв).
- •6.2. Самовозгорание.
- •6.3. Цепное самовоспламенение (цепной взрыв).
- •6.4. Зажигание.
- •Тема 7. Распространение пламени.
- •7.1. Тепловая теория горения.
- •7.2. Горение в замкнутом объеме.
- •7.3. Движение газов при горении.
- •7.4. Факторы ускорения горения.
- •7.5. Условия возникновения взрыва.
- •Тема 8. Ударные волны и детонация.
- •8.1. Ударные волны в инертном газе.
- •8.2. Воспламенение при быстром сжатии.
- •8.3. Возникновение детонации.
- •8.4. Стационарный режим распространения детонации.
- •8.5. Определение скорости детонации.
- •8.6. Вырождение детонации.
- •Тема 9. Погасание пламени (прекращение горения).
- •9.1. Концентрационные пределы распространения пламени.
- •9.2.Общие закономерности для пределов распространения пламени.
- •9.3. Затухание пламени в узких каналах.
- •9.5. Закономерности для точки флегматизации.
- •9.6. Механизм флегматизации взрывоопасных смесей.
6.1. Тепловое самовоспламенение (тепловой взрыв).
Самовоспламенение – это явление резкого увеличения скорости экзо-термических реакций, приводящее к самопроизвольному возникновению го-рения вещества в отсутствии источника зажигания.
Теория теплового самовоспламенения разработана академиком Семе-новым Н.Н., который исходил из представления об ускорении реакций окис-ления с температурой и преобладания скорости тепловыделения над тепло-отводом.
При окислительной реакции, проходящей с полной отдачей образую-щегося тепла, горение не возникает. Горение возникает лишь в условиях рез-кого самоускорения химического процесса, связанного с накоплением либо тепла в системе (так называемое тепловое самовоспламенение), либо катали-зирующих промежуточных продуктов реакции (цепное самовоспламенение). Суть теории заключается в следующем. Рассмотрим поведение горючей сме-си, заключенной в сосуд объемом V с постоянной температурой стенок Т0. В смеси протекает химическая реакция. Температура во всех точках сосуда одинакова и равна Т.
Исходя из физико-химических свойств газов, рассмотренных нами Ра-нее, скорость химической реакций υр подчиняется соотношению
![]() (6.1)
(6.1)
где: К – константа скорости реакций, зависящая от температуры;
с – концентрация реагирующих веществ;
n – порядок реакции;
Е – энергия активации реакции.
Скорость выделения тепла при реакции:
![]() ,
(6.2)
,
(6.2)
где: Q – тепловой эффект реакции;
V – объем сосуда;
τ – время.
Видно, что с повышением температуры скорость выделения тепла рас-тет по экспоненте.
Выделившееся тепло расходуется на нагрев смеси и потери в окру-жающую среду за счет теплопроводности и излучения.
Количество тепла, отводимое от поверхности сосуда в единицу времени выражается линейною зависимостью:
![]() (6.3)
(6.3)
где: α – коэффициент теплоотдачи;
S – площадь поверхности стенок сосуда.
Тогда изменение подвода и отвода тепла в зависимости от температуры можно проиллюстрировать следующим образом (рис. 22):

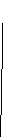
![]()
q2’’
q2’
q2’’’
q1
Р
q2
 ис.
22. Соотношение теп-ловыделения и
теплоотво-да при тепловом взрыве.
ис.
22. Соотношение теп-ловыделения и
теплоотво-да при тепловом взрыве.
а'
T
То Т1
То' Тк
То" Тсв
Т2
Три линии q2 соответствуют трем значениям начальной температуры смеси То, Тк и То’.
Решающим условием возникновения процесса горения является пре-вышение или равенство скорости выделения тепла реакции над скоростью отдачи тепла реагирующей системой в окружающую среду, например, стен-кам реакционного сосуда.
При установившимся состоянии системы q1=q2 и температура в сосуде определяется как абсцисса точек пересечения линии q1 с линиями q2. Из ри-сунка видно, что линии прихода и отвода могут пересекаться в двух точках (точки a и b) либо в одной точке (точка с), либо не пересекаться.
Рассмотрим первый случай: нагрев смеси, имеющей начальную темпе-ратуру То. При T=Tо скорость теплоотвода по условиям равна нулю и хотя q1 невелико, реагирующий газ начинает нагреваться. С повышением температу-ры и q1 и q2 возрастают. Пока температура газа лежит в интервале между Т0 и Т1 он продолжает нагреваться. При достижении Т1 величины q1 и q2 сравни-ваются и температура газа становится постоянной. Состояние системы в этой точке является устойчивым. Если в результате случайных причин температу-ра газа превысит Т1 то теплоотвод скажется больше тепловыделения и систе-ма сама вернется в прежнее состояние. Если мы искусственно охладим газ, то он нагреется сам за счет реакции до T1. Режим медленной реакции, протее-кающий с практически постоянной скоростью при Т=T1 сохраняется дли-тельное время.
Вторая точка пересечения кривых (b) находится в области больших вы-соких температур, и режим тепловой реакции в этом случае будет неустой-чивым. При отклонении от равновесного состояния в точке b система в него уже не возвращается.
Повышение начальной температуры стенок сосуда То до То' приводит к смещению вправо линии теплоотвода q2. Значение стационарной температу-ры Т1 будет при этом плавно расти (точка а'), и при температуре стенки Тк линии подвода и отвода тепла будут касаться одна другой в точке С, которая является граничной точкой существования стационарного режима, неболь-шое повышение температуры стенки выше Тк будет сопровождаться превы-шением теплоприхода над теплоотводом, что вызовет повышение температу-ры смеси и соответственно, резкое ускорение реакции.
Этот процесс перехода от медленно протекающей реакций к прогрес-сивно ускоряющемуся возгоранию смеси, является процессом самовоспламе-нения. А температура, откладываемая на оси абсцисс от точки С – темпера-тура самовоспламенения Тсв.
Минимальную температуру стенок сосуда Тк, при которой смещение достигнет равенства q1 = q2” – называют критической температурой воспла-менения.
При повышении температуры сосуда до То" условия тепловыделения по-прежнему описываются кривой q1, тогда как прямая теплоотвода q2''' пере- местится вправо параллельно самой себе. При температуре То" сосуда тепло-приход больше теплоотвода при любой температуре газа, и температура газа, а с нею и скорость реакции, будут прогрессивно расти.
Температура сосуда, для которой прямая теплоотвода q2” касательна к кривой тепловыделения, является предельной для перехода от режима мед-ленной реакции к взрыву. При Tо>Tк скорость реакции и температура газа неограниченно увеличиваются и происходит тепловой взрыв. При Tо< Tк ус-танавливается стационарный режим, при котором скорость реакции мала.
Время, в течение которого в реагирующей системе достигается разо-грев от Ткр до Тсв, называется периодом индукции самовоспламенения.
Теория теплового самовоспламенения хорошо объясняет зависимость между давлением и температурой самовоспламенения горючей смеси. До-пустим, что сосуд, в который вводится смесь, имеет постоянную температуру То. При малых давлениях количество выделяющегося тепла не превышает количества отводимого тепла, и реакция протекает при постоянной темпера-туре, близкой к температуре сосуда.
При
увеличении давления и соответственно,
массы вещества выделяет-ся больше тепла,
чем отводится, температура газов
повышается и происходит их самовоспламенение.
Наглядно зависимость теплоприхода и
теплоотвода
![]() (где τ – время), от температуры при
различных давлениях показана на рис
(где τ – время), от температуры при
различных давлениях показана на рис унке
23:
унке
23:
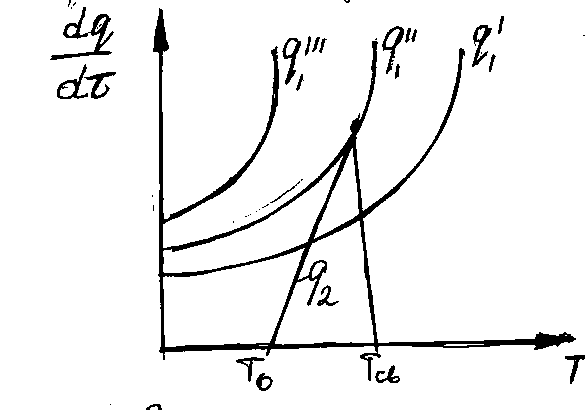
Рис. 23. Соотношение теплопри- хода и теплоотвода при различном давлении газовой смеси: q1' < q1"< q1'''
Тут
![]()
![]()
![]() показывают тепловыделение при давлениях
соответствен-но Р1<Р2<Р3
при
одинаковом составе смеси. Количество
отводимого от зоны горения тепла
характеризуется прямой q2
. Критические
условия самовоспла-менения реализуются
при давлении Р2
(кривая
показывают тепловыделение при давлениях
соответствен-но Р1<Р2<Р3
при
одинаковом составе смеси. Количество
отводимого от зоны горения тепла
характеризуется прямой q2
. Критические
условия самовоспла-менения реализуются
при давлении Р2
(кривая
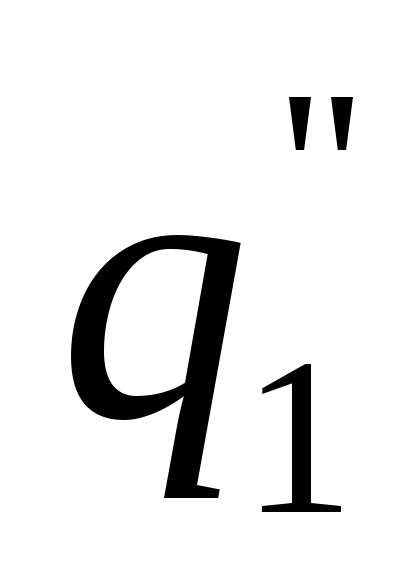 ).
).
Условия
самовоспламенения предельного состава
горючей смеси пока-зана на кривых
![]() и
и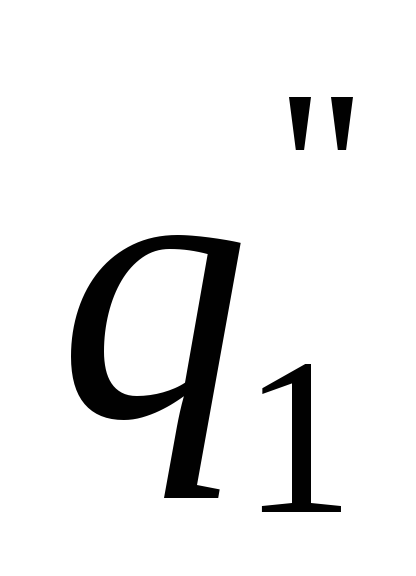 .
В общем, условие теплового самовоспламенения
сво-дится к тому, что начальный саморазогрев
горючей смеси в результате реак-ции
окисления должен превысить некоторое
критическое значение
.
В общем, условие теплового самовоспламенения
сво-дится к тому, что начальный саморазогрев
горючей смеси в результате реак-ции
окисления должен превысить некоторое
критическое значение![]() ,
называемое характеристическим интервалом
температуры. Вывод этого по-казателя
изложен в § 9.3.
,
называемое характеристическим интервалом
температуры. Вывод этого по-казателя
изложен в § 9.3.
Зависимость температуры самовоспламенения от состава горючей сме-си показана на рисунке 24. Минимальная Тсв характерна для стехиометриче-ских смесей.

Рис. 24. Область самовоспламе-нения горючих смесей.
