
- •Билеты по химии
- •11.Классификация химических реакций в неорганической химии
- •14.Обратимость химических реакций
- •15. Электролитическая диссоциация
- •Вопрос 17: Обратимые и необратимые химические реакции.
- •Вопрос 18: Реакции ионного обмена______________________
- •Вопрос 19: Сущность окислительно-восстановительных реакций.
- •Вопрос 20: Составление окислительно-восстановительных реакций методом электронного___________.
- •Вопрос 21: Гидролиз солей.
- •Вопрос 22:
- •Неорганические вещества, содержащие углерод:
- •Вопрос 25:
- •Вопрос 28: Металлы, их положение в периодической системе химических элементов д.И. Менделеева, строение их атомов, металлические связи. Общие химические свойства металлов.
- •I. Реакции с неметаллами
- •II. Реакции с кислотами
- •III. Взаимодействие с водой
- •Вопрос 29: Кислород. Физические свойства, распространение кислорода в природе. Физиологическое значение кислорода. Его роль в жизни и применение.
- •31) Классификация органических соединений.
- •32) Основные положения теории химического строения а.М.Бутлерова. Химическое строение как порядок соединения и взаимного влияния атомов в молекулах. Основные направления развития данной теории.
- •33) Изомерия органических соединений, ее виды.
- •34) Предельные углеводороды. Гомологический ряд, химические свойства алканов.
- •35) Применение и способы получения алканов.
- •36) Механизм реакции замещения на примере предельных углеводородов. Практическое значение предельных углеводородов.
- •37) Нефть, ее свойства и состав. Продукты фракционной перегонки нефти. Охрана окружающей среды при нефтепереработке и транспортировке нефтепродуктов.
- •38) Циклопарафины, их химическое состояние, свойства, нахождение в природе, практическое значение.
- •39) Непредельные углеводороды ряда этилена, общая формула и химические свойства. Применение этиленовых углеводородов в медицине.
- •40) Механизм реакции присоединения на примере непредельных углеводородов ряда этилена. Правило Марковникова. Применение этиленовых углеводородов в органическом синтезе.
- •Вопрос 41
- •Вопрос 42
- •Вопрос 43
- •Вопрос 44
- •Вопрос 46
- •Вопрос 48
- •Лабораторные методы получения альдегидов Окислительные методы
- •Восстановительные методы
- •Синтез ароматических альдегидов
- •Вопрос 49
Вопрос 48
Альдеги́ды (от лат.alcohol dehydrogenatus — спирт, лишённый
водорода) — класс органических
соединений, содержащих альдегидную
группу (–CHO)[1].
ИЮПАК определяет альдегиды как вещества
вида RCHO, в которых карбонильная
группа связана
с одним атомом водорода и одной группой
R[2].

CH2O- муравьиный альдегид, С2Н4О-уксусный альдегид, С3Н6О-пропионовый альдегид, C4H8O-маслянистый альдегид, C5H10O-валерьяновый альдегид.

Лабораторные методы получения альдегидов Окислительные методы
Для получения альдегидов в лабораторных условиях часто используется реакция окисления первичных спиртов реагентами
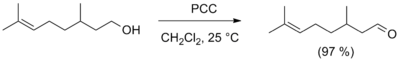
Как
метод получения альдегидов может
использоваться восстановительный озонолиз симметричных
дизамещённых алкенов либо
циклических алкенов (в данном случае
реакция приводит в образованию
диальдегида) ![]()
Также к данному типу реакций относится окисление вицинальных диолов йодной кислотой или тетраацетатом свинца[12].

Важным методом также является гидроборирование — окисление алкинов, в ходе которого к алкину против правила Марковникова присоединяется диалкилборан (например, дисиамилборан), а полученный продукт окисляется щелочным раствором пероксида водорода, что приводит к образованию альдегида[13].
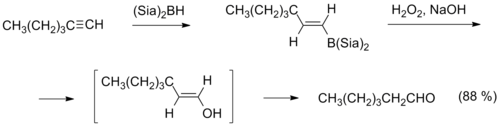
Восстановительные методы
в реакции Розенмунда хлорангидриды восстанавливают под действием водорода на палладиевом катализаторе. Аналогичное превращение можно провести под действием три(трет-бутокси)алюмогидрида лития[15].

Сложные эфиры селективно восстанавливаются до альдегидов под действием диизобутилалюминийгидрида[
Синтез ароматических альдегидов
Альдегидную
группу можно ввести в ароматические
соединения реакциями Гаттермана, Гаттермана
— Коха, Вильсмейера
— Хаака, Рихе и Раймера
— Тимана. 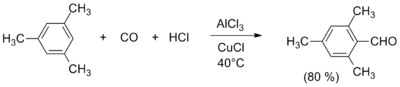
![]()
Также ароматические альдегиды могут быть получены окислением метилзамещённых бензолов под действием ряда окислителей, в том числе, оксида хрома(VI) CrO3, оксида марганца(IV) MnO2 и нитрата церия — аммония[en][18].
Реакция Соммле позволяет окислять бензилгалогениды ArCH2X под действием уротропина с последующим гидролизом образующейся соли до альдегида. Данная реакция применима для синтеза разнообразных ароматических и гетероциклических альдегидов. Подобное превращение можно осуществить, также окисляя бензилгалогениды солями 2-нитропропана[18].

Ароматические альдегиды можно получать из производных ароматических карбоновых кислот общими методами, однако существуют и специфические реакции. Например, реакция Стефена позволяет восстанавливать ароматические нитрилыхлоридом олова(II) SnCl2 с последующим гидролизом, что приводит к ароматическому альдегиду[18].
Вопрос 49
К
одноосновным предельным карбоновым
кислотам относятся органические
вещества, в молекулах которых имеется
одна карбоксильная группа, связанная
с радикалом предельного углеводорода
или с атомом водорода.
Муравьиная кислота, уксусная кислота, Масляная кислота, Валериановая кислота. Капроновая, каприловая и каприновая кислоты, Энантовая кислота, Пеларгоновая кислота, Лауриновая кислота.
Уксусная кислота обладает всеми свойствами карбоновых кислот. Связь между водородом и кислородом карбоксильной группы (−COOH) карбоновой кислоты является сильно полярной, вследствие чего эти соединения способны легко диссоциировать и проявляют кислотные свойства.

В результате диссоциации уксусной кислоты образуется ацетат-ион CH3COO− и протон H+. Уксусная кислота является слабой одноосновной кислотой со значением pKa в водном растворе равным 4,75. Раствор с концентрацией 1.0 M (приблизительная концентрация пищевого уксуса) имеет pH 2,4, что соответствует степени диссоциации 0,4 %.
На слабой диссоциации
уксусной кислоты в водном растворе
основана качественная
реакция на
наличие солей уксусной кислоты: к
раствору добавляется сильная кислота
(например, серная),
если появляется запах уксусной кислоты,
значит, соль уксусной кислоты в растворе
присутствует (кислотные остатки уксусной
кислоты, образовавшиеся из соли, связались
с катионами водорода от сильной кислоты
и получилось большое количество молекул
уксусной кислоты)[13].
Исследования показывают, что в кристаллическом состоянии молекулы образуют димеры, связанные водородными связями.[14]
Уксусная кислота способна взаимодействовать с активными металлами. При этом выделяется водород и образуются соли —ацетаты.
Mg(тв) + 2CH3COOH → (CH3COO)2Mg + H2
Уксусная кислота может хлорироваться действием газообразного хлора. При этом образуется хлоруксусная кислота.
CH3COOH + Cl2 → CH2ClCOOH + HCl

Этим путем могут быть получены также дихлоруксусная (CHCl2COOH) и трихлоруксусная (CCl3COOH) кислоты.
Уксусная кислота вступает во все реакции, характерные для карбоновых кислот. Она может быть восстановлена доэтанола действием алюмогидрида лития. Уксусная кислота также может быть превращена в хлорангидрид действием тионилхлорида. Натриевая соль уксусной кислоты декарбоксилируется при нагревании со щелочью, что приводит к образованию метана.
Карбоновые кислоты - исходные соединения для получения промежуточных продуктов органического синтеза, в частности кетенов, галогенангидридов, виниловых эфиров, галогенкислот. Соли карбоновых кислот и щелочных металлов применяют как мыла, эмульгаторы, смазочные масла; соли тяжелых металлов - сиккативы, инсектициды и фунгициды, катализаторы. Эфиры кислот - пищевые добавки, растворители; моно- и диэфиры гликолей и полигликолей пластификаторы, компоненты лаков и алкидных смол; эфиры целлюлозы - компоненты лаков и пластмассы. Амиды кислот - эмульгаторы и флотоагенты.
Муравьиная кислота является сильным восстановителем и обладает сильным бактерицидным эффектом. На этих свойствах основано ее применение в медицине (используется муравьиный спирт - 1,25% спиртовой раствор муравьиной кислоты), как консерванта (при силосировании зелёной массы и фруктовых соков) и для дезинфекции. Также применяется для обработки кожи и отделке текстиля и бумаги. Широко используются эфиры муравьной кислоты - метилформиат, этилформиат и изоамилформиат.[11]
Уксусная кислота – в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров). В домашнем хозяйстве как вкусовое и консервирующее вещество. В промышленности - растворитель лаков, коагулянт латекса, ацетилирующий агент[12].
Масляная кислота – для получения ароматизирующих добавок (эфиры метилбутират и изоамилбутират - ароматизаторы в промышленности), пластификаторов и флотореагентов, как экстрагент щелочно-земельных металлов.[13]
Щавелевая кислота – в металлургической промышленности (удаление окалины), в качестве протравы при крашении, для отбелки соломы, при приготовлении чернил, как реагент в аналитической органической химии[14].
Стеариновая C17H35COOH и пальмитиновая кислота C15H31COOH – в качестве поверхностно-активных веществ (натриевая соль), смазочных материалов в металлообработке, как компонент и эмульгатор кремов и мазей. Эфиры - антиоксиданты и стабилизаторы пищевых продуктов, компоненты клеящих паст и для обработки текстиля и кожи.[15]
Олеиновая кислота C17H33COOH – флотореагент при обогащении руд цветных металлов.
51)Сложные
эфиры - класс органических соединений,
представляющих собой производные
неорганических или органических кислот,
в которых гидроксильная группа заменена
на алкоксильную группу.![]()
Взаимодействие карбоновых кислот со спиртами (реакция этерификации) сложных эфиров:

Применяются как растворители, благодаря приятному запаху применяются в пищевой и парфюмер косметической промышленности. В природе выполняют несколько ролей:
1)Строительная- жиры входят в состав клеточной мембраны.
2)Энергетическая – в ходе расщепления жиров происходит высвобождение энергии.
3)Запасающая- жиры запасают энергию.
52) В зависимости от числа углеводородных радикалов, связанных с атомом азота, различают первичные, вторичные и третичные амины, а также четвертичные аммониевые соли.
RNH2 RR/NH RR/R//N RR/R// R///N+X-
Первичныеамины
вторичные амины третичныеамины
четвертичные аммониевые соли
Пример:
Химические свойства аминов. Отличительная способность аминов – присоединять нейтральные молекулыс образованием органоаммониевых солей, подобных аммонийным солям в неорганической химии.
Растворяясь в воде, амины по такой же схеме захватывают протон, в результате в растворе появляются ионы ОН–, что соответствует образованию щелочной среды, ее можно обнаружить с помощью обычных индикаторов.
Получение аминов. В промышленности алифатические амины получают каталитическим взаимодействием спиртов с NH3 при 300–500° С и давлении 1–20 МПа, в результате получают смесь первичных, вторичных и третичных аминов
Применение аминов.
Амины
широко применяются для получения
лекарств, полимерных материалов. Анилин
— важнейшее соединение данного класса,
которое используют для производства
анилиновых красителей, лекарств
(сульфаниламидных препаратов), полимерных
материалов. ![]()
53)
Он находит широкое применение
в качестве полупродукта в производстве
красителей, взрывчатых веществ и
лекарственных средств.Анилин представляет
собой бесцветную маслянистую жидкость
с характерным запахом . На воздухе быстро
окисляется и приобретает красно-бурую
окраску. Ядовит.
Основной способ получения анилина — восстановление нитробензола. В промышленных условиях восстановление проводят водородом при 250-350 °С на никелевом или медном катализаторе.
В лаборатории для этой цели используют цинк в кислой среде:
С6Н5NО2 + 3Zn + 7HCl → C6H5NH3Cl + 3ZnCl2 + 2Н2О
или алюминий в щелочной среде:
C6H5NO2 + 2Al + 2NaOH + 4Н2О → C6H5NH2 + 2Na[Al(OH)4].
54) Аминокислоты - это органические кислоты, у которых атом водорода -углеродного атома замещен на аминогруппу - NH2. Следовательно, по химической природе это -аминокислоты с общей формулой: Из этой формулы видно, что в состав всех аминокислот входят следующие общие группировки: - CH2, - NH2, - COOH. Боковые же цепи (радикалы - R ) аминокислот различаются.


Химические свойства:
Взаимодействие с основаниями:
H2N – CH2 – COOH + NaOH → H2N – CH2 - COONa + H2O
Взаимодействие с кислотами:
H2N – CH2 – COOH + HCI → [H3N+ - CH2 – COOH]CI-
Образование внутренних солей – биполярных ионов:
H2N – CH2 – COOH ⇄ H3N+ — CH2 – COO-
Взаимодействие с формальдегидом с образованием метиленаминокислот:
CH3 – CH(NH2) – COOH + CН2О → CH3 – CH(N=CH2) – COOH + H2O
5. Реакция со спиртами:
СН3 – СН(NH2) – СООН + С2Н5ОН ↔ СН3 – СН(NH2) – СООС2Н5 + Н2O
6. Взаимодействие с азотистой кислотой:
СН3 – СН(NH2) – СООН + HONO → CH3 – CH2OH + N2↑ + H2O + CO2↑
7. Гомополиконденсация. Так из ε-аминокапроновой кислоты получают полимер – капрон:
nH2N – (CH2)5 – COOH → [-HN – (CH2)5 – CO- ]n + (n – 1)Н2О
8. Сополиконденсация различных аминокислот с образованием полипептидов:
R – CH(NH2) – COOH + H2N – CH(R1) – COOH → R – CH (NH2) – C(O) – N(H) –CH(R1) –COOH
-H2O
Образование внутренних солей – биполярных ионов:
H2N – CH2 – COOH ⇄ H3N+ — CH2 – COO-
Взаимодействие с формальдегидом с образованием метиленаминокислот:
CH3 – CH(NH2) – COOH + CН2О → CH3 – CH(N=CH2) – COOH + H2O
5. Реакция со спиртами:
СН3 – СН(NH2) – СООН + С2Н5ОН ↔ СН3 – СН(NH2) – СООС2Н5 + Н2O
6. Взаимодействие с азотистой кислотой:
СН3 – СН(NH2) – СООН + HONO → CH3 – CH2OH + N2↑ + H2O + CO2↑
55)

56) Крахмал – основной источник резервной энергии в растительных клетках – образуется в растениях в процессе фотосинтеза и накапливается в клубнях, корнях, семенах:
6CO2 + 6H2O свет, хлорофилл → C6H12O6 + 6O2
nC6H12O6 → (C6H10O5)n + nH2O
глюкоза крахмал
Крахмал чаще всего получают из картофеля. Для этого картофель измельчают, промывают водой и перекачивают в большие сосуды, где происходит отстаивание. Полученный крахмал еще раз промывают водой, отстаивают и сушат в струе теплого воздуха.

В медицине применяют крахмал как наполнитель, а в хирургии - для приготовления неподвижных повязок. Широко используется в присыпках, мазях, пастах вместе с оксидом цинка, тальком. Внутрь применяют как обволакивающее при желудочно-кишечных заболеваниях.
Качественная реакция на крахмал.
(C6H10O5)n+nI2=комплекс синефиолетового цвета
57) Сахароза C12H22O11, или свекловичный сахар, тростниковый сахар, в быту просто сахар — дисахарид из группы олигосахаридов, состоящий из двух моносахаридов — α-глюкозы и β-фруктозы. Изомеры сахарозы:
С сахарозой гидроксид меди (II) образует голубой раствор:
С12H22O11 + Cu(OH)2 = голубой раствор
58) Целлюлоза (клетчатка) – растительный полисахарид, являющийся самым распространенным органическим веществом на Земле.
Физические свойства. Это вещество белого цвета, без вкуса и запаха, нерастворимое в воде, имеющее волокнистое строение. Растворяется в аммиачном растворе гидроксида меди (II) – реактиве Швейцера.
Нахождение в природе. Этот биополимер обладает большой механической прочностью и выполняет роль опорного материала растений, образуя стенку растительных клеток. В большом количестве целлюлоза содержится в тканях древесины (40-55%), в волокнах льна (60-85%) и хлопка (95-98%). Основная составная часть оболочки растительных клеток. Образуется в растениях в процессе фотосинтеза.
Состоит из остатков β - глюкозы

Целлюлоза используется в производстве бумаги, искусственных волокон, пленок, пластмасс, лакокрасочных материалов, бездымного пороха, взрывчатки, твердого ракетного топлива.
Гидролиз
(C6H10O5)n + nH2O t,H2SO4 → nC6H12O6
глюкоза
Гидролиз протекает ступенчато:
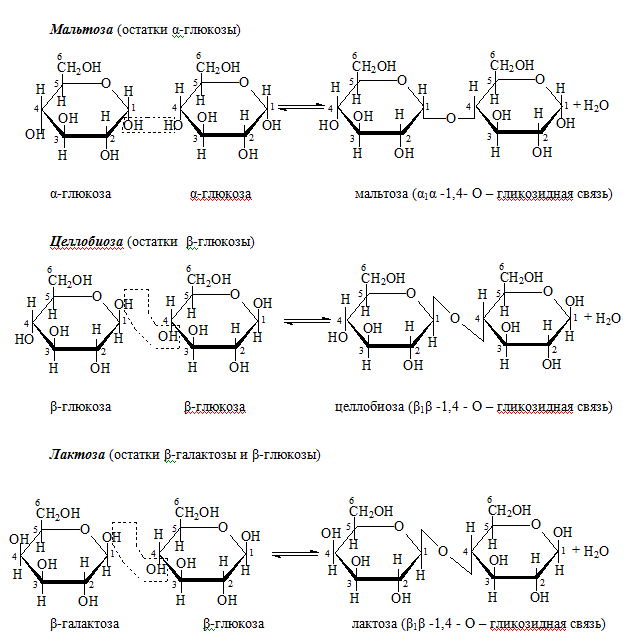
(C6H10O5)n → (C6H10O5)m → xC12H22O11 → n C6H12O6 (Примечание, m<n)
крахмал декстрины мальтоза глюкоза
59) Ферменты— обычно белковые молекулы или молекулы РНК или их комплексы, ускоряющие химические реакции в живых системах.
Витамины - органические, биологически активные вещества, необходимые для нормальной жизнедеятельности человека и животных; они играют решающую роль в обмене веществ. Витамины не синтезируются в организме или синтеризуются в недостаточном количестве. Они поступают с растительной или животной пищей. Большинство витаминов участвует в обмене веществ, входя в состав более чем 100 ферментов или конферментов.
Все витамины делят на жирорастворимые ( A, D, E, K), и водорастворимые ( B, C, PP и др.). Иногда одной буквой обозначаются несколько веществ или их смеси.
Гормоны — биологически активные вещества органической природы, вырабатывающиеся в специализированных клетках желёз внутренней секреции, поступающие в кровь и оказывающие регулирующее влияние на обмен веществ и физиологические функции. Гормоны служат гуморальными (переносимыми с кровью) регуляторами определённых процессов в различных органах и системах.
Лекарственные вещества разделяют по двум классификациям:
Фармакологическая
Химическая
Первая классификация более удобна для медицинской практики. Согласно этой классификации, лекарственные вещества делятся на группы в зависимости от их действия на системы и органы. Например:
Снотворные и успокаивающие(седативные);
Сердечно – сосудистые;
Анальгезирующие (болеутоляющие),жаропонижающие и противовоспалительные;
Противомикробные (антибиотики,сульфаниламидные препараты и др.);
Местно-анестезирующие;
Антисептические;
Диуретические;
Гормоны;
Витамины
60)
Качественная реакция на
белки. Белки выявляются в основном на
реакциях, основанных на окрасках.
Ксантопротеиновая реакция. Данная реакция обнаруживает ароматические аминокислоты, входящие в белки (на примере тирозина):
(OH)C6H4CH(NH2)COOH + HNO3 —-H2SO4——>
(OH)C6H3(NO2)CH(NH2)COOH↓ + H2O — выпадает осадок
желтого цвета.
(OH)C6H3(NO2)CH(NH2)COOH + 2NaOH ——->
(ONa)C6H3(NO2)CH(NH2)COONa + H2O — раствор становится
оранжевым.
