
Карцев В.Г. - Избранные методы синтеза и модификации гетероциклов. Том 2 (2003)(ru)
.pdf
Производные бензотионинов 27a–b, 28 синтезированы 2,3-сигматропной перегруппировкой ацетиленовых илидов 29a–c, полученных из бициклических солей 30a–c [29]. Строение продуктов зависит от характера заместителя при тройной связи. Илиды с алкильными заместителями 29a, b превращаются в алленовые сульфиды 27a, b, тогда как арильный заместитель способствует изомеризации в 1,3-диены 28 (схема 7).
|
|
|
|
|
|
Схема 7 |
|
|
|
|
R = Me, Bu |
S |
O |
|
DBU |
|
|
|
|
OEt |
|
S+ |
|
|
27a−b |
R |
|
|
S+ |
− |
|
|
||
OTf |
− |
|
|
R = Ph |
S |
O |
O OEt |
O |
|
|
|
||
|
|
OEt |
|
OEt |
||
|
|
R |
|
|
|
|
|
R |
|
|
|
Ph |
|
|
30a−c |
29a−c |
|
|
28 |
|
|
R = Me (a), Bu (b), Ph (c) |
|
|
|
|
|
Перегруппировка Соммле–Хаузера арилзамещенных илидов 31, образующихся при десилилировании солей 32, дает 3-замещенные 7,8-дигидро-5Н,13Н- дибензо[c,f]тионины 33 [30] (схема 8).
Схема 8
|
a |
S |
S+ |
|
|
S+ |
− |
|
− |
|
CH2 |
OTf |
SiMe3 |
R |
|
|
|
R |
R |
|
32 |
31 |
33 |
a - CsF, DBU, ДМСО, 20°C; |
|
|
R = H, Me, OMe, CF3 |
|
|
Перегруппировка цианстабилизированного илида 34 происходит по-иному, с образованием спиро[4,5]тиекинового производного 35 [31]. При взаимодействии илида 34 с сукцинимидом образуется экзоциклический метилид 36, 2,3-сигма- тропная перегруппировка которого приводит к соединению 35. При термолизе соединение 35 изомеризуется в тетрагидротиепин 37, а при ваимодействии с эфиром ацетилендикарбоновой кислоты дает циклоаддукты 38a, b (схема 9).
Избранные методы синтеза и модификации гетероциклов, том 2 |
211 |

Схема 9
O
|
|
a |
|
− N |
|
|
+ |
|
|
− S |
+ |
|
S |
+ |
O |
|
S |
− |
|
|
|
|
− |
O |
CH2 |
||||
CN |
|
|
CN |
|
O N |
CN |
|
|
|
|
|
|
H |
|
|
|
|||
34 |
|
|
|
|
|
|
36 |
|
|
|
|
|
b |
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
CN |
|
NC |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
37 |
|
|
|
|
|
|
|
|
EtO |
C |
|
EtO2C |
|
|
|
|
|
|
2 |
|
|
EtO2C |
|
|
35 |
|
|
EtO2C |
S |
|
|
|
||
|
|
|
|
|
|
||||
|
|
|
c |
|
|
|
+ |
|
S |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
CN |
|
38b |
CN |
|
|
|
|
|
|
38a |
|
|
||
|
a - |
, бензол; b - 205°C; c - EtO2CHC=CHCO2Et |
|
|
|||||
|
|
O N |
O |
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
При взаимодействии 1-цианоилидов 34 с активированными ацетиленами получается смесь соединений 39 и 40 (~1 : 1) с общим выходом 75% [31]. Согласно механизму реакции в качестве промежуточного соединения образуется цвиттерион 41, который изомеризуется по двум разным направлениям. При внутримолекулярном депротонировании S-метильной группы (путь а), образуется илид 42, 2,3-сигматропная перегруппировка которого приводит к соединению 39. За счет нуклеофильной атаки винильного аниона на положительно заряженный атом серы образуется нестабильный σ-сульфурановый интермедиат 43, превращающийся в илид 40 (схема 10).
Схема 10
R |
R' |
|
|
− S + |
|
S+ |
|
CN |
NC |
− |
|
R |
R' |
||
|
|||
34 |
41 |
|
212 |
Серия научных монографий InterBioScreen |

а |
S |
+ |
− |
|
S |
|
|
|
|||
|
|
|
CH |
|
|
|
NC |
|
2 |
|
|
|
|
|
|
|
|
|
R |
|
R' |
NC |
R' |
|
|
|
|
R |
|
|
42 |
|
|
39 |
b |
|
S |
+ |
|
S |
||
NC |
R |
R' |
− R' |
|
NC |
R |
|
|
|
||
|
43 |
|
40 |
R = H, R' = CO2Me; R = R' = CO2Me
Реакция цианстабилизированного трициклического илида серы 44а – производного тиафенантрена – с активированными ацетиленами протекает с образованием спироциклических соединений 45 (до 31%) [32]. Соединения 45 образуются в результате атаки карбаниона промежуточного илида 46а на атом С(4) и одновременным разрывом связи С(10)-S (перегруппировка Соммле–Хаузера). При нагревании соединения 45 претерпевают 1,5-перегруппировку, давая дибензотиониновые производные 47 с выходом до 95%. В случае этильного заместителя у атома серы в соединении 46b возникает стерическое препятствие для такой 2,3-сигматропной перегруппировки, и в результате протекает 1,2-перегруппировка Стивенса с образованием продукта расширения цикла 48 (путь b) (схема 11).
Схема 11
|
|
EC CE |
|
|
|
|
− S + |
|
PhH |
S+ R |
|
S+ − |
R |
CN |
R |
NC |
− |
NC |
|
|
E |
E |
E |
E |
|
||
|
|
|
||||
44a, b |
|
|
|
46a, b |
|
|
Избранные методы синтеза и модификации гетероциклов, том 2 |
|
213 |
||||

S |
CN |
|
|
|
a |
|
|
S |
|
R = H |
|
200°C |
|
|
|
|
|
||
|
E |
|
|
|
|
|
|
|
|
|
E |
|
|
E |
45 |
|
|
NC |
|
|
|
E |
||
|
|
|
|
|
|
|
|
|
47 |
b
S
R = Me
NC  E E
E E
48
R = H, Me; E = CO2Me, CO2Et
В последнее время появилось много публикаций, посвященных синтезам гетероциклических соединений с участием тиокарбонильных илидов. Тиокарбонильные илиды – доступные, весьма реакционноспособные промежуточные соединения, которые легко подвергаются перегруппировкам, вступают в реакции циклоприсоединения с диполярофилами и в реакции 1,3- и 1,5-электроциклизации. Эти реакции, как правило, проходят с высокой регио- и стереоселективностью. Описано несколько способов получения тиокарбонильных илидов: реакции 1,3-ди- полярного циклоприсоединения диазосоединений к тиокетонам с образованием 1,3,4-тиодиазолинов и последующим элиминированием азота [33]; присоединение тиокетонов к оксиранам [34]; фотоизомеризация арилвиниловых сульфидов [35]; взаимодействие диазосоединений с тиокетонами в присутствии катализаторов [36]. Так, производные дигидротиофена 49 и 50 получены 1,5-электроциклизацией винилтиокарбонильных илидов (схема 12), образующихся при взаимодействии диазосоединения 51 с тиохромонами 52, 53 [37].
|
|
|
|
|
Схема 12 |
|
R |
Ph |
CN |
Ph |
|
S |
CN |
+ − |
R |
|
CN |
N2 |
S |
S |
|||
|
|
|
R |
||
|
|
|
|
||
|
Ph 51 |
|
|
|
|
O |
Rh2(OAc)4 |
O |
|
O |
|
|
|
|
|||
52 |
|
|
|
49 (83%) |
|
214 |
Серия научных монографий InterBioScreen |

|
|
|
|
|
|
|
|
Ph |
|
R |
|
|
S |
|
|
|
|
|
S |
|
|
|
|
|
|
|
|
|
|
CN |
||
|
|
|
|
|
51 |
|
|
|||
|
|
|
|
|
|
|
|
|
||
|
|
O |
|
Rh2(OAc)4 |
|
O |
|
|
||
|
|
|
|
|
|
|
|
|
||
|
|
53 |
|
|
|
|
|
50 (66%) |
||
|
|
|
|
R = 4-ClC6H4 |
|
|
|
|
||
При взаимодействии тиокарбонильных илидов с диенофилами с высоким |
||||||||||
выходом и региоселективностью образуются продукты 1,3-диполярного цикло- |
||||||||||
присоединения. Этим методом были получены замещенные тиоланы 54–56 [38]. |
||||||||||
Исходные илиды 57 генерировали нагреванием тиадиазолинов 58, полученных в |
||||||||||
реакции тиокетонов 59 с диазометаном (схема 13). |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
Схема 13 |
|
O |
|
|
O |
|
R |
∆ |
O |
|
|
R |
S |
CH2N2 |
|
S |
|
R |
− |
S |
||
|
−70°C |
|
|
S |
−N2 |
|
+ |
|||
|
S |
N |
N |
|
S |
|||||
|
|
|
|
|
|
|
||||
|
59 |
|
|
58 |
|
|
|
|
57 |
|
|
|
|
|
|
|
|
O |
OMe |
|
|
|
|
|
CO2Me |
|
S |
|
|
54 |
||
|
|
|
|
|
|
R |
S |
|
||
|
|
|
|
|
|
O |
O |
|
|
|
|
|
NC |
CO2Et |
|
|
|
|
|
||
|
|
|
|
S |
R |
|
|
|||
|
|
|
|
|
|
|
|
|
||
|
|
EtO2C |
CN |
|
|
S |
|
|
||
|
|
|
NC |
|
55 |
|||||
|
|
|
|
|
|
|
CN |
|||
|
|
|
|
|
|
EtO2C |
|
CO2Et |
|
|
|
|
|
O |
|
|
O |
R O |
|
|
|
|
|
O |
O |
|
S |
|
|
|
||
|
|
|
|
|
|
S |
|
O |
56 |
|
|
|
|
|
|
|
|
|
O |
|
|
Аналогично были получены замещенный тиолан 60 и 1,3-дитиоланы 61а–с и |
||||||||||
62а–е [39] (схема 14). |
|
|
|
|
|
|
|
|
|
|
Избранные методы синтеза и модификации гетероциклов, том 2 |
215 |

Схема 14
|
|
O |
|
|
|
|
|
− |
CO2Me |
MeO |
|
|
|
|
|
|
|
|
|
|
|
||
CH2 |
|
|
|
S |
|
|
|
S + |
|
|
|
|
|
|
|
|
|
60 |
|
|
|
|
|
|
S |
S |
S |
|
S |
|
R |
R |
R |
|
+ |
|
S |
R |
|
|
|
|
|||||
|
|
R R |
|
|
|||
|
|
|
|
|
|
||
|
|
61a−c |
|
|
62a−e |
|
|
R2C = Ph2C (a), |
|
(b), |
|
|
|
|
|
S |
(c), |
(d), |
O |
|
(e) |
|
|
|
|
|
|
|
|
|
|
С высоким выходом и региоселективностью получены 1,3-дитиолановые спироциклические циклоаддукты 63а–с реакцией 1,3-диполярного циклоприсоединения тиокарбонильных илидов 64а–с с тиазол-5(4Н)-тионами 65 [40] (схема 15).
Схема 15
|
|
|
|
|
|
R' |
R" |
|
|
|
|
|
|
|
N |
S |
63a |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R'" |
S |
S |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
Ph |
Ph |
|
|
|
|
|
|
|
|
||
|
R' |
R2C |
|
+ |
− |
R' |
R" |
O |
|
S |
|
CH2 |
N |
S |
63b |
||
|
N |
R" |
64a−c |
|||||
|
|
S |
||||||
R'" |
S |
S |
|
|
|
R'" |
S |
|
|
|
|
|
|||||
|
65 |
|
|
|
|
R' |
R" |
|
|
|
|
|
|
|
N |
S |
63c |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
R'" |
S |
S |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
R2C=Ph2C (a), O |
(b), |
(c) |
|
|||
216 |
Серия научных монографий InterBioScreen |

2. Синтез и модификация азотсодержащих гетероциклов
Синтез азабициклооктана 66 – ключевого соединения для получения пирролизидиновых алкалоидов (±)-трахелантамедина 67a, (±)-изоретронеканола 67b и
(±)-супенидина 68 осуществлен внутримолекулярной циклизацией диазосульфида 69 [41, 42]. Образующийся циклический илид 70 в результате 1,2-перегруппировки превращается в продукт 66 (схема 16).
Схема 16
S Ph |
O |
Ph |
O |
OEt |
|||
N |
Rh2(OAc)4 |
S+− |
OEt |
N2 |
N |
|
|
|
|
|
|
O |
|
O |
|
69 |
|
70 |
|
H R R'
 ...
... 
Ph S |
O |
||
OEt |
|||
|
|
||
|
N |
|
|
O |
66 |
... |
|
|
|||
a R = CH2OH, R' = H; b R = H, R' = CH2OH
N
O 67a, b
H OH
N
O 68
В работе [43] исследованы стереоселективные реакции диазосульфидов 71a, b под действием родиевых, медных и палладиевых катализаторов, протекающие с образованием соединений пирролизидинового ряда 72a, b и 73a, b. Показано, что природа используемого катализатора значительно влияет на направление реакции. В случае капролактама родия (Rh2(Cap)4) преимущественно образуется циклический илид, 2,3-сигматропная перегруппировка которого дает азабициклооктаны 72a, b. Использование же катализаторов с электроноакцепторными лигандами
(Rh2(OAc)4, Cu(acac)2, Cu(OTf)2, Pd(OAc)2) позволяет преимущественно или селек-
тивно получать трициклические соединения 73a, b – продукты реакции внутримолекулярного циклопропанирования (схема 17).
Избранные методы синтеза и модификации гетероциклов, том 2 |
217 |

|
|
Ph |
|
|
|
|
Схема 17 |
H |
S |
H |
|
|
H |
S Ph |
|
|
|
|
Ph |
||||
|
|
кат. |
|
|
|
|
|
|
|
|
S |
+ |
|
|
|
N |
N2 |
бензол |
N |
N |
|
||
|
|
|
|||||
O |
|
|
O |
|
O |
|
|
|
|
|
|
|
|||
71a |
|
|
72a |
|
|
73a |
|
Ph S |
|
|
|
|
|
|
|
H |
|
|
H |
|
Ph |
H |
|
|
|
кат. |
|
|
|
|
|
|
|
|
S |
+ |
|
|
|
N |
|
бензол |
N |
N |
S Ph |
||
|
|
|
|||||
|
|
N2 |
|
O |
|
|
|
O |
|
|
|
|
O |
||
|
|
72b |
|
|
|
|
|
71b |
|
|
|
|
73b |
|
Высокая стереоселективность 1,2-перегруппировок и введение в указанные реакции хиральных сульфидов открывают широкие возможности для их использования в асимметрическом синтезе [14]. В частности, перегруппировки Стивенса позволяют решить такую ключевую проблему в синтезе природных азотсодержащих соединений, как стереоселективное формирование новых С-С связей в α-положении к атому азота. Так, на примере синтеза бициклического β-лактама 74 продемонстрирован новый подход к 6-амидокарбопенициллиновым антибиотикам [44]. Фотолиз диазокетона 76 приводит к илиду 75, который после перегруппировки дает соединение 74 со стереоселективным образованием новой связи С-С (схема 18).
Схема 18
O |
H Bn |
N2 |
O |
|
H |
Bn |
|
|
N |
O |
|
|
N |
|
O |
||
|
|
|
hν |
|
|
|
|
|
N |
S O |
OR |
|
N |
|
+ |
− |
O |
|
H |
S |
|
|||||
R |
H |
|
|
R |
|
|
OR |
|
76 |
|
|
75 |
|
||||
|
|
|
|
|
|
|||
H
Bn
O
 N
N
O
N  O
O
 R H S OR
R H S OR
74 (72%) R = 4-NO2C6H4
218 |
Серия научных монографий InterBioScreen |
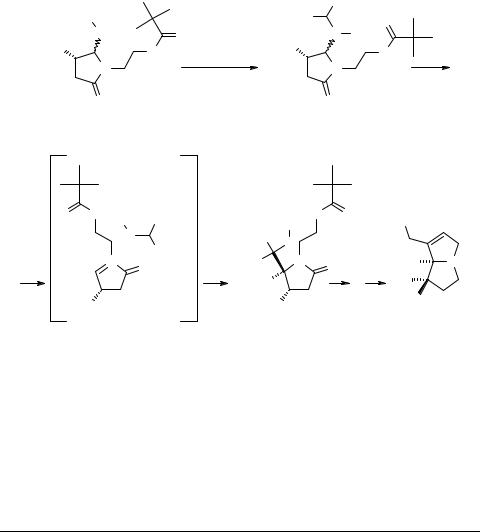
Развивая синтетический подход, использованный в предыдущей работе, авторы провели стереоселективный синтез алкалоидов (+)-гелиотридина 77a и
(+)-ретронецина 77b [45]. Оптически активный сульфид 78, легко получаемый из
(S)-яблочной кислоты, в каталитической реакции с α-диазомалонатом образует илид 79, 1,2-перегруппировка которого протекает с высокой стереоселективностью. Полагают, что в этой реакции превоначально происходит разрыв связи C-S и образуется ацилиминиевая соль 80. Нуклеофильная атака карбанионом связи С=N происходит преимущественно с наименее экранированной стороны (схема 19), в результате чего образуется производное 2,3-транс-пирролидона 81, на основе которого были получены алкалоиды 77a, b (схема 19).
Схема 19
|
|
|
|
CO2Bn |
||
|
Ph |
O |
BnO2C − |
|
O |
|
TBSO |
S |
TBSO |
S |
+ |
Ph |
|
O |
N2C(CO2Bn)2 |
|
O |
|||
|
|
N |
||||
|
N |
Rh2(OAc)4 |
|
|
||
|
|
|
|
|
|
|
|
O |
|
|
O |
|
|
|
78 |
|
|
79 |
|
|
O O Ph |
S |
CO2Bn |
BnO2C |
Ph O |
O |
HO |
|
|
|
|
− |
S |
|
|
|
||
|
|
CO2Bn |
|
|
|
|||
N |
+ |
BnO2C |
N |
O |
H |
N |
||
|
O |
|
||||||
|
|
|
|
H |
|
... |
R" |
|
TBSO |
|
|
|
TBSO |
|
|
R' |
|
|
|
|
|
|
|
|
||
80 |
|
|
81 (82.6%) |
|
|
77a, b |
||
a R' = H, R" = OH; b R' = OH, R" = H; |
|
|
|
|
||||
TBS - t-BuMe2Si |
|
|
|
|
|
|||
Предложен [46, 47] новый подход к стереоселективному синтезу синтетических аминокислот из хиральных лактамов. При взаимодействии активированных хиральных β-лактамов 82a, b с диметилсульфоксонийметилидом легко образуются β-кетосульфоксониевые илиды 83a, b. Последние под действием родиевых катализаторов стереоселективно дают производные 4-оксопирролидина 84a или 5-оксопиперидина 84b, которые получаются в результате циклизации промежуточных карбенов 85a, b. Соединения 84a, b использованы в синтезе оптически активных α-аминокислот [48] (схема 20).
Избранные методы синтеза и модификации гетероциклов, том 2 |
219 |

Схема 20
|
( |
|
) |
|
CO2Bn |
|
|
|
|
O− |
O− CO2Bn |
||||
|
|
|
|
|
a |
|
|
|
|
|
|
|
b |
||
n |
|
|
|
|
|
S 2+ |
|
|
|||||||
|
|
|
|
|
|
|
|
|
( )n NH |
||||||
O |
|
|
|
N |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
Boc |
|
|
|
|
|
|
|
Boc |
|||
|
|
|
82a, b |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
83a, b |
|
|
||||
|
|
|
|
|
O |
|
CO2Bn |
O |
|
|
|||||
|
. . |
( )n |
|
|
|
|
|
( |
)n |
||||||
|
|
NH |
|
N |
CO2Bn |
||||||||||
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
Boc |
|||||||
|
|
|
|
|
|
|
|
|
Boc |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
85a, b |
|
|
|
|
84a, b |
||||
|
|
|
|
|
Boc = t-BuOCO; n = 1 (a), 2 (b); |
|
|
||||||||
|
|
|
|
|
a - Me SOCH , ДМСО, 20°C (97%); b - [Rh2+] |
||||||||||
|
|
|
|
|
|
2 |
2 |
|
|
|
|
|
|
|
|
Перспективный путь к синтезу азотсодержащих гетероциклов, в том числе аналогов алкалоидов, открывает реакция внутримолекулярной циклизации фталимидозамещенных карбонилстабилизированных илидов серы [49–56]. Из N-фта- лоил-α- 86 и β-аминокислот 87 в условиях реакции Арндта–Эйстерта [57, 58] генерируют бромкетоны, легко образующие соответствующие сульфониевые соли. Внутримолекулярная циклизация стабилизированных илидов 88 и 89, полученных депротонированием этих солей, происходит при нагревании в толуоле с эквимольными количествами бензойной кислоты [53]. В результате образуются метилтиозамещенные пирролизидин- 90 и индолизидиндионы 91 (схема 21). Важно отметить, что при использовании оптически активных илидов рацемизация не происходит.
Схема 21
|
|
|
OH |
|
|
|
O |
S + |
|
|
|
R |
|
O |
|
R |
|
− |
|
|
|
|
|
N |
|
|
N |
O |
|
R |
||
O |
|
O a, b, |
O |
|
O |
|
||||
|
|
|
|
|
||||||
|
|
|
|
f |
N |
|
||||
|
|
|
c, d, e |
|
|
|
|
O |
||
|
|
|
|
|
|
|
|
−PhCO2Me |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
|
|
86 |
|
|
|
88 |
|
|
90 |
|
|
|
|
R = H, Me, i-Pr, Bn |
|
|
|
|
|
|
|
220 |
Серия научных монографий InterBioScreen |
