
- •Задания и методические указания к выполнению конторольныХ работ по дисциплине «транспортная энергетика»
- •С о д е р ж а н и е
- •Основные положения термодинамики. Частные процессы
- •1.1. Основные понятия и определения
- •Теплоемкости идеального газа
- •1.2. Термодинамические процессы с участием идеальных газов
- •1.2.1. Изотермический процесс
- •1.2.2. Изохорный процесс
- •1.2.3. Изобарныйй процесс
- •1.2.4. Адиабатный процесс
- •2. Метод термодинамических циклов
- •2.1. Цикл Карно
- •2.2. Цикл двигателя внутреннего сгорания с подводом теплоты при постоянном объеме (цикл Отто)
- •2.3. Теоретический цикл двигателя внутреннего сгорания с сообщением теплоты при постоянном давлении. Цикл Дизеля
- •2.4. Теоретический цикл двигателя с сообщением теплоты при постоянных объеме и давлении. Смешанный цикл Тринклера
- •3. Задания и исходные данные к контрольной работе
- •3.1. Задание 1. Термодинамические процессы
- •Условие задания
- •Учебно-методическое и информационное обеспечение контрольной работы
- •Конторольная работа по дисциплине «транспортная энергетика»
Теплоемкости идеального газа
Для одноатомных газов:
mсv = (3/2)R; сv = (3/2)R0 и mср = (5/2)R; ср = (5/2)R0. (1.1.8)
Для двухатомных газов:
mсv = (5/2)R; сv = (5/2)R0 и mср = (7/2)R ; ср = (7/2)R0 . (1.1.9)
1.2. Термодинамические процессы с участием идеальных газов
1.2.1. Изотермический процесс
И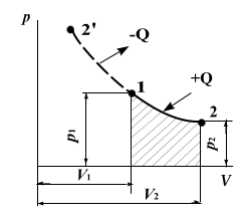 зотермическим
называют
процесс, проводимый при постоянстве
температуры (рисунок 1.2.1). В
р-V –
координатах процесс изображается
равнобокой гиперболой (изотермой),
уравнение которой :
зотермическим
называют
процесс, проводимый при постоянстве
температуры (рисунок 1.2.1). В
р-V –
координатах процесс изображается
равнобокой гиперболой (изотермой),
уравнение которой :
рV = (М/μ)RТ = const. (1.2.1)
Уравнение изотермического процесса:
р1V1 = р2V2 , (1.2.2)
Рисунок
1.2.1-Диаграмма
изотермического
процесса
Работа изотермического процесса:
L = (М/ μ)RТln (V2/V1). (1.2.3)
Теплота изотермического процесса:
Q = L. (1.2.4)
Изменение внутренней энергии:
U = U2 - U1 = 0 (1.2.5)
Теплоемкость в изотермическом процессе:
сизот
= ![]() (1.2.6)
(1.2.6)

1.2.2. Изохорный процесс
Изохорным называют процесс, при совершении которого объем системы не изменяется (рисунок 1.2.2). В р-V – координатах процесс изображается прямой линией, параллельной оси р (изохорой), уравнение которой :
р/[(М/ μ)RТ] = V = const. (1.2.7)
Рисунок
1.2.2-Диаграмма
изохорного процесса
Уравнение изохорного процесса:
р1/Т1 = р2/Т2. (1.2.8)
Работа изохорного процесса: L = р ΔV = 0. (1.2.9)
Теплота процесса:
Q
=
![]() U
= U2
- U1
= М.сv(Т2
- Т1)
=
U
= U2
- U1
= М.сv(Т2
- Т1)
=![]() .
(1.2.10)
.
(1.2.10)
Изменение внутренней энергии ΔU: см. формулу (1.2.10).
Теплоемкость: сизохор = сv. (1.2.11)
1.2.3. Изобарныйй процесс
И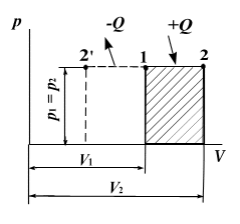 зобарным
называют процесс, при совершении которого
давление в системе остается неизменным
(рисунок 1.2.3). В
р-V –
координатах процесс изображается прямой
линией, параллельной оси V
(изобарой),
уравнение которой :
зобарным
называют процесс, при совершении которого
давление в системе остается неизменным
(рисунок 1.2.3). В
р-V –
координатах процесс изображается прямой
линией, параллельной оси V
(изобарой),
уравнение которой :
[(М/μ)RТ]/V = р = const . (1.2.12)
Уравнения изобарного процесса:
Рисунок
1.2.3-Диаграмма
изобарного процесса
Т1/V1 = Т2/V2 . (1.2.13)
Работа процесса:
L = р(V2 - V1) . (1.2.14)
Теплота процесса:
Q = (U2 - U1) + р(V2 - V1) = М сv (Т2 - Т1) + р(V2 - V1) =
= (М/μ)mсv (Т2 - Т1) + р(V2 - V1). (1.2.15)
Изменение внутренней энергии ΔU:
ΔU = U2 - U1 = (М/μ).mсv (Т2 - Т1). (1.2.16)
Теплота процесса и изменение энтальпии (Н = U + рV) системы:
Q = (U2 + рV2) - (U1 + рV1) = Н2 - Н1 = Δ Н = Мср (Т2 - Т1). (1.2.17)
Изобарная теплоемкость: сизобар = ср. (1.2.18)
