
- •Задания и методические указания к выполнению конторольныХ работ по дисциплине «транспортная энергетика»
- •С о д е р ж а н и е
- •Основные положения термодинамики. Частные процессы
- •1.1. Основные понятия и определения
- •Теплоемкости идеального газа
- •1.2. Термодинамические процессы с участием идеальных газов
- •1.2.1. Изотермический процесс
- •1.2.2. Изохорный процесс
- •1.2.3. Изобарныйй процесс
- •1.2.4. Адиабатный процесс
- •2. Метод термодинамических циклов
- •2.1. Цикл Карно
- •2.2. Цикл двигателя внутреннего сгорания с подводом теплоты при постоянном объеме (цикл Отто)
- •2.3. Теоретический цикл двигателя внутреннего сгорания с сообщением теплоты при постоянном давлении. Цикл Дизеля
- •2.4. Теоретический цикл двигателя с сообщением теплоты при постоянных объеме и давлении. Смешанный цикл Тринклера
- •3. Задания и исходные данные к контрольной работе
- •3.1. Задание 1. Термодинамические процессы
- •Условие задания
- •Учебно-методическое и информационное обеспечение контрольной работы
- •Конторольная работа по дисциплине «транспортная энергетика»
1.2.4. Адиабатный процесс
Адиабатным называют процесс, в котором и система и окружающая среда не обмениваются энергией в форме теплоты (рисунок 1.2.4).
Уравнение адиабатного процесса:
рVk= const , (1.2.19)
где k = mсp /mсv = сp /сv.
Для идеальных одноатомных газов k = 1,66, а для двухатомных k = 1,4.
Адиабатный процесс в р-V – координатах процесс изображается неравнобокой гиперболой (адиабатой):
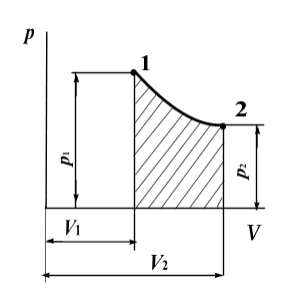
Уравнения адиабатного процесса:
р1V1k = р2V2k; Т1V1k - 1 = Т2 V2k – 1,
р11 - kТ1k = р21 - k Т2k. (1.2.20)
Работа процесса:
L
=
![]() U
= U2
- U1
= М сv
(Т2
-
Т1)
=
U
= U2
- U1
= М сv
(Т2
-
Т1)
=
= (М/μ)mсv (Т2 - Т1). (1.2.21)
Рисунок
1.2.4-Диаграмма адиабатного процесса
Теплота процесса
Q = 0 . (1.2.22)
Изменение внутренней энергии см. формулу (1.2.21).
Теплоемкость садиабат. = 0.
2. Метод термодинамических циклов
Круговым циклическим процессом называют процесс, в котором термодинамическая система, пройдя ряд состояний, возвращается в исходное состояние, При этом возможно неоднократное повторение соответствующих преобразований, каждое из которых представляет собой замкнутый цикл. Практически все тепловые двигатели работают с использованием тех или иных циклов. Существенным для работы двигателя, преобразующего тепловую энергию в работу является то, что находящееся в двигателе рабочее упругое тело (газ) обязательно контактирует с, так называемым, нагревателем, получая от него теплоту (Qн) и холодильником, которому рабочее тело отдает часть тепла (Qх). Таким образом, полное превращение тепла в работу невозможно.
Исследование закономерностей работы тепловых двигателей на основе количественного анализа термодинамических процессов, составляющих замкнутый цикл конкретного типа теплового двигателя, проводится с использованием метода термодинамических циклов. Циклы, рассматриваемые в данном методе, составляются из равновесных частных термодинамических процессов, моделирующих реальную работу двигателя. Такой анализ позволяет выявить наиболее эффективные условия превращения тепла в работу.
2.1. Цикл Карно
Цикл Карно начинается с изотермического процесса 34 в котором, получивший от нагревателя теплоту (Qн) газ расширяется, производя работу. Затем, контакт с нагревателем прерывается, но газ продолжает расширяться 41 в адиабатических условиях.
В состоянии 1 газ приводится в контакт с холодильником и отдает ему теплоту (Qх).
П
Рисунок
2.1-Теоретическая
диаграмма цикла
Карно
идеального
газа
Итак, цикл Карно состоит из следующих термодинамических процессов: изотермического 34; адиабатического 41; изотермического 12 и адиабатного 23.
При количественном анализе цикла Карно необходимо обращаться к формулам и определениям, рассмотренным нами ранее в разделе 1.
Так, для изотермического процесса 34 :
Qн = L 34 = (М/μ)RТн.ln(V4/V3), (2.1.1)
а для изотермического процесса 12:
Qх = L12 = (М/μ)RТхln(V2/V1). (2.1.2)
Полезная работа цикла определяется алгебраической суммой: L0 = L34 + L12. С другой стороны, полезная работа совершается за счет алгебраической суммы теплот L0 = Qн + Qх. Таким образом, энергетический баланс запишется в виде:
Qн + Qх = L34 + L12 = (М/μ)R(Тн ln(V4/V3) - Тх ln(V1/V2). (2.1.3)
Используя уравнения адиабаты, для точек 4 и 1: р4 V4k= р1V1k и для точек 2, 3: р3 V3k = р2 V2k, применяя так же уравнения изотерм: р3V3 = р4V4 ( 34) и р1V1 = р2 V2 ( 12), найдем соотношение: V4/V3 = V1/V2 . Последнее позволит упростить уравнение (2.1.3):
Qн + Qх = (М/μ)R(Тн - Тх)ln(V4/V3) . (2.1.4)
Последняя формула позволит определить термический коэффициент полезного действия цикла Карно (). Согласно определению, он равен отношению полезно затраченной теплоты ко всей исходной теплоте процесса:
= (Qн + Qх)/Qн.
Подставляя в определительное уравнение для выражения из формул (2.1.4) и (2.1.1) найдем:
![]() (2.1.5)
(2.1.5)
К.П.Д. цикла Карно с идеальным газом зависит только от абсолютных температур нагревателя и холодильника.
