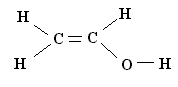Лабораторные работы / Лабораторные работы - 2003 / Отчёты / 1 / Отчет по лабе 1 - C2H4O
.docОтчет о лабораторной работе №1
Студентов группы О-21
«Неэмпирический квантовохимический расчет молекулы C2H4O»
1. ЦЕЛИ И ЗАДАЧИ РАСЧЕТА.
Цель расчета: Определение критериев выбора и изучение принципов построения стандартного базисного набора для расчета молекулярных систем. Изучение методов интерпретации результатов расчета и представления молекулы в виде вектора свойств на их основе. Знакомство с программным комплексом GAMESS.
Задача расчета: Выбрать наименьший из возможных оптимальный базис для неэмпирического расчета длин связей и валентных углов молекулы C2H4O по программному комплексу GAMESS с точностью порядка 0.01 Å для длин связей и 1 градус для валентных углов, сравнимой с экспериментальной. На основании результатов расчета оценить стабильность и факторы, определяющие реакционную способность этой молекулы.
2. ХАРАКТЕРИСТИКА И ОБОСНОВАНИЕ МЕТОДА РАСЧЕТА.
Расчет молекулы C2H4O осуществлен по программному комплексу GAMESS в стандартном базисном наборе Попла 6-31G*. Этот базис является валентно-расщепленным. Валентные МО представлены линейными комбинациями 2 сжатых комбинаций гауссовых орбиталей, остовные МО – 1-й. На каждом неводородном атоме также центрировано по 6 компонент поляризационных d-функций. Таким образом, базис для расчета молекулы C2H4O состоит из 52 функций:
2*C(1(1s) + 2*4(2s + 2p) + 6(3d)) + 1*O(1(1s) + 4*2(2s + 2p) + 6(3d)) +4*H(2(1s)) = 52
Все валентные базисные функции двухэкспоненциальные (6-31G*), остовные 1s МО - одно-экспоненциальные. s- и p-сжатия, соответствующие (с формальной точки зрения) одному главному квантовому числу n, свернуты в sp-оболочки [(2s + 2p), (3s + 3p)] и представлены различными линейными комбинациями гауссовых примитивов с одинаковыми экспонециальными множителями.
Каждая экспонента остовного сжатия представлена линейной комбинацией из 6 гауссовых примитивов (6-31G*). Каждая экспонента сжатия для валентных электронов представлена линейной комбинацией либо из 3 (6-31G*), либо из 1 (6-31G*) гауссовых примитивов.
Базис 6-31G* является наименьшим из возможных базисов для расчета длин связей и валентных углов молекулы C2H4O с экспериментальной точностью. Добавление поляризационных d-функций (6-31G*) учитывает поляризацию «рыхлых» электронных оболочек атомов галогенов при образовании связей (обеспечивает уменьшение длины связей ~ 0.05 Å).
3. ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ РАСЧЕТА.
1. Оценка стабильности молекулы.
Энтальпия образования молекулы C2H4O из простых веществ равна:
fH0 (C2H4O) = E(C2H4O) - E(C2) – 1/2E(O2) – 4E(H2) = -152.888+ ½*149.533 +75.37903 + 2*1.12683 = -0,48884 а. е -306,986 ккал/моль = -1283,44942 кДж/моль
Вывод: Молекула C2H4O стабильна в стандартных условиях.
2. Свойства связей молекулы C2H4O.
Уточненная геометрия и порядки связей молекулы C2H4O:
|
Связь |
Длина, А |
Порядок |
Валентный угол, град 126.956 122.397 110.384 122.397 |
Атомы C=C-O C2-C1-H C-O-H H-C2-C1 |
|
C=C |
1.318 |
1.891 |
||
|
C-O |
1.347 |
0.963 |
||
|
O-H |
0.948 |
0.755 |
||
|
С1-H |
1.077 |
0.957 |
||
|
C2-H |
1.074 |
0.945 |
Обычно неэмпирические расчеты в базисе 6-31G* позволяют получить геометрию молекул, подобных исследуемой, с экспериментальной точностью. Аналогичной степени точности следует ожидать и для молекулы C2H4O.
Валентность атомов по Коулсону в молекуле C2H4O:
ATOM ВАЛЕНТНОСТЬ
1 C 3.829
2 C 3.771
3 O 1.764
4 H 0.768
5 H 0.927
6 H 0.943
7 H 0.941
Сопоставляя длину связей в молекуле C2H4O с их порядком и валентностью атомов, можно сделать вывод: Связи в молекуле C2H4O ковалентные полярные.
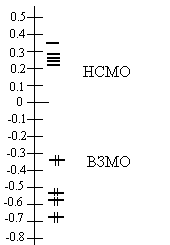
3. Энергетическая диаграмма (а.е.):
|
|
№ орбитали |
Энергия |
|
|
8 |
-0,6702 |
||
|
9 |
-0,5764 |
||
|
10 |
-0,5413 |
||
|
11 |
-0,5317 |
||
|
12 |
-0,3457 |
||
|
13 |
0,208 |
||
|
14 |
0,2273 |
||
|
15 |
0,277 |
||
|
16 |
0,2974 |
||
|
17 |
0.3451 |
4.Определение нуклеофильных и электрофильных свойств молекулы C2H4O.
Энергия НВМО молекулы C2H4O положительна (0,2080 а.е.).
Вывод: Молекула C2H4O - нуклеофил.
5. Определение жесткости и мягкости молекулы.
ВЗМО молекулы C2H4O невырождена. Разница ее энергии и энергии более низколежащих МО составляет 0,1860 а.е.= 5,0592 эВ.
Вывод: Молекула C2H4O является мягким реагентом.
Жесткость молекулы C2H4O:
=
![]() (ЕНВМО
– ЕВЗМО) = ½(0.208
+ 0.3457)
= 0,2768
а.е.
(ЕНВМО
– ЕВЗМО) = ½(0.208
+ 0.3457)
= 0,2768
а.е.
Мягкость молекулы C2H4O:
S=![]() =1,806
а.е.-1
=1,806
а.е.-1
6. Определение положения реакционных центров.
Реакционная способность молекулы C2H4O как мягкого реагента определяется граничной плотностью электронов на атомах. Распределение граничной плотности электронов на атомах следующее:
ATOM Заселенность по Малликену ЗАРЯД АТОМОВ
1 C 6.504384 -0.504384
2 C 5.789299 0.210701
3 O 8.709519 -0.709519
4 H 0.546535 0.453465
5 H 0.800352 0.199648
6 H 0.834553 0.165447
7 H 0.815359 0.184641
Максимальная граничная плотность электронов на атоме O.
Вывод: Атом O – наиболее вероятный центр электрофильной атаки.
7. Оценка растворимости.
Электрический дипольный момент молекулы C2H4O имеет большую величину 1.054 D.
Вывод: Молекула C2H4O растворима преимущественно в сильно полярных растворителях (спирты, арилгалогениды).