
- •Л.В. Кольцов, м.А. Лосева
- •Глава 1.1
- •Классификация по агрегатному состоянию фаз
- •Глава 1.2 Молекулярно-кинетические свойства дисперсных систем
- •Тема 1.2.1.Броуновское движение
- •Тема 1.1.2. Диффузия
- •Тема 1.2.3. Осмотическое давление
- •Глава 1.3 Оптические свойства и методы исследования дисперсных систем
- •Глава 2.1 Термодинамика поверхностного слоя
- •Тема 2.1.1. Термодинамическая характеристика дисперсных систем. Термодинамический метод избыточных величин Гиббса и метод «слоя конечной толщины
- •Тема 2.1.2. Поверхностное натяжение. Методы измерения поверхностного натяжения. Зависимость поверхностного натяжения от температуры и концентрации. Уравнение Шишковского
- •Тема 2.1.3. Уравнение Гиббса-Гельмгольца для поверхностной энергии. Полная поверхностная энергия
- •Глава 2.2 Адсорбция
- •Тема 2.2.2.Фундаментальное уравнение Гиббса. Определение Гиббсовской адсорбции. Адсорбционное уравнение Гиббса
- •Тема 2.2.3.Поверхностная активность. Поверхностно-активные и поверхностно-инактивные вещества. Анализ уравнения Гиббса. Пав. Эффект Ребиндера. Правило Дюкло-Траубе
- •Глава 2.3 Адсорбционные равновесия
- •Тема 2.3.3. Адсорбция на границе «твердое тело – жидкость». Молекулярная адсорбция. Правило выравнивания полярностей Ребиндера
- •Глава 2.4 Адгезия. Когезия. Смачивание и растекание жидкости
- •Тема 2.4.1. Понятие когезии и адгезии. Смачивание и растекание. Работа адгезии и когезии. Уравнение Дюпре. Краевой угол смачивания. Закон Юнга. Гидрофобные и гидрофильные поверхности
- •Тема 2.4.2.Коэффициент растекания по Гаркинсу. Условие растекания и смачивания. Эффект Марангони. Правило Антонова
- •Глава 2.5 Адсорбция ионов на кристалле. Электрокинетические явления
- •Тема 2.5.1. Образование и строение дэс. Электрокинетический потенциал. Правила написания мицелл
- •Тема 2.5.2. Обменная адсорбция. Иониты. Уравнение Никольского
- •Тема 2.5.3. Электрокинетические явления. Электрофорез. Электроосмос. Расчет -потенциала по скорости электрофореза и электроосмоса. Понятие поверхностной проводимости
- •Глава 3.1 Стабилизация и коагуляция дисперсных систем
- •Тема 3.1.1. Виды устойчивости дисперсных систем. Лиофобные и лиофильные золи
- •Правила коагуляции:
- •Тема 3.1.3. Теория длфо
- •Тема 3.1.4. Виды коагуляции: концентрационная и нейтрализационная. Коагуляция смесями электролитов. Явление «неправильные ряды». Механизм и кинетика коагуляции
- •При коагуляции смесью электролитов различают два типа процессов:
- •Тема 3.1.5. Седиментация и диффузия. Гипсометрический закон. Седиментационно-диффузионное равновесие. Скорость седиментации
- •Глава 4.1 Теория структурообразования Управление структурно-механическими свойствами материалов
- •Тема 4.1.2. Классификация дисперсных систем по структурно-механическим свойствам. Возникновение объемных структур в различных дисперсных системах
- •Глава 5.1 Свойства растворов высокомолекулярных соединений
- •Тема 5.1.1. Свойства вмс. Мембранное равновесие Доннана. Набухание вмс. Их растворение. Давление набухания. Степень набухания. Пластификаторы. Уравнение Хаггинса
- •Тема 5.1.2. Белки как полиэлектролиты.
- •Тема 5.1.3. Вязкость дисперсных систем и растворов вмс. Уравнение Бингама. Удельная, характеристическая, относительная вязкости. Методы измерения вязкости. Тиксотропия
- •Рассмотрим три наиболее распространенных метода измерения вязкости:
- •Глава 6.1 суспензии
- •Глава 6.2 пасты
- •Глава 6.3 эмульсии
- •Глава 6.4 пены
- •Глава 6.5 аэрозоли
- •Классификация аэрозолей
- •Глава 6.6 порошки
|
|
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ РОССИЙСКОЙ ФЕДЕРАЦИИ ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «САМАРСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ» |
Л.В. Кольцов, м.А. Лосева
ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ
В ДИСПЕРСНЫХ СИСТЕМАХ
УЧЕБНОЕ ПОСОБИЕ
Самара 2005
УДК 543
Поверхностные явления в дисперсных системах: Учеб. пособие/Л.В. Кольцов, М.А. Лосева; Самар. гос. техн. ун-т. Самара, 2005. 131 с.
Кратко рассмотрены основные разделы курса «Поверхностные явления в дисперсных системах». Предназначено студентам заочного факультета химических специальностей для самостоятельного изучения теоретических основ курса.
ISBN 5-7964-0746-5
Ил. 40. Табл. 2. Библиогр: 7 назв.
Печатается по решению редакционно-издательского совета Самарского государственного технического университета
Рецензенты: д-р хим. наук И.К. Г а р к у ш и н
канд. хим. наук Н.А. Р а с щ е п к и н а
|
I
|
© Л.В. Кольцов, М.А. Лосева, 2005 © Самарский государственный технический университет, 2005 | |
|
Раздел 1. |
СВОЙСТВА ДИСПЕРСНЫХ СИСТЕМ | |
Глава 1.1
Предмет курса. Основные понятия. Шкала дисперсности.
Удельная поверхность. Степень дисперсности. Классификация
дисперсных систем. Понятия: дисперсная фаза и дисперсионная
среда. Методы получения дисперсных систем
Предмет курса «Поверхностные явления в дисперсных системах» (коллоидной химии) - изучение дисперсных систем и явлений, происходящих на поверхности раздела фаз.
Дисперсной называют систему, в которой одно вещество распределено в среде другого, причем между частицами и дисперсионной средой есть граница раздела фаз. Дисперсные системы состоят из дисперсной фазы и дисперсионной среды.
Дисперсная фаза - это частицы, распределенные в среде. Ее признаки: дисперсность и прерывистость (рис. 1.1.1.1).
Дисперсионная среда - материальная среда, в которой находится дисперсная фаза. Ее признак - непрерывность.
Поверхность раздела фаз характеризуется раздробленностью и гетерогенностью. Раздробленность характеризуется:
1)
степенью дисперсности:
![]() ,
[см-1;
м-1],
где В
- суммарная межфазная поверхность или
поверхность всех частиц дисперсной
фазы; V
- объем частиц дисперсной фазы.
,
[см-1;
м-1],
где В
- суммарная межфазная поверхность или
поверхность всех частиц дисперсной
фазы; V
- объем частиц дисперсной фазы.
2) дисперсностью - величиной, обратной минимальному размеру а:
![]() [
[![]() ;
;![]() ];
];
3)удельной
поверхностью:
![]() ,
[м2/кг;
см2/г];
,
[м2/кг;
см2/г];
![]() где
m
- масса частиц дисперсной фазы.
где
m
- масса частиц дисперсной фазы.
4)
кривизной
поверхности:
![]() .
Для частицы неправильной формы
.
Для частицы неправильной формы![]() ,
,
где r1 и r2 - радиусы окружностей при прохождении через поверхность и нормаль к ней в данной точке двух перпендикулярных плоскостей.
Дисперсная
система

































Дисперсная
фаза



Дисперсионная
среда
Поверхность раздела
фаз

Непрерывность


Гетерогенность Раздробленность










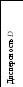
dx


dx







dy dy









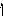

dz



dх “Плёнка”
dx
10-7 см,
dy,
dz
10-2
см





“Нить” dx,
dy
10-7 см
dz
10-2
см
“Суспензия”
(золь) dx,
dy,
dz![]() 10-7
см
10-7
см
Р
и с. 1.1.1.1. Характеристики дисперсной
системы
5) размером тела по трем осям, причем определяющим является размер по той оси, где он минимальный. В зависимости от размеров частиц они имеют свои исторические названия (см. рис. 1.1.1.1).
6) приведенным (эквивалентным, эффективным) радиусом - радиусом воображаемых идеально сферических частиц, обладающих той же массой и оседающих с той же скоростью, что и частицы дисперсной системы.
Классификация дисперсных систем осуществляется по нескольким признакам (рис. 1.1.1.2).
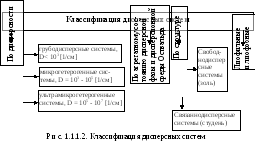

По дисперсности различают:
а) грубодисперсные системы, для них D < 103 [1/см] (рис. 1.1.1.3);
б) микрогетерогенные системы, для них D = 103 - 105 [1/см];
в) ультрамикрогетерогенные системы, для них D = 105 - 107 [1/см].
По агрегатному состоянию дисперсной фазы и дисперсионной среды. Эта классификация была предложена Оствальдом (см. табл. 1.1.1.1).
По структуре дисперсные системы различают:
свободные дисперсные системы, когда частицы обеих составляющих системы могут свободно перемещаться друг относительно друга (золь);
связанные дисперсные системы, когда одна из составляющих системы представляет собой структурированную систему, т.е. частицы фазы жестко связаны между собой (студень, композиты).
Таблица 1.1.1.1

