
1.2 Свойства аминопиридинов
2- и 4-аминопиридины способны к таутомерному превращению соответственно в 2- и 4-пиридонимины, однако, в обычных условиях существуют практически в аминной форме, например:

Моноаминопиридины обладают многими. свойствами первичных аминов. При взаимодействии 2-аминопиридина с алкилирующими агентами (алкилгалогенидами, алкилсульфатами или диазометаном) алкилируется в первую очередь кольцевой атом N. В присутствии NaNH2 образуется 2-алкиламинопиридин. Дальнейшим алкилированием получают диалкиламинопиридины.Существенное различие в химических свойствах изомерных моноаминопиридинов проявляется в их реакциях с HNO2: 3-аминопиридин диазотируется с образованием солей диазония, 2- и 4-аминопиридины образуют в слабокислом растворе гидроксипиридины (пиридоны), а в присутствии концентрированной соляной кислоты - хлорпиридины. Соли диазосоединений из 2-аминопиридина получают по реакции[19]:

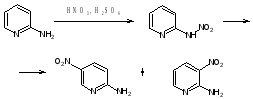
Моноаминопиридины реагируют с сильными электрофилами, восстанавливаются в производные пиперидина. Аминогруппа компенсирует дезактивирующий эффект атома N пиридина и ориентирует замещение в кольце. Если аминогруппа находится в положении 2, 3 или 4, то электрофильное замещение происходит соответственно в положения 5, 2 или 3 (5). При действии на 2-аминопиридин нитрующей смеси образуется нитрамин, который в присутствии H2SO4 изомеризуется в смесь 5-нитро- и З-нитро-2-аминопиридинов с выходами соотв. 80 и 10%[20]:
Особого внимания заслуживает взаимодействие аминопиридинов с трифенилфосфином в присутствии диэтилазодикарбоксилата. Реакция служит эффективным способом синтеза арилиминофосфоранов. Процесс протекает при обычных условиях и комнатной температуре.[21]

2. Обсуждение результатов
Нами был осуществлен трехстадийный синтез по схеме:

3. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
3.1 Реагенты
|
Название |
Формула |
Масса, г |
Объем, мл |
Количество вещества, моль |
|
Пиридин |
С5H5N |
- |
10 |
0.092 |
|
Тионилхлорид |
SOCl2 |
- |
18.3 |
0.0184 |
|
Соляная кислота |
HCl |
- |
10 |
0.370 |
|
Метанол |
CH3OH |
- |
7 |
0.027 |
|
Аммиак |
NH3 |
- |
18.5 |
0.420 |
|
Гидроксид натрия |
NaOH |
1.65 |
- |
0.006 |
|
Бензол |
C6H6 |
- |
16.5 |
0.028 |
|
Толуол |
C7H9 |
- |
10 |
0.084 |
3.2 Синтез целевых продуктов
3.2.1 Получение 1-пиридин-4-пиридиния
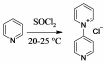
В трёхгорлой колбе, емкостью 250 мл, снабженной капельной воронкой, мешалкой, обратным холодильником, при энергичной работе мешалки смешивают 10 мл сухого пиридина и 30 г) тионилхлорида (технического продукта), поддерживая t=+20°C.
После полного прибавления тионилхлорида реакционная смесь оставляется при комнатной температуре на 3 дня. Затем, тионилхлорид отгоняется в вакууме, причем температура водяной бани постоянно повышается до кипения, и при этой температуре содержимое колбы выдерживается дополнительно 2 часа.
Оставшийся в колбе сухой остаток при кипячении примерно с 7 мл сухого метанола превращается в гомогенную кристаллическую кашу, которую отсасывают после охлаждения до 0°C. Промытый небольшим количеством спирта сырой продукт после высушивания при 110°С имеет температуру плавления 145-148°С. Выход 3,5г(31% от теоретического). Для дальнейшей очистки сырой продукт растворяют в небольшом количестве 2н. HCl, отфильтровывают и обрабатывают фильтрат активным углем несколько раз. После упарки в вакууме и прибавления спирта выделяются почти белые кристаллы, которые после охлаждения отсасывают и высушивают. Окончательная перекристаллизация из метанола дает почти бесцветные кристаллы с температурой плавления 151°С.
