
- •Лу́жні мета́ли — елементи головної підгрупи першої групи періодичної системи. Назва пов'язана з
- •Комплексонометрія (трілонометрія) - титриметричний метод, заснований на реакціях утворення
- •Завдання 2
- •Завдання 2
- •Завдання 2
- •Завдання 2
- •Завдання 2
- •Максимальне значення валентності елемента збігається з номером групи періодичної системи, у якій він
- •Завдання 2
- •Завдання 2
- •Завдання 2
- •Завдання 2
- •Завдання2
Завдання 2
-
Максимальне значення валентності елемента збігається з номером групи періодичної системи, у якій він
розміщений. Проте трапляються і винятки - Нітроген, Оксиген, Флуор, Купрум тощо. Номер групи позначено римською цифрою над відповідним вертикальним стовпчиком періодичної системи.
Група періодичної системи — хімічні елементи, розташовані в одному стовпці періодичної системи елементів і характеризуються подібністю хімічних власивостей завдяки спільним рисам у електронній конфігурації атомів.
Існує 18 груп, які IUPAC з 1989 року рекомендує номерувати арабськими цифрами: група 1, група 2 тощо. Така нумерація була запропонована для того, щоб уникнути плутанини попередніх систем. В цих системах групи нумерувалися римськими цифрами, але ця нуменрація була різною в Європі і США.
-
ДОБУТОК РОЗЧИННОСТІ (ДР, КS) — добуток рівноважних концентрацій іонів у насиченому розчині
малорозчинного сильного електроліту. Показники ступеня для концентрацій, які входять у ДР, дорівнюють стехіометричним коефіцієнтам у рівнянні дисоціації електроліту.
У загальному вигляді вираз ДР для малорозчинної речовин Кх Ау, що розпадається на іони за рівнянням Кх Ау = х Ку+ + у Ах–, має вигляд ДР Кх Ау = [ Ку+] х ⋅ [А х–] у.
Значення ДР малорозчинних у воді сполук визначають за допомогою електрохімічних методів: шляхом вимірювання електрорушійної сили або за електропровідністю насичених розчинів.
-
Манга́н, ма́рганець (Mn) – хімічний елемент з атомним номером 25. Метал, який відповідає цьому елементу —
марганець.
Сполуки мангану широко використовують при виробництві скла, оліфи і в гальванічних елементах (піролюзит), в медицині (перманганат калію), у фарбувальній справі (хлорид і сульфат мангану).
В-11
Завдання 1
-
Комплексні сполуки — це сполуки, до складу яких входять комплексні частинки (комплекси), що вміщують
центральний атом (комплексоутворювач) оточений лігандами. Утворення комплексів можна представити як результат взаємодії за донорно-акцепторним механізмом стабільних при звичайних умовах частинок: атомів, йонів або молекул.
Основна ідея координаційної теорії А. Вернера полягає у тому, що комплексна сполука, як структурний елемент вміщує комплексну частинку, що складається з центрального атома, який оточений певною кількістю лігандів.
Класифікація комплексних сполук:
-
за знаком заряду: катіонні, аніонні, нейтральні, бікомплексні.
-
За кількістю ядер: моноядерні, поліядерні.
Константа нестійкості є мірою міцності внутрішньої сфери, чим меншу величину має константа нестійкості, тим міцніший комплекс.
Завдання 2
-
В 1900 р. німецький фізик Планк висунув гіпотезу про квантовий характер випромінювання. Суть її полягала в наступному:
- випромінювання світла носить дискретний характер;
- поглинання відбувається теж дискретно-порціями, квантами.
Енергія кожного кванта представляється по формулі E=hn, де h – постійна Планка, а n – це частота світла.
3. Манга́н, ма́рганець (Mn) – хімічний елемент з атомним номером 25. Метал, який відповідає цьому елементу —
марганець.
Сполуки мангану широко використовують при виробництві скла, оліфи і в гальванічних елементах (піролюзит), в медицині (перманганат калію), у фарбувальній справі (хлорид і сульфат мангану).
В-12
Завдання 1
-
Якщо слабку основу титрують сильною кислотою, то точка еквівалентності також не збігається з точкою нейтральності і знаходиться в слабо-кислому середовищі. Це пов’язано з утворенням у результаті титрування солі, що містить катіон слабкої основи і аніон сильної кислоти, яка внаслідок гідролізу створює слабко-кисле середовище.
В такому випадку, коли pH= 4-6, можна застосувати метиловий оранжевий індикатор.
Завдання 2
-
Головне квантове число - ціле число, що позначає номер енергетичного рівня. Характеризує енергію електронів, що займають даний енергетичний рівень. Із зростаючим головним квантовим числом зростають радіус орбіти і енергія електрона. Головне квантове число позначається як n.
Найбільше число електронів на енергетичному рівні визначається за формулою N = 2n2.
-
Розчинність малорозчинного електроліту збільшується в присутності побічних електролітів, які не містять загальних іонів. Таке явище тримало назву солевого ефекту.
-
Ступінь окиснення -1
Позитивні ступені окислення у хлору також +4 і +6
Флуор в усіх сполуках має ступінь окиснення −1;
В-13
Завдання 1
Завдання2
-
Прото́н – єдина стабільна частинка з позитивним зарядом +е. Маса протона складає 1,00727663 а.о.м. або 938,2723 МеВ.
Електро́н— стабільна, негативно заряджена елементарна частинка, що входить до складу всіх атомів.Має електричний заряд (-е= −1,6021892(46)×10-19 Кл) і масу (9,109554(906)×10−31 кг).
Нейтро́н— елементарна частинка, яка входить до складу ядра.
Маса нейтрона приблизно дорівнює масі протона 1,6749543•10-24г = 1838,5 мас електрона.
-
Координаці́йне число— кількість атомів (йонів, молекул), найближчих до даного атома (йона, молекули) в
кристалі.
В алмазі координаційне число дорівнює 4, в кам'яній солі — 6. Координаційне число визначається природою і формою структурних частинок, характером і спрямованістю їх взаємодій, умовою мінімуму енергії системи.
Іноді задають координаційне число для другої, третьої і т. д. координаційної сфери.
В аморфних тілах і рідинах координаційне число має тільки статистичний зміст.
-
Mg і лужноземельні метали мають ступінь окиснення— (+2)
В-14
Завдання 1
-
Дисоціація слабких електролітів гальмується в присутності сильних електролітів, що утворюють однойменні iони. Так, сильна кислота гальмує дисоціацію слабкої кислоти, а сильна основа - слабкої основи). Слабкі електроліти мало впливають на дисоціацію сильних електролітів.
Процес дисоціації слабких електролітів є зворотнім і в системі існує динамічна рівновага, яку можна описати константою рівноваги.
Константу
дисоціації можна виразити таким
рівнянням:

Завдання2
-
l ― орбітальне квантове число, квантує момент імпульсу
Орбітальне квантове число набуває значень l=0,1,2,...
-
Ліганд— атом, йон або молекула, безпосередньо зв'язані з одним або декількома центральними (комплексоутворювальними) атомами металу в комплексній сполуці.
Число займаних лігандом координаційних місць центрального атома (або атомів), називається дентатностью.
-
Хром легко утворює сполуки, в яких він тривалентний або шестивалентний.
Метали підгрупи хрому при високій температурі здатні сполучатись з вуглецем і утворювати карбіди.
Хром найтвердіший з усіх металів.
В-15
Завдання 1
-
Рівняння електролітичної дисоціації кислот: HCl → H+ + Cl–
Приклад дисоціації солей: NaNO3 → Na+ + NO3–
Рівняння електролітичної дисоціації лугів: NaOH → Na+ + OH–
Ступінь дисоціації - доля дисоційованих молекул в електроліті.Позначається зазвичай α і є безрозмірною величиною.
Дисоціація слабких електролітів гальмується в присутності сильних електролітів, що утворюють однойменні iони. Слабкі електроліти мало впливають на дисоціацію сильних електролітів.
Константу
дисоціації можна виразити таким
рівнянням:
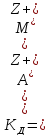
Закон розведення Оствальда — співвідношення, що виражає залежність еквівалентної електропровідності розведеного розчину бінарного слабкого електроліту від концентрації розчину.
