
- •В. Р. Зайлалова учебное пособие по курсу «химия нефти и газа»
- •Введение
- •1. Происхождение нефти
- •2. Элементарный состав нефти
- •3. Фракционный состав нефти
- •3.1. Детонационная стойкость горючего
- •3.2. Переработка углеводородного сырья
- •3.2.1. Переработка каменного угля
- •3.2.2. Перспективы развития энергетики
- •4. Групповой углеводородный состав нефти. Классификация нефти
- •5. Молекулярный вес
- •6. Физические свойства нефти
- •6.1. Плотность
- •6.2. Вязкость
- •6.3. Температурные переходы и агрегатные превращения
- •6.4. Тепловые свойства
- •6.5. Оптические свойства
- •6.6. Электрические свойства
- •7. Фазовое равновесие в системе «нефть — газ»
- •8. Классификация углеводородов
- •8.1. Предельные (насыщенные) углеводороды. Алканы (парафины)
- •Физические свойства
- •Химические свойства
- •Способы получения
- •8.2. Предельные углеводороды. Циклоалканы
- •Физические свойства
- •Химические свойства
- •Способы получения
- •8.3. Непредельные (ненасыщенные) углеводороды. Алкены (этиленовые углеводороды)
- •Физические свойства
- •Химические свойства
- •Способы получения
- •8.4. Непредельные углеводороды. Алкадиены
- •Химические свойства
- •Способы получения
- •8.5. Непредельные углеводороды. Алкины (ацетиленовые углеводороды)
- •Физические свойства
- •Химические свойства
- •Способы получения
- •8.6. Ароматические углеводороды. Бензол и его гомологи
- •Химические свойства
- •Свойства бензола
- •Свойства гомологов бензола
- •Способы получения
- •9. Неуглеводородные соединения нефти
- •9.1. Кислородные соединения
- •Азотистые соединения
- •Сернистые соединения
- •10. Смолистые вещества
- •11. Минеральные компоненты нефти
- •12. Методы выделения компонентов
- •12.1. Перегонка
- •12.2 Азеотропная и экстрактивная ректификация, экстракция, абсорбция
- •И селективность растворителей при 60°с
- •12.3. Адсорбция
- •12.4. Кристаллизация
- •12.5. Диффузионные методы разделения углеводородов
- •13. Природные и попутные газы. Применение газа
- •13.1 Природные газы
- •Попутные (нефтяные) газы
- •Применение газа
- •Термические превращения углеводородов нефти
- •14.1. Термодинамика процесса
- •14.2. Кинетика и механизм процесса
- •Энергия связи с—с, кДж/моль: 335; 322; 314; 310; 314; 322; 335
- •14.3. Термические превращения углеводородов в газовой фазе
- •Превращения алканов
- •14.3.2. Превращения циклоалканов
- •14.3.3. Превращения алкенов
- •Суммарную реакцию можно записать уравнением:
- •14.3.4. Превращения алкадиенов и алкинов
- •14.3.5. Превращения аренов
- •15. Термокаталитические превращения
- •15.1. Механизм действия катализаторов окислительно-восстановительного типа
- •15.2. Кислотный катализ
- •15.3. Реакции карбкатионов
- •15.4. Каталитический крекинг
- •15.4.1. Превращения алканов
- •15.4.2. Превращение циклоалканов
- •15.4.3. Превращение алкенов
- •15.4.4. Превращение аренов
- •15.4.5. Катализаторы каталитического крекинга
- •15.4.6. Каталитический крекинг в промышленности
- •15.5. Каталитический риформинг
- •15.5.1. Химические основы процесса
- •15.5.2. Катализаторы риформинга
- •15.5.3. Каталитический риформинг в промышленности
- •16. Гидрогенизация в нефтепереработке
- •16.1. Классификация процессов
- •16.2. Классификация каталитических реакций с водородом
- •16.3. Термодинамика и катализаторы гидрирования
- •Список литературы
- •Содержание
15.3. Реакции карбкатионов
Изомеризация. Изомеризация карбкатионов может происходить в результате переноса как гидрид-иона, так и метиланиона:
+ + +
CH2 CH CH2 CH2 CH3 CH3 CH CH CH2 CH3 CH3 CH2 CH CH2 CH3
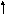 ••
••
••
••


 Н
Н
Н
Н
+ + +
C H3CHCH2:CH3
CH3CHCH2
CH3CCH3+
76 кДж/моль
H3CHCH2:CH3
CH3CHCH2
CH3CCH3+
76 кДж/моль
 |
|
|
|
 CH3
CH3
CH3
CH3
Подобное перемещение происходит быстро в направлении от первичного иона карбония к вторичному и далее к наиболее устойчивому — третичному.
Распад по β-правилу. Расщепление карбкатионов обычно происходит по наиболее слабой связи β-С—С. Реакция эндотермична:
+
CH2 CH2 CH2 CH2 CH2 CH2 CH2 CH3
+
CH2=CH2 + CH2 CH2 CH2 CH2 CH2 CH3— 92 кДж/моль
Склонность к распаду снижается при переходе от первичного иона к вторичному и от вторичного к третичному. Если для распада первичного октилкатиона требуется 92 кДж/моль, то для вторичного октилкатиона надо затратить 176 кДж/моль.
Склонность к распаду возрастает при отщеплении вторичного иона и — еще в большей степени — третичного:
+
CH3 CH2 CH CH2 C(CH3)2 CH2 CH3
+
CH3CH2CH=CH2 + C(CH3)2CH2CH3- 21 кДж/моль
Сопоставление энергетики распада и изомеризации карбкатионов показывает, что изомеризация должна предшествовать в большинстве случаев распаду. Преимущественное образование третичных карбкатионов и их устойчивость должны приводить к накоплению изоструктур при распаде неразветвленных алкильных карбкатионов с большим числом углеродных атомов.
Присоединение карбкатионов к алкенам и аренам. Эта реакция обратна реакции распада карбкатионов:
+ CH3 +
|
(CH3)3C + CH2=CCH3 (CH3)3CCH2C(CH3)2
+
(CH3)3C
+ C6H6
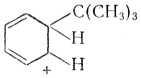
Поэтому характер изменения теплового эффекта противоположен реакции распада.
Потеря протона смежным углеродным атомом и передача протона молекуле алкена. Например:
+
СН3СН2СНСН3 СН3СН=СНСН3 + Н+
+
СН2СН(СН3)СН3 + СН3СН=СНСН3
+
СН2=С(СН3)СН3+СН3СНСН2СН3 + 42 кДж/моль
Наиболее энергетически выгодна такая реакция, когда протон отщепляется от первичного карбкатиона, а в результате образуется третичный карбкатион.
Отрыв гидрид-иона от молекулы углеводорода. Например:
+
СН3СНСН2СН3 + СН3СН(СН3)СН3
+
СН3СН2СН2СН3 + СН3С(СН3)СН3 + 67 кДж/моль
Активность карбкатиона в реакции отрыва гидрид-иона от молекулы углеводорода также снижается в ряду:
R+перв > R+втор > R+трет
Карбкатионные реакции всегда протекают или в жидкой фазе, или на поверхности твердого катализатора. Сольватация в растворе и адсорбция при реакции на твердой поверхности значительно изменяют тепловые эффекты реакции ионов. В результате соотношения между различными реакциями ионов в реальных процессах могут существенно отличаться от расчетных.
