
- •Министерство образования и науки Российской Федерации
- •Основы общей химии
- •Глава 1 Первоначальные понятия химии
- •1.1. Предмет химии
- •1.2. Атомно-молекулярное учение
- •1.3. Основные понятия химии
- •1.3.1. Простые и сложные вещества
- •1.3.2. Атомная и молекулярная массы
- •1.3.3. Моль, молярная масса, молярный объем
- •1.3.4. Связь между массой вещества и его количеством
- •1.3.5. Связь между объемом вещества и его количеством
- •1.3.6. Валентность, степень окисления
- •1.4. Уравнения химических реакций
- •2 Моль атомов н - 1 моль молекул н2,
- •1.5. Вопросы для самоконтроля по теме
- •1.6. Примеры комплексных тестов для самоконтроля знаний по теме «Первоначальные понятия химии» Вариант № 1
- •1. 17, 2. 35,5, 3. 71 Г/моль, 4. 71 г, 5. 71?
- •Вариант № 2
- •1. 0,233, 2. 233, 3. 233 Г/моль, 4. 104, 5. 233 г.
- •Вариант № 3
- •1.7. Тесты и задачи для самоподготовки по теме
- •1) Воздух, 2) речная вода, 4) хлорид меди (II), 8) нефть,
- •16) Природный газ, 32) раствор соляной кислоты*.
- •1) Гашеная известь**, 2) соляная кислота, 4) резина, 8) квасцы**, 16) хлорная вода**
- •1) Мел, 2) пирит*, 4) цемент, 8) бензол, 16) глюкоза.
- •1)Гидроксид натрия, 2) оксид фосфора (V), 4) гашеная известь**,
- •8) Бензин, 16) сахароза.
- •1.7.3. Простые и сложные вещества
- •1) В состав нитрата железа входят железо, азот и кислород,
- •1) Молекула водорода, состоящая из двух атомов, 2) две молекулы водорода, 4) два атома водорода, 8) два моль атомов водорода, 16) два моль молекул водорода.
- •1) Имеет размерность г/моль, 2) численно равна значению молярной массы элемента, 4) равна отношению массы атома к массе 1 а.Е.М,
- •8) Может быть выражена в граммах, 16) может быть выражена в атомных единицах массы, 32) является безразмерной величиной.
- •1.7.5. Валентность, степень окисления
- •1.7.6. Расчеты по химическим формулам
- •1.7.7. Моль – единица измерения количества вещества
- •6,02·10 23 Атомов Cu – 64 г,
- •1 Атом Cu – х г;
- •1) 34 Г, 2) 34 г/моль, 4) 1,99 · 1022, 8) 34 а.Е.М., 16) 5,65 · 1023 г.
- •1.7.8. Ответы к комплексным заданиям для тестирования знаний по теме «Первоначальные понятия химии» Вариант № 1
- •Вариант № 2
- •Вариант № 3
- •6,02 ·1023 Молекул 98 г,
- •10 Молекул х г;
1.7.8. Ответы к комплексным заданиям для тестирования знаний по теме «Первоначальные понятия химии» Вариант № 1
Задание 1. Ответ 3.
Простыми веществами, то есть веществами, состоящими из атомов только одного элемента, являются: железо, сера и графит.
Задание 2. Ответ 4.
2Н2О.
Задание 3. Ответ 71.
Мr(С12) = 2Аr (С1) = 2 ∙ 35,5 = 71.
Задание 4. Ответ 1.
Количество вещества, определяемое по формуле
ν = m/M,
при одинаковой массе вещества будет тем больше, чем меньше значение молярной массы вещества. Меньшее значение имеет молярная масса водорода.
Задание 5. Ответ 3.
Сплав массой 100 г содержит 60 г меди и 40 г цинка. Найдем количества каждого вещества в молях, содержащихся в указанных массах веществ:
ν(Сu) = m(Cu) / M(Cu) = 60/64 = 0,938
ν(Zn) = m(Zn) / М(Zn) = 40/65 = 0,615,
откуда ν(Cu) / ν(Zn) =1,525.
Вариант № 2
Задание 1. Ответ 2.
Задание 2. Ответ 3.
Среди приведенных веществ металлами являются: магний, кальций, олово.
Задание 3. Ответ 233.
Относительная молекулярная масса определится как сумма относительных атомных масс:
Мr (ВаSO4) = Аr (Ва) + Аr (S) + 4Аr (O) =
= 137 + 32 + 4 · 16 = 233.
Задание 4. Ответ 1.
1,66·1024 г. Атомная единица массы 1/12 часть массы атома соответствующего изотопа углерода, то есть а.е.м. = 1/12·1,99·1024 г. = = 1,66 · 1023 г.
Задание 5. Ответ 4.
С3Н6О. Зная качественный состав вещества, обозначим его формулу СхНуОz. Учитывая, что число молей атомов равно
ν = m/M,
разделив значение массы каждого элемента на величину его молярной массы, перейдем от отношения масс к отношению количеств вещества (моль атомов) или отношению атомов в молекуле:
x
: у : z
= ν(C)
: ν(H)
: ν(O)
=
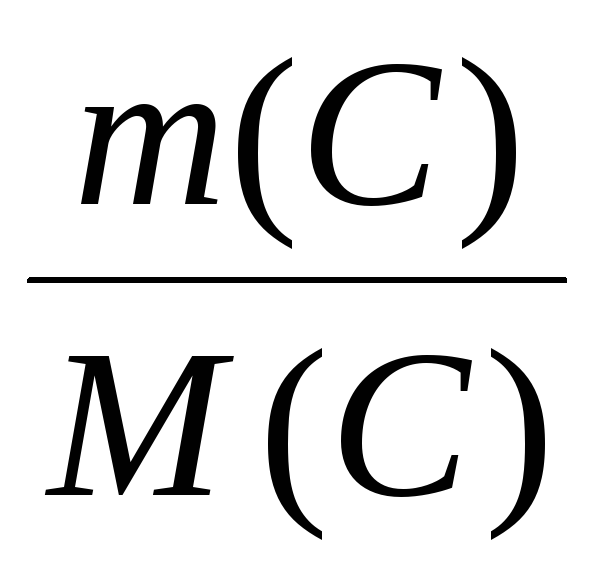 :
:
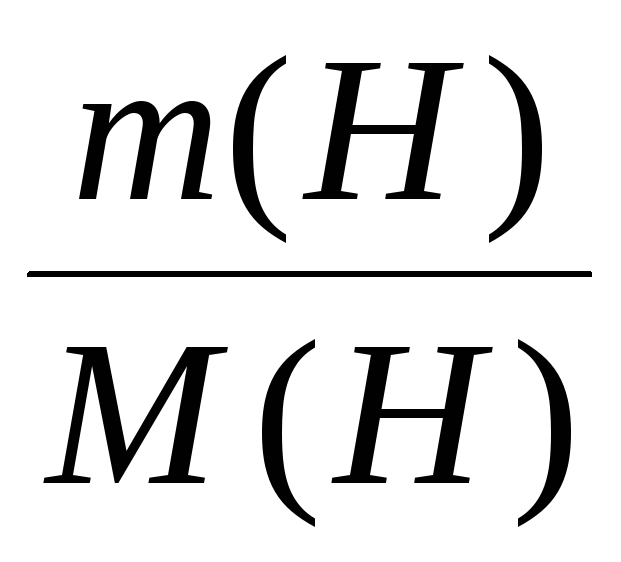 :
:
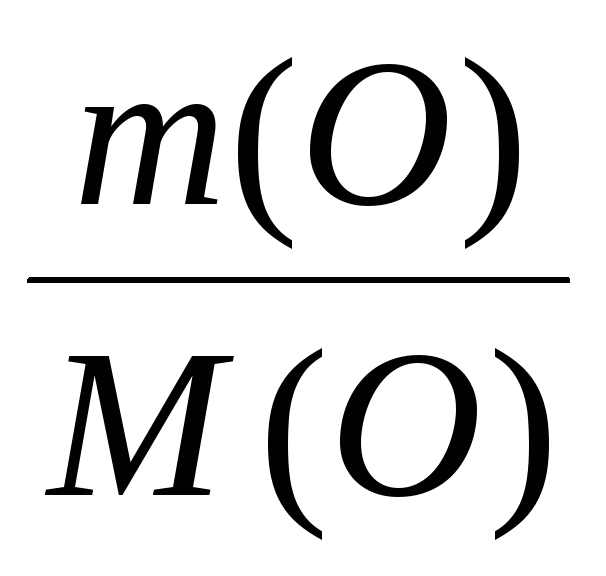 =
=
![]() :
:
![]() :
:
![]() = 1,5 : 3 : 0,5, или, переходя к целым числам,
= 1,5 : 3 : 0,5, или, переходя к целым числам,
ν (С) : ν (H) : ν (O) = 3 : 6 : 1.
Простейшая формула вещества С3Н6О.
Вариант № 3
Задание 1. Ответ 4.
Веществами (или смесями различных веществ) являются вода, сахар, бензин и железо.
Задание 2. Ответ 4.
Признаками химических реакций, из числа приведенных, являются: образование осадка, выделение газообразного вещества, изменение окраски, появление запаха.
Задание 3. Ответ 1.
1 : 6 : 8. Учитывая, что в состав 1 молекулы СН3СООН входят 4 атома элемента водорода, 2 атома элемента углерода, и 2 атома элемента кислорода, имеющие массы 2Аr (С), 4Аr (Н) и 2Аr (O), то есть отношение масс:
m (Н) : m (С) : m (O) = 4 : 24 : 32, или
m (Н) : m (С) : m (O) = 1 : 6 : 8.
Задание 4. Ответ 1.
1,63·1023. Учитывая, что 1 моль молекул серной кислоты
(6,02∙1023 молекул) имеют массу, равную молярной массе
М (H2SO4) = 98 г/моль, составим пропорцию:
6,02 ·1023 Молекул 98 г,
10 Молекул х г;
x = 98·10/6,02·1023 = 1,63·1021.
Задание 5. Ответ 1. 91,4%.
Найдем значение относительной молекулярной массы Н2S:
Мr(Н2S) = 2Аr (Н) + Аr (S) = 2 + 32 = 34.
Моль молекул сероводорода имеет массу 34 г. В одном моль молекул сероводорода содержится моль атомов серы и два моль атомов водорода. Относительная атомная масса серы Аr(S) = 32, а масса одного моль атомов серы равна 32 г. Массовая доля серы в сероводороде равна:
ω
= ![]() ·100% = 32/34 · 100% = 0,941 ·
100% = 94,1%.
·100% = 32/34 · 100% = 0,941 ·
100% = 94,1%.
