
- •1) Теория строения органических соединений а.М. Бутлерова
- •2) Электронное строение атома углерода в составе молекул органических соединений. Гибридизация атомных орбиталей. Типы гибридизации атомных орбиталей углерода в молекулах органических соединений.
- •3) Электронное строение атома кислорода в составе молекул органических соединений. Гибридизация атомных орбиталей. Типы гибридизации атомных орбиталей кислорода в молекулах органических соединений.
- •4)Электронное строение атома азота в составе молекул органических соединений. Гибридизация атомных орбиталей. Типы гибридизации атомных орбиталей азота в молекулах органических соединений.
- •5) Химическая связь в молекулах органических в-в. Сигма и пи-связи: способы образования. Основные характеристики.
- •6) Пространственное строение. Конформация и конфигурация как способы описания пространственного строения молекулы.
- •7) Структурная изомерия.
- •8) Пространственная изомерия
- •9) Электронные эффекты: индуктивный и мезомерный. Понятие о резонансе. Электродонорные и электроноакцепторные заместители.
- •10) Классификация р-ций и реагентов в орган. Химии. Механизмы р-ций в орг.Химии.
- •11. Основные принципы классификации органических соединений. Гомологический ряд. Функциональная группы. Основы номенклатуры орган.Соед.
- •12) Предельные углеводороды. Строение молекул алканов и циклоалканов. Методы получения предельных углеводородов.
- •13) Химические св-ва предельных углеводородов. Радикальный механизм р-ций замещения в алканах. Селективность р-ций замещения. Особенности хим. Св-в малых циклов.
- •14) Непредельные углеводороды. Строение молекул алкенов и алкинов. Методы получения непредельных углеводородов.
- •15) Химические св-ва алкенов: р-ции электрофильного присоединения. AdE и реакции окисления.
- •16) Химические свойства алкинов: р-ции электрофильного присоединения AdE, замещения, окисления.
- •17) Алкадиены. Особенности электронного строения с сопряженными двойными связями. Особенности хим. Св-в сопряженных алкадиенов: 1,2-присоед, 1,4-присоед.
- •18)Ароматические углеводороды. Современные представления о представлении молекулы бензола. Гомологический ряд бензола: изомерия и номенклатура. Методы синтеза гомологов.
- •20) Гидроксильные соединения: спирты и фенолы. Строение функциональной группы. Водородная связь и ее влияние на физ.Св-ва гидроксильных соед. Методы получения гидрокс. Соединий.
- •21) Общая хар-ка хим. Св-в одноатомных спиртов. Р-ции с разрывом связи с-он и он. Хим.Особенности первичных, вторичных и третичных спиртов.
- •22)Особенности хим.Св-в многоатомных спиртов на примере этиленгиколя и глицерина.
- •23) Фенолы. Строение функциональной группы. Общая хар-ка хим.Св-в. Влияние заместителей на кислотность фенолов.
- •25) Хим. Св-ва карбонильных соед. Р-ции нуклеофильного присоединения. Р-ции замещения в углеводородном скелете. Окисление карбонильных соединений.
- •27) Химические свойства карбоновых кислот. Зависимость кислотных свойств от строения молекулы. Получение функциональных производных карбоновых кислот.
- •28) Простые и сложные эфиры. Методы получения. Общая характеристика физических и химических свойств простых и сложных эфиров.
- •29) Амины. Строение функциональной группы. Первичные, вторичные и третичные амины. Водородная связь и ее влияние на физические свойства аминов. Методы получения аминов.
- •30) Химические свойства аминов и их химическая идентификация. Зависимость основности аминов от строения молекулы.
- •32) Белки. Химические свойства белков. Гидролиз. Цветные реакции.
- •33) Глицериды. Классификация глицеридов. Животные жиры и растительные масла: общая характеристика физических и химических свойств.
- •34) Углеводы. Моносахариды. Классификация и номенклатура моносахаридов. Стереоизомерия. Проекционные формулы Фишера. D- и l-моносахариды. Кольчато-цепная таутомерия. Перспективные формулы Хеуорса.
- •35) Химические свойства моносахаридов.
- •36)Углеводы. Дисахариды. Восстанавливающие и невосстанавливающие дисахариды.
- •37) Углеводы. Полисахариды. Крахмал и целлюлоза: структура и химические свойства.
13) Химические св-ва предельных углеводородов. Радикальный механизм р-ций замещения в алканах. Селективность р-ций замещения. Особенности хим. Св-в малых циклов.
Алканы проявляют свою реакционную способность в основном в реакциях замещения.
Радикальный механизм.
Р-ция галогенирования
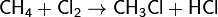

Р-ция замещения
у алканов селективны: легче всего идет
замещение водорода третичного атома
углерода, труднее у вторичного, еще
труднее у первичного, у четвертичного
нечего замещать. Селективность р-ций
снижается с увел. активности галогенов
и температуры. 2) Р-ции нитрования (при
температуре 140 °C и небольшом давлении)![]() 3)Р-ции окисления. Алканы при обычных
условиях не обесцвечивают водный растворKMnO4. Это может служить
качественной реакцией на алканы.
3)Р-ции окисления. Алканы при обычных
условиях не обесцвечивают водный растворKMnO4. Это может служить
качественной реакцией на алканы.
а) Горение
![]() При
недостатке кислорода обр-ся продукты
неполного окисления – угарный газ и
сажа, что характерно для высших алканов.
б) Дегидрирование. Условия протекания:
400—600 °C, катализаторы — Pt, Ni, Al2O3,
Cr2O3, например, образование
этилена из этана. Строение продуктов
зависит от условий проведения реакций
и от длины цепи исходного алкана. От 2
до 4:
При
недостатке кислорода обр-ся продукты
неполного окисления – угарный газ и
сажа, что характерно для высших алканов.
б) Дегидрирование. Условия протекания:
400—600 °C, катализаторы — Pt, Ni, Al2O3,
Cr2O3, например, образование
этилена из этана. Строение продуктов
зависит от условий проведения реакций
и от длины цепи исходного алкана. От 2
до 4:![]() .
5 атомов: 5-ти членный цикл. От 6: образование
бензола.
.
5 атомов: 5-ти членный цикл. От 6: образование
бензола.![]()
Р-ция электрофильного замещения (изомеризация).
Хим. св-ва циклоалканов. Малые циклы – циклопропан и циклобутан.
1) Р-ции присоединения (малые циклы) Циклопропан и циклобутан способны присоединять бром. Циклопропан и его производные способны обесцвечивать бромную воду (качественная р-ция на малые циклы):
С3H6+ Br2→ BrCH2—CH2—CH2Br
Наличие электродонорных заместителей в цикле способствует протеканию р-ций, сопровождающихся раскрытием цикла; электроакцепторных – затрудняет их протекание.
2)Р-ции замещения (все, что и алканов). Наиболее характерны для «больших циклов» (от С5 и более протекает по механизму радикального замещения SR).
14) Непредельные углеводороды. Строение молекул алкенов и алкинов. Методы получения непредельных углеводородов.
Непредельные углеводороды - это углеводороды, содержащие кратные связи в углеродном скелете молекулы. Алкены CnH2n - алифатические непредельные углеводороды, молекулы которых содержат одну двойную связь. Атомы углерода связаны двойной связью, находятся в sp2-гибридном состоянии.
Методы:
1)Р-ции элиминирования. Правило Зайцева:
отщепление атома водорода в реакциях
элиминирование происходит преимущественно
от наименее гидрированного атома. а)
Дегидрогалогенирование галогеналканов
(спирт,
температура)![]() б)Дегидратация спиртов (при
повышенной температуре в присутствии
сильных минеральных кислот):
б)Дегидратация спиртов (при
повышенной температуре в присутствии
сильных минеральных кислот):
![]()
в)
Дегалогенирование вицинальных (рядах)
дигалогеналканов (цинк, спирт)
![]()
г)
Дегидрирование алканов (температура,
катализатор):
![]()
Алкины– алифатические непредельные углеводороды, молекулы которых содержат одну тройную связь С-С.
CnH2n-2.Атомы углерода, связанные тройной связью, нах-ся вsp-гибридном состоянии.
1)Гидролиз карбида кальция.
![]() 2) Дегидрогалогенирование вицинальных
и геминальных дигалогеналканов (протекает
в соответствии с правилом Зайцева).
2) Дегидрогалогенирование вицинальных
и геминальных дигалогеналканов (протекает
в соответствии с правилом Зайцева).![]()
3) Алкилирование ацетиленидов (удлинение цепи)
