
- •Оглавление
- •2 Электрохимические системы
- •2.1. Определение электрохимической системы
- •2.2. Прохождение электрического тока в электрохимической системе. Законы фарадея
- •2.3. Термодинамически обратимые и необратимые электрохимические системы
- •2.4. Классификация термодинамически обратимых электрохимических систем
- •2.5. Составляющие электрохимической системы
- •2.6. Идеальные и реальные электрохимические системы
- •3 Метод активности
- •3.1. Формальный метод активности льюиса
- •3.2. Расчет коэффициента активности по дебдш и хюккелю
- •3.3. Расчет коэффициента активности по робинсону и стоксу
- •3.4. Эмпирические способы расчета коэффициентов активности
- •4 Ионные равновесии
- •4.1. Ионные равновесия в растворах электролитов
- •4.2. Сольволиз и буферные свойства
- •4.3. Константы образования комплексных ионов
- •4.4. Ступенчатая диссоциация электролитов
- •4.5. Ионные равновесия в растворах электролитов в присутствии твердой фазы
- •5 Процессы переноса в электрохимических системах
- •5.1. Электрическая проводимость
- •5.1.1. Электронная проводимость
- •Ионная проводимость
- •Электрическая проводимость газов
- •5.1.2.2. Электрическая проводимость твердых тел
- •5.1.2.3. Электрическая проводимость расплавленных соединений
- •5.1.2.4. Электрическая проводимость растворов
- •5.1.3. Теории электрической проводимости растворов
- •5.1.3.1. Простая гидродинамическая теория
- •5.1.3.2. Теория дебая – хюккеля – онзагера
- •5.1.3.3. Теория эйринга
- •5.1.3.4. Протолитическая теория электролитической проводимости
- •5.1.3.5. Применение средней ионной активности для расчета проводимости
- •5.2. Диффузия в растворах электролитов
- •5.3. Диффузионный, или жидкостный, потенциал
- •5.4. Конвективный перенос в растворах
- •5.5. Термодиффузия
- •6. Напряжение электрохимических систем
- •6.1. Возникновение напряжения в электрохимической системе
- •6.2. Равновесные потенциалы на границах раздела фаз
- •6.3. Уравнения равновесного электродного потенциала
- •6.4. Влияние температуры на электродный потенциал
- •6.5. Выбор относительной шкалы потенциалов
- •6.6. Электроды сравнения
- •6.7. Правило лютера
- •6.8. Термодинамическое равновесие с растворителем
- •6.9. Расчет напряжения электрохимических систем с помощью потенциалов в относительной шкале
- •6.9.1. Напряжение электрохимических систем с химической реакцией
- •Напряжение электрохимических систем без химической реакции
- •Напряжение электрохимических систем без химической реакции
- •6.10. Методы устранения диффузионного потенциала
- •4,2 Кмоль/м3 20,4 кмоль/м3
- •6.11. Термодинамика электрохимических систем
- •6.12. Ионоселективные электроду
- •6.12.1. Уравнение мембранного потенциала
- •6.12.2. Электроды с твердыми ионитовыми мембранами
- •6.12.3. Электроды с жидкими ионитовыми memбpahaми
- •6.12.4. Измерение напряжения электрохимических систем с ионоселективными электродами
- •7 Двой ной электрический слой
- •Явления адсорбции при образовании двойного электрического слоя
- •Злектрокапиллярные явления на ртути и твердых металлах
- •7.3. Емкость двойного электрического слоя
- •7.3.1. Влияние специфической адсорбции ионов на поверхностное натяжение и емкость двойного электрического слоя
- •7.3.2. Заряжение емкости двойного электрического слоя
- •7.4. Теории строения двойного электрического слоя
- •7.5. Двойной слой на твердых электродах
- •7.6. Двойной слой на электродах в расплавленных и твердых электролитах
- •%(%8 Кинетика электродных процессов
- •8.1. Поляризационные кривые
- •8.2. Перенапряжение электрохимической стадии
- •8.2.1. Уравнение поляризационной кривой без учета специфической адсорбции и ψ’-потенциала
- •Влияние ψ’-потенциала на скорость реакции разряда — ионизации
- •8.2.3. Стандартная константа скорости реакции переноса электрона и стандартная плотность тока обмена
- •8.2.4. Способы определения коэффициентов переноса из поляризационных кривых
- •8.3. Стадийные электродные реакции
- •8.4. Электрохимические реакции, включающие быстрые химические стадии
- •8.5. Определение порядков электрохимических реакций
- •8.6. Безбарьерные и безактивациониые электрохимические реакции
- •8.7. Кинетика реакций при конечных степенях заполнения поверхности
- •9 Диффузионная кинетика
- •9.1. Перенапряжение диффузии
- •9.2. Перенапряжение диффузии с учетом миграции
- •9.3. Поляризационные кривые при замедленной стадии диффузии
- •9.4. Окислительно-восстановительные реакции
- •9.5. Сложные окислительно-восстановительные реакции
- •9.6. Наложение перенапряжения диффузии и замедленного переноса электронов (смешанная кинетика)
- •10 Перенапряжение химической реакции
- •10.1. Перенапряжение, обусловленное предшествующей гомогенной химической реакцией в катодном процессе и последующей химической реакцией в анодном процессе
- •10.2. Общий случай электрохимической реакции с замедленной гомогенной химической стадией
- •10.3. Перенапряжение, обусловленное гетерогенными химическими стадиями
- •10.4. Зависимость плотности тока от концентрации и порядок химической реакции
- •11 Примеры различных механизмов электрохимических реакций
- •11.1. Реакция выделения водорода
- •11.2. Кинетика реакций в расплавах и твердых электролитах
- •12 Кинетика реакций электрохимического выделения металлов
- •12.1. Кинетика реакций выделения металлов на жидких катодах
- •12.2. Кинетика реакций при электроосаждении металлов на твердых электродах
- •12.3. Влияние поверхностно-активных веществ на рост кристаллов
- •12.4. Влияние природы металла и состава раствора на кинетические параметры
- •12.5. Электроосаждение металлов из расплавов
- •12.6. Электрохимическое восстановление оксидов
- •13 Анодное растворение и пассивность металлов
- •13.1. Анодное растворение металлов
- •13.2. Пассивность металлов
- •13.2.1. Теория пассивности
- •13.2.2. Кинетика процесса пассивирования
- •14 Короткозамкнутые электрохимические системы
- •14.1. Общие положения
- •14.2. Электрохимическая коррозия
- •14.2.1. Скорость коррозии металла и коррозионный потенциал
- •14.2.2. Растворение металлов под током в коррозйонноактивных средах
- •14.2.3. Коррозия технических металлов
- •14.2.4. Способы снижения скорости коррозионного процесса
- •14.3. Контактное вытеснение металлов (цементация)
- •14.3.1. Общие положения
- •14.3.2. Кинетика процесса цементации
- •14.3.3. Конечный период цементации
- •15 Параллельные электрохимические реакции
- •15.1. Условия протеканий параллельных реакций
- •15.2. Распределение плотности тока между параллельными реакциями
- •16 Основы методов исследования электрохимических реакций
- •16.1. Общие требования к методам исследования
- •16.2. Электроды, применяемые в кинетических исследованиях
- •16.3. Измерение потенциалов под током
- •16.4. Методы исследования
- •Литература
4.2. Сольволиз и буферные свойства
Наличие, хоть и очень небольших, концентраций ионов, образующихся при диссоциации растворителя, приводит к их взаимодействию с ионами растворенных в данном растворителе веществ и возникновению новых ионных равновесий. Это явление в общем случае называется сольволиз, а если растворитель — вода, то гидролиз. Допустим, что мы растворили в воде соль слабой кислоты и сильного основания, например, ацетат натрия. Тогда получим два равновесия:
CH3COONa = СН3СОO– + Na+
2H2O = H3O+ +OH–
Ацетат натрия в воде является сильным электролитом, т. е. распадается на ионы практически нацело. Между ионами в растворе возникает взаимодействие
Na+ + ОН– = NaOH
СНзСОO– + Н3О+ = СНзСООН + Н2О
Но щелочь является также сильным электролитом, так что первое из этих равновесий практически нацело сдвинуто влево. Уксусная кислота электролит слабый и, следовательно, ионы СН3СОО– и Н3О+ образуют в основном нейтральные молекулы. В результате этих двух реакций в растворе устанавливается равновесие
CH3COONa + Н2О = СН3СООН + Na+ + ОН–
и раствор будет иметь щелочную реакцию.
Если растворить в воде соль слабого основания и сильной кислоты, например сульфат железа (III), то можно записать следующие реакции равновесия
Fe2(SO4)3 = 2Fe3+ + 3SO42–
12H2O = 6H3O+ + 6OH–
Fe2 (SO4)3 + 12Н2О = 2Fe (OH)3 + 6Н3О+ + 3SO42–
т. е. реакция раствора будет кислая.
Из сказанного ясно, что в случае растворения в воде соли сильной кислоты и сильного основания нейтральная реакция среды должна сохраняться. Однако часто «силы» сильного основания и сильной кислоты не вполне одинаковы. Тогда раствор будет приобретать слабокислые или слабоосновные свойства.
Растворы, содержащие слабые кислоты и соли, образуемые этими кислотами и сильными основаниями, или содержащие слабыеоснования и соли, образуемые этими основаниями и сильными кислотами, обладают замечательным свойством противостоять изменению рН при добавлении к ним кислот или оснований. Это свой-ство называется буферным свойством, растворов, а растворы, обладающне им, — буферными растворами.
Вернемся к рассмотрению водного раствора, содержащего уксусную кислоту и ацетат натрия. Добавим к этому раствору сильное основание, например гидроксид натрия. Произойдет реакция нейтрализации NaOH слабой кислотой
СН3СООН + Na+ + ОН– = СН3СОO– + Na+ + Н2O
благодаря чему кислотность раствора практически останется не-изменной или изменится во много раз меньше, чем если бы мы добавили NaOH к раствору ацетата натрия.
Если же к буферному раствору добавить сильную кислоту, например соляную, то произойдет реакция с ацетатом натрия
СНзСОO– + Na+ + Н3О+ + Cl– = СН3СООН + Na+ + Сl– + Н2О
с образованием недиссоциированных молекул уксусной кислоты, т. е. с поглощением ионов гидроксония.
Изменение концентрации ионов гидроксония буферного раствора в результате добавки кислого или щелочного реагента рассчитывают следующим образом. Записывают константу равновесия для уксусной кислоты:
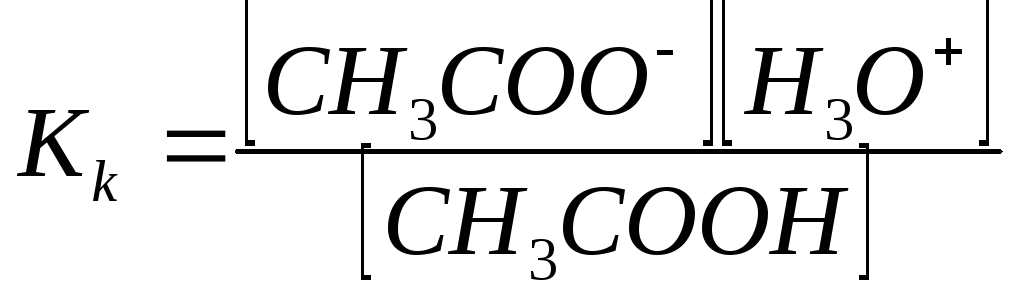
В Кk входит [Н2О]. В этом уравнении концентрация недиссоциированных молекул очень слабо диссоциирующей уксусной кислоты практически равна аналитической концентрации кислоты (Ск), а концентрация ацетат-ионов равна аналитической концентрации полностью диссоциирующего ацетата натрия (Сс). Тогда
[H3O+] = KkCk/Cc
В буферном растворе, содержащем хлорид аммония и аммиак, при добавлении кислоты происходит ее нейтрализация аммиаком
NH4ОН + Н3О+ + Cl– = NH4+ + Сl– + 2Н2О
а при добавлении щелочи гидроксид-ионы связываются ионами аммония в недиссоциирующие молекулы аммиака:
NH4+ + Сl– + Na+ + ОН– = NH4OH + Na+ + Сl–
Концентрация ионов водорода определяется из выражения для константы равновесия основания:
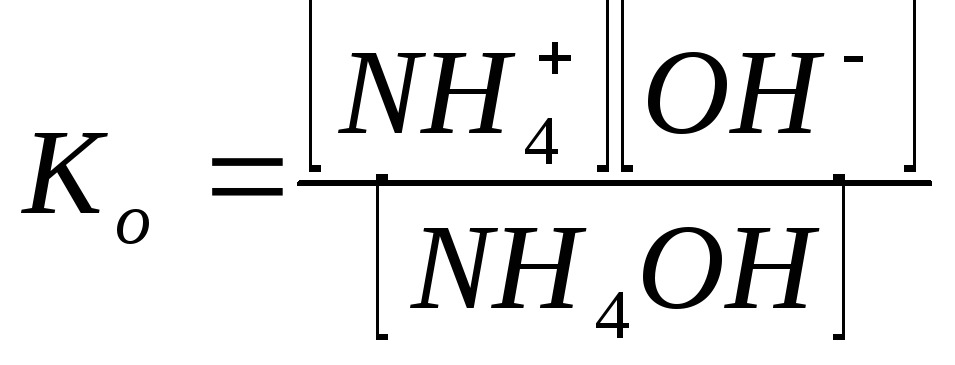
Поскольку в буферной смеси концентрацию недиссоциированных молекул аммиака можно считать равной аналитической концентрации аммиака (С0), а концентрацию NH4+ — аналитической концентрации хлорида аммония (Сс), то
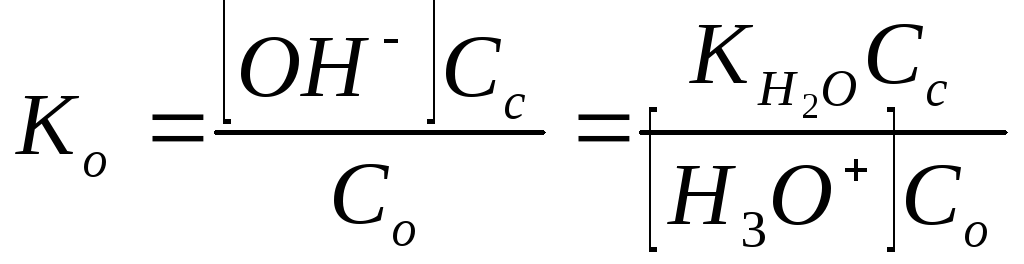 и
и
![]()
Таким образом, концентрация ионов водорода (и соответственно рН) в буферном растворе зависит от отношения в нем аналитических концентраций кислоты или основания и соли, а также от константы равновесия. Следовательно, при разбавлении буферного раствора его рН не должно изменяться. На самом деле небольшое изменение часто наблюдается. Это изменение рН обусловлено изменением коэффициента активности соли с разведением. Поскольку соль в буферном растворе является сильным электролитом, мы должны для строгого описания ее поведения пользоваться понятием активности, а не концентрации.
Способность буферных растворов противостоять изменению рН количественно выражается величиной
![]()
и называется буферной емкостью. Буферная емкость — это количество добавляемой кислоты или щелочи (dx), необходимое для изменения рН на единицу.
Определение буферной емкости производится следующим образом. Пусть имеем буферный раствор, состоящий из слабой одноосновной кислоты НА и ее соли с сильным основанием. Определим сперва концентрацию недиссоциированных молекул кислоты НА, Очевидно
[HA] = Ck – [A–]
Из условия электронейтральности раствора имеем
[K+] +[H3O+] = [A–] + [OH–]
где [К+] — концентрация катионов в буферном растворе.
Запишем теперь выражение для константы равновесия кислоты
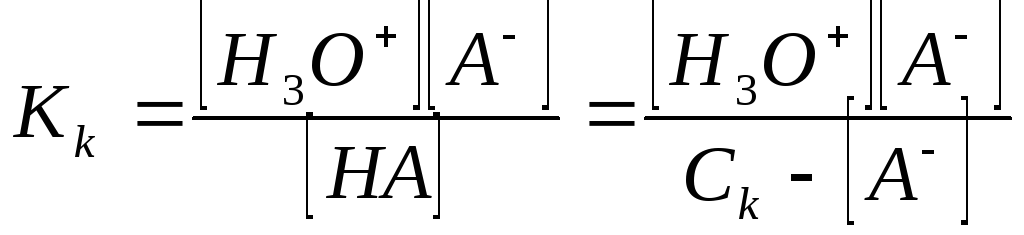
откуда
KKCK – KK [A–] = [H3O+][A–]
и

Подставим это выражение в уравнение электронейтральности и определим [К+]

Изменение концентрации катионов в буферном растворе может произойти только за счет концентрации добавленного основания, т. е.
∂[K+] = ∂x
Тогда
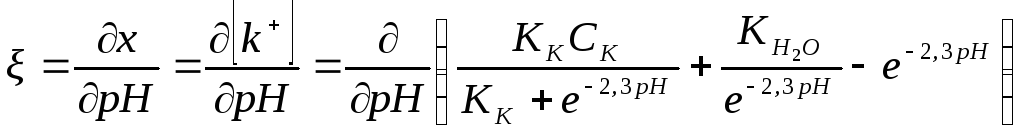
В скобках концентрация ионов гидроксония заменена выражением, содержащим рН. Поскольку – ln [Н3О+] = 2,3 рН, то [Н3О+] = е–2,3pH.
Дифференцирование выражений в скобках по рН дает:
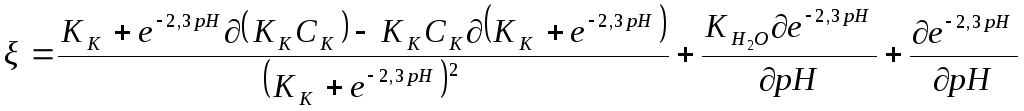
Так как
![]()
то окончательно имеем

В этом выражении первый член в скобках обычно много больше второго и третьего членов. Действительно, например, для буферного раствора СН3СООH + CH3COONa, для которого Кк ≈10–5, если примем, что Ск = 1,0, то, [Н3О+] ≈10–4. Тогда
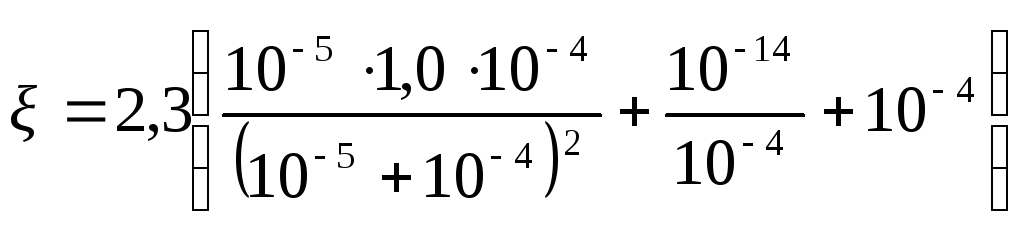
И первый член в скобках составит примерно 10–1, т. е. окажется на три порядка больше последнего члена и на девять порядков больше второго члена. Следовательно, с достаточной точностью можно записать:
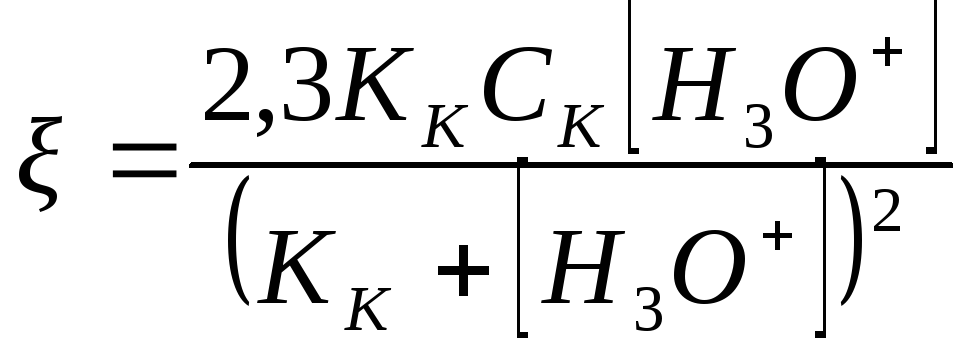
Буферная емкость раствора может быть различной в разных областях кислотности. Для определения области кислотности максимальной буферной емкости продифференцируем последнее уравнение по рН:
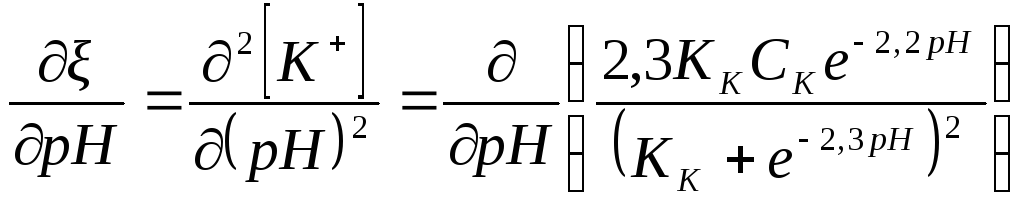
Обозначим
u = 2,3KKCKe–2,3pH; v2 = (KK + e–2,3pH)2
Тогда
du = 2,3 KKCK(–2,3)e–2,3pH
dv2 = 2vdv = 2v(–2,3e–2,3pH)
Следовательно
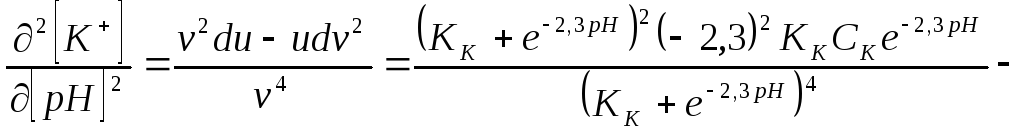

или

Для определения положения максимума приравняем правую часть уравнения нулю. Тогда после соответствующих сокращений получим
 или
KK
= [H3O+];
pKK
= pH
или
KK
= [H3O+];
pKK
= pH
Следовательно, максимум буферной емкости раствора будет при том значении рН, которое численно равно показателю константы равновесия кислоты. На основе этого вывода подбирают буферные растворы, обладающие наибольшим буферным действием в заданном интервале рН.
