
- •Оглавление
- •2 Электрохимические системы
- •2.1. Определение электрохимической системы
- •2.2. Прохождение электрического тока в электрохимической системе. Законы фарадея
- •2.3. Термодинамически обратимые и необратимые электрохимические системы
- •2.4. Классификация термодинамически обратимых электрохимических систем
- •2.5. Составляющие электрохимической системы
- •2.6. Идеальные и реальные электрохимические системы
- •3 Метод активности
- •3.1. Формальный метод активности льюиса
- •3.2. Расчет коэффициента активности по дебдш и хюккелю
- •3.3. Расчет коэффициента активности по робинсону и стоксу
- •3.4. Эмпирические способы расчета коэффициентов активности
- •4 Ионные равновесии
- •4.1. Ионные равновесия в растворах электролитов
- •4.2. Сольволиз и буферные свойства
- •4.3. Константы образования комплексных ионов
- •4.4. Ступенчатая диссоциация электролитов
- •4.5. Ионные равновесия в растворах электролитов в присутствии твердой фазы
- •5 Процессы переноса в электрохимических системах
- •5.1. Электрическая проводимость
- •5.1.1. Электронная проводимость
- •Ионная проводимость
- •Электрическая проводимость газов
- •5.1.2.2. Электрическая проводимость твердых тел
- •5.1.2.3. Электрическая проводимость расплавленных соединений
- •5.1.2.4. Электрическая проводимость растворов
- •5.1.3. Теории электрической проводимости растворов
- •5.1.3.1. Простая гидродинамическая теория
- •5.1.3.2. Теория дебая – хюккеля – онзагера
- •5.1.3.3. Теория эйринга
- •5.1.3.4. Протолитическая теория электролитической проводимости
- •5.1.3.5. Применение средней ионной активности для расчета проводимости
- •5.2. Диффузия в растворах электролитов
- •5.3. Диффузионный, или жидкостный, потенциал
- •5.4. Конвективный перенос в растворах
- •5.5. Термодиффузия
- •6. Напряжение электрохимических систем
- •6.1. Возникновение напряжения в электрохимической системе
- •6.2. Равновесные потенциалы на границах раздела фаз
- •6.3. Уравнения равновесного электродного потенциала
- •6.4. Влияние температуры на электродный потенциал
- •6.5. Выбор относительной шкалы потенциалов
- •6.6. Электроды сравнения
- •6.7. Правило лютера
- •6.8. Термодинамическое равновесие с растворителем
- •6.9. Расчет напряжения электрохимических систем с помощью потенциалов в относительной шкале
- •6.9.1. Напряжение электрохимических систем с химической реакцией
- •Напряжение электрохимических систем без химической реакции
- •Напряжение электрохимических систем без химической реакции
- •6.10. Методы устранения диффузионного потенциала
- •4,2 Кмоль/м3 20,4 кмоль/м3
- •6.11. Термодинамика электрохимических систем
- •6.12. Ионоселективные электроду
- •6.12.1. Уравнение мембранного потенциала
- •6.12.2. Электроды с твердыми ионитовыми мембранами
- •6.12.3. Электроды с жидкими ионитовыми memбpahaми
- •6.12.4. Измерение напряжения электрохимических систем с ионоселективными электродами
- •7 Двой ной электрический слой
- •Явления адсорбции при образовании двойного электрического слоя
- •Злектрокапиллярные явления на ртути и твердых металлах
- •7.3. Емкость двойного электрического слоя
- •7.3.1. Влияние специфической адсорбции ионов на поверхностное натяжение и емкость двойного электрического слоя
- •7.3.2. Заряжение емкости двойного электрического слоя
- •7.4. Теории строения двойного электрического слоя
- •7.5. Двойной слой на твердых электродах
- •7.6. Двойной слой на электродах в расплавленных и твердых электролитах
- •%(%8 Кинетика электродных процессов
- •8.1. Поляризационные кривые
- •8.2. Перенапряжение электрохимической стадии
- •8.2.1. Уравнение поляризационной кривой без учета специфической адсорбции и ψ’-потенциала
- •Влияние ψ’-потенциала на скорость реакции разряда — ионизации
- •8.2.3. Стандартная константа скорости реакции переноса электрона и стандартная плотность тока обмена
- •8.2.4. Способы определения коэффициентов переноса из поляризационных кривых
- •8.3. Стадийные электродные реакции
- •8.4. Электрохимические реакции, включающие быстрые химические стадии
- •8.5. Определение порядков электрохимических реакций
- •8.6. Безбарьерные и безактивациониые электрохимические реакции
- •8.7. Кинетика реакций при конечных степенях заполнения поверхности
- •9 Диффузионная кинетика
- •9.1. Перенапряжение диффузии
- •9.2. Перенапряжение диффузии с учетом миграции
- •9.3. Поляризационные кривые при замедленной стадии диффузии
- •9.4. Окислительно-восстановительные реакции
- •9.5. Сложные окислительно-восстановительные реакции
- •9.6. Наложение перенапряжения диффузии и замедленного переноса электронов (смешанная кинетика)
- •10 Перенапряжение химической реакции
- •10.1. Перенапряжение, обусловленное предшествующей гомогенной химической реакцией в катодном процессе и последующей химической реакцией в анодном процессе
- •10.2. Общий случай электрохимической реакции с замедленной гомогенной химической стадией
- •10.3. Перенапряжение, обусловленное гетерогенными химическими стадиями
- •10.4. Зависимость плотности тока от концентрации и порядок химической реакции
- •11 Примеры различных механизмов электрохимических реакций
- •11.1. Реакция выделения водорода
- •11.2. Кинетика реакций в расплавах и твердых электролитах
- •12 Кинетика реакций электрохимического выделения металлов
- •12.1. Кинетика реакций выделения металлов на жидких катодах
- •12.2. Кинетика реакций при электроосаждении металлов на твердых электродах
- •12.3. Влияние поверхностно-активных веществ на рост кристаллов
- •12.4. Влияние природы металла и состава раствора на кинетические параметры
- •12.5. Электроосаждение металлов из расплавов
- •12.6. Электрохимическое восстановление оксидов
- •13 Анодное растворение и пассивность металлов
- •13.1. Анодное растворение металлов
- •13.2. Пассивность металлов
- •13.2.1. Теория пассивности
- •13.2.2. Кинетика процесса пассивирования
- •14 Короткозамкнутые электрохимические системы
- •14.1. Общие положения
- •14.2. Электрохимическая коррозия
- •14.2.1. Скорость коррозии металла и коррозионный потенциал
- •14.2.2. Растворение металлов под током в коррозйонноактивных средах
- •14.2.3. Коррозия технических металлов
- •14.2.4. Способы снижения скорости коррозионного процесса
- •14.3. Контактное вытеснение металлов (цементация)
- •14.3.1. Общие положения
- •14.3.2. Кинетика процесса цементации
- •14.3.3. Конечный период цементации
- •15 Параллельные электрохимические реакции
- •15.1. Условия протеканий параллельных реакций
- •15.2. Распределение плотности тока между параллельными реакциями
- •16 Основы методов исследования электрохимических реакций
- •16.1. Общие требования к методам исследования
- •16.2. Электроды, применяемые в кинетических исследованиях
- •16.3. Измерение потенциалов под током
- •16.4. Методы исследования
- •Литература
14.3.3. Конечный период цементации
Конечный период цементации характеризуется резким замедлением основной реакции восстановления ионов вытесняемого металла. В связи с этим скорости побочных реакций становятся соизмеримыми с реакцией восстановления основного металла и ими уже нельзя пренебрегать.
В первую очередь необходимо учитывать реакцию восстановления растворенного в электролите молекулярного кислорода. Благодаря малой растворимости кислорода в электролите скорость этой реакции быстро достигает предельного тока диффузии кислорода к поверхности катодных участков, причем скорость восстановления обычно невелика. Поэтому во время главного периода цементации ею можно пренебречь. Но, когда концентрация восстанавливающихся ионов становится очень малой, а поляризация анодного металла еще невелика, значительная часть растворяющегося металла идет на компенсацию реакции восстановления кислорода. Если же к концу процесса происходит пассивация вытесняющего металла или резкое уменьшение анодных участков, приводящее к очень сильной поляризуемости анодного процесса, то может не только прекратиться катодное восстановление ионов металла, но и начаться анодное растворение осевшего ранее металла.
15 Параллельные электрохимические реакции
Очень часто при поляризации электрода на нем протекает не одна какая-то электрохимическая реакция, а две или несколько реакций параллельно. Это происходит из-за того, что в электролите находится несколько сортов частиц (ионов, молекул), способных при данном потенциале электрода претерпевать электрохимическое превращение.
15.1. Условия протеканий параллельных реакций
В основе теории параллельных реакций лежит принцип независимого их протекания, согласно которому каждая из параллельных реакций протекает независимо от всех других электродных реакций, идущих на том же электроде. Из этого принципа следует, что при заданном потенциале и прочих равных условиях скорость какой-нибудь реакции, протекающей одновременно с другими, равна скорости этой же реакции в отсутствие параллельных реакций. Для количественного рассмотрения вопроса введем допущение о том, что электрод под током имеет во всех точках один и тот же потенциал и, следовательно, ток распределяется по всей поверхности равномерно. Поскольку направленное протекание процесса возможно только тогда, когда потенциал под током лежит отрицательнее равновесного потенциала электродной реакции для катодного процесса и положительнее — для анодного процесса, то в случае параллельных реакций это же условие должно соблюдаться для всех реакций.
Равновесный потенциал одной из параллельных реакций, естественно, не должен зависеть от наличия или отсутствия других электрохимических реакций. Действительно, если вести электролиз водного раствора, содержащего сульфат меди и ионы Fe3+ и Fe2+, то на катоде будут протекать реакции:
Сu2+ + 2е = Сu; Fe3+ + е = Fe2+
Равновесные потенциалы этих реакций в соответствии с формулой Нернста (aCu = 1) запишутся в виде
![]() ;
;
![]()
Продукты реакций выделяются в разные фазы, поэтому их активности не зависят друг от друга.
Аналогичные рассуждения справедливы и для всех других случаев, когда продукты реакций выделяются в разные фазы, например при электролизе чистого подкисленного раствора сульфата меди, насыщенного кислородом. На катоде наряду с восстановлением ионов меди до металлической меди будет идти реакция восстановления молекулярного кислорода
О2 + 4Н3О+ + 4е = 6Н2О
равновесный потенциал которой равен
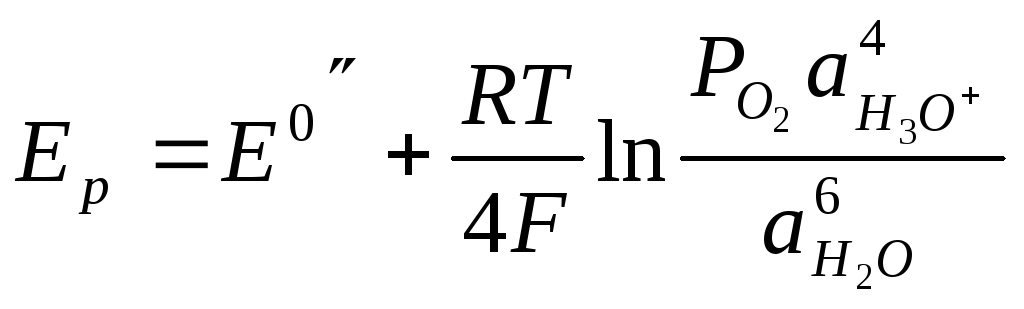
τ.
е.
зависит не только от
![]() и
и
![]() ,
но и от состава газовой фазы, равновесной
с раствором. Если, например, раствор
находится в равновесии с воздухом, то
равновесный потенциал будет положи-тельнее
потенциала в инертной атмосфере, когда
давление кислорода над раствором равно,
скажем, 1 Па. Но тем не менее равновесный
потенциал реакции восстановления
кислорода не будет зависеть от параллельной
реакции.
,
но и от состава газовой фазы, равновесной
с раствором. Если, например, раствор
находится в равновесии с воздухом, то
равновесный потенциал будет положи-тельнее
потенциала в инертной атмосфере, когда
давление кислорода над раствором равно,
скажем, 1 Па. Но тем не менее равновесный
потенциал реакции восстановления
кислорода не будет зависеть от параллельной
реакции.
Более сложным является вопрос о равновесном потенциале, если продукты параллельных реакций образуют одну фазу. Например, из нейтрального раствора хлорида натрия на инертном (платиновом) электроде при анодной поляризации совместно выделяются хлор и кислород. Равновесные потенциалы каждой из реакций в соответствии с их уравнениями
2Сl– – 2е = С12; 6Н2О – 4е = О2 + 4Н3О+
будут определяться активностями участников реакции в растворе и парциальным давлением газов над раствором. Здесь равновесные потенциалы обеих реакций зависят от состава общей газовой фазы; Но, так как взаимодействие хлора и кислорода в газовой фазе отсутствует, то парциальные давления этих компонентов газовой фазы легко можно определить.
Существенно иные соотношения получаются при катодном осаждении сплава или при взаимодействии продукта реакции с материалом катода. Когда на катоде образуется сплав двух металлов по реакциям
![]() +
z1e
= М1
(сплав) и
+
z1e
= М1
(сплав) и
![]() + z2e
= М2
(сплав)
+ z2e
= М2
(сплав)
то равновесные потенциалы обеих электрохимических реакций равны:
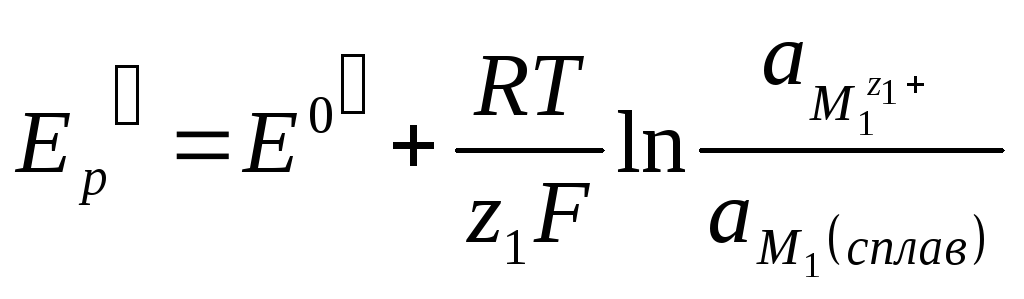
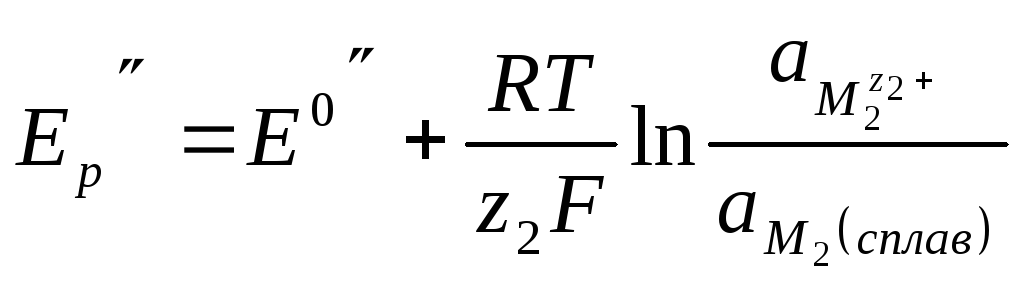
Активности компонентов сплава сильно зависят от характера взаимодействия между компонентами. Если сплав образует твердый раствор, близкий к идеальному, то активности компонентов в нем будут изменяться пропорционально их мольной доле. Когда компоненты сплава образуют химическое соединение, то активности резко снижаются и потенциалы сдвигаются в сторону электроположительных значений.
Активность компонента в сплаве будет зависеть и от его состава, поскольку в бинарных или многокомпонентных сплавах в зависимости от состава образуются, как правило, разные фазы. При этом, как показали П. М. Вячеславов и Г. К. Буркат с соавторами, диаграмма состояния сплавов, полученных электролизом, может либо повторять диаграмму состояния металлургических сплавов, либо существенно отличаться от нее не только протяженностью областей существования той или иной фазы, но и появлением или исчезновением отдельных фаз.
Взаимодействие продукта реакции с материалом катода также приводит к сдвигу равновесного потенциала в электроположительную сторону. Типичным примером такого взаимодействия является выделение натрия на ртутном катоде при электролизе водного раствора хлорида натрия. Благодаря тому, что натрий образует с ртутью химические соединения типа NaHgx (например, NaHg4 и NaHg6), равновесный потенциал реакции
Na+ + e + (Hg) = NaHgx
оказывается более чем на 1 В положительнее равновесного потенциала реакции
Na+ + e = Na
Рассмотрим условия, при которых протекают параллельные реакции. Если состав электролита таков, что на электроде возможно несколько электродных реакций, то в первую очередь будет протекать та электрохимическая реакция, для осуществления которой необходима наименьшая затрата энергии. Следовательно, при катодной поляризации электрода на нем начнется та из реакций, равновесный потенциал которой наиболее положителен, а при анодной поляризации — та, равновесный потенциал которой наименее положителен. Если же задать на электрод определенный катодный потенциал, например Ек, то на электроде будут протекать все те восстановительные реакции, равновесные потенциалы которых более электроположительны, чем Ек. Аналогично, если задать на электрод анодный, потенциал, скажем Еа, то на электроде будут протекать все те окислительные реакции, равновесные потенциалы которых менее положительны, чем, Еа. Следует только подчеркнуть еще раз, что необходимо оперировать равновесными потенциалами электрохимических реакций в данных конкретных условиях.
В качестве примера разберем возможные катодные реакции при электролизе водного раствора, содержащего в литре по 1 молю сульфата меди и сульфата никеля. Равновесный потенциал медного электрода в таком растворе будет составлять примерно 0,30 В. При iк, например, 100 А/м2 потенциал катода будет равен приблизительно 0,24 В по водородной шкале, т. е. катодная поляризация составит около 0,06 В. Равновесный же потенциал никелевого электрода в этом растворе равен примерно –0,27 В. Следовательно, на основе этих значений потенциалов говорить о возможности совместного разряда ионов меди и никеля не приходится. На самом деле благодаря образованию твердого раствора и уменьшению вследствие этого активности никеля в меди равновесный потенциал реакции Ni2+ + 2e = = Ni(Cu) при очень малой активности Ni(Cu) может стать положительнее потенциала катода и разряд ионов никеля станет возможным. Верхний предел включения никеля в медный осадок будет ограничиваться условием, согласно которому равновесный потенциал Ni2+/Ni(Сu) не должен быть отрицательнее потенциала работающего катода, а разряд ионов никеля должен происходить практически без поляризации. На основании этих допущений
![]()
или
![]()
Отсюда, считая, что в разбавленном твердом растворе, каким является сплав медь — никель, активность равна мольной доле компонента, получим для содержания никеля в катодном осадке меди значение ~3·10–18. Такая концентрация никеля в меди никакими способами, естественно, обнаружена быть не может, и мы вправе считать, что ионы никеля совместно с ионами меди практически не разряжаются. Тем не менее принципиально совместный разряд происходит. Если же между компонентами сплава проявляются силы химического взаимодействия, то как указано выше, вероятность совместного разряда возрастает. Так, В. А. Плотников и Д. П. Зосимович установили, что при подключении электрохимической системы
(–) М2 | М1z+Az– | M1 (+)
к внешнему источнику тока на аноде начинается растворение металла M1, а на катоде — образование поверхностного сплава металла M1 с материалом катода — более электроположительным металлом М2. Толщина образовавшегося поверхностного сплава определяется в первую очередь скоростью диффузии атомов M1 в глубину катода. Образование четырехкомпонентного поверхностного сплава наблюдал Д. П. Зосимович в системе
( –)
Cd
CdSO4
сплав Bi
– Sn
– Pb
(+)
–)
Cd
CdSO4
сплав Bi
– Sn
– Pb
(+)
 0,5
кмоль/м3
0,5
кмоль/м3
При электролизе на катоде такой системы, если процесс вести при температуре выше 75 °С, образуется капля жидкого четверного сплава Cd – Bi – Sn – Pb, температура плавления эвтектики которого 70 °С.
С тех же исходных позиций объясняется и открытое Б. Н. Кабановым, И. И. Астаховым и И. В. Киселевой внедрение электроотрицательных металлов, таких, как натрий, в свинец при электролизе водного раствора, например сульфата натрия, со свинцовым катодом. Наряду с основным катодным процессом — выделением водорода по реакции 2Н2О + 2е = Н2 + 2ОН– – при высоких катодных потенциалах идет разряд ионов натрия с образованием интерметаллических соединений.
Взаимодействие продуктов реакции влияет не только на равновесный потенциал, но и на расположение поляризационных кривых. При этом поляризационная кривая восстановления ионов компонента А совместно с ионами компонента Б (т. е. парциальная поляризационная кривая компонента А) может располагаться как при менее электроотрицательных, так и при более электроотрицательных потенциалах, по сравнению с поляризационной кривой восстановления только ионов компонента А из раствора с той же активностью ионов этого компонента. В первом случае говорят, что выделение компонента А совместно с компонентом Б происходит с деполяризацией, а во втором — со сверхполяризацией.
Причин сверхполяризации и деполяризации может быть несколько. Так, добавление к раствору компонента Б может, не отражаясь на активности ионов компонента А, привести к возникновению ψ’-потенциала. Тогда при заданном потенциале в зависимости от знака ψ’-потенциала парциальная скорость разряда ионов компонента А может как увеличиваться, так и уменьшаться. Следовательно, возникновение ψ’-потенциала способно вызвать как эффект сверхполяризации, так и деполяризации. Однако этот фактор вряд ли является решающим, поскольку указанные эффекты известны и в условиях, заведомо исключающих возникновение ψ’-потенциала. Кроме того, часто при осаждении на катоде двухкомпонентного сплава один из компонентов выделяется в сплав с деполяризацией, а другой — со сверхполяризацией, причем в обеих электродных реакциях участвуют катионы металлов. Между тем возникновение ψ’-потенциала в этих условиях должно оказывать одинаковый эффект на скорость разряда ионов обоих компонентов.
Причиной деполяризации, согласно К. М. Горбуновой и Ю. М. Полукарову, может быть энергия сплавообразования, вызывающая снижение энергии активации процесса разряда (рис. 15.1). Действительно, чем больше выделяется энергии при сплавообразо-вании, тем меньше потенциальная энергия компонента в сплаве и, следовательно, ниже располагается кривая потенциальной энергии (кривая 3). Вследствие этого уменьшается и энергия активации от
А1–2 до А1–3.
Эффект сверхполяризации не нашел еще достаточно однозначного объяснения. Согласно А. Т. Ваграмяну, он может быть вызван
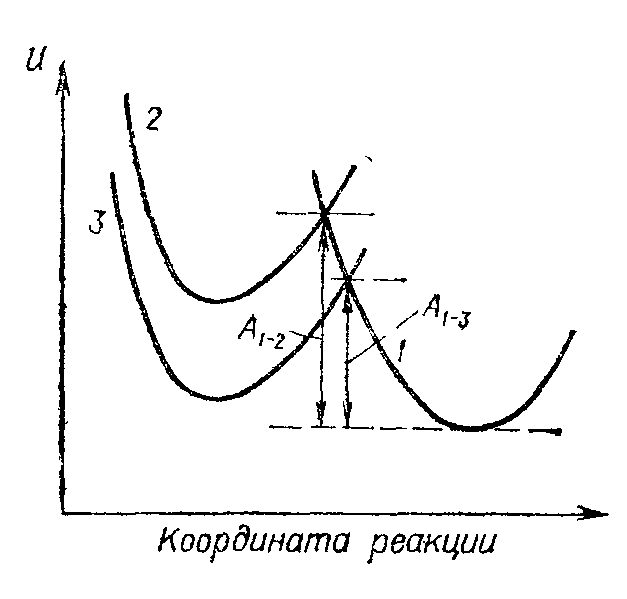
Рис. 15.1. Расположение кривых потенциальной энергии при разряде ионов металла в чистый металл (1, 2) и в сплав (3).
взаимным вытеснением ионов обоих компонентов в двойном слое. Если способность к адсорбции ионов одного из компонентов значительно больше способности к адсорбции ионов другого компонента, то будет происходить вытеснение последних из двойного слоя, что и вызовет эффект сверхполяризации.
Другое объяснение базируется на предположении, что скорость электрохимической реакции определяется удалением потенциала электрода от потенциала нулевого заряда. Поскольку потенциалы нулевого заряда сплавов в зависимости от состава изменяются от потенциала нулевого заряда первого компонента до потенциала нулевого заряда второго компонента, то при осаждении сплава энергия активации одного компонента будет снижена, а другого — повышена по сравнению с восстановлением каждого иона из компонентов в чистом виде. А это приводит к эффекту деполяризации для компонента с более электроотрицательным потенциалом нулевого заряда и одновременно к эффекту сверхполяризации для компонента с более электроположительным потенциалом нулевого заряда.
