- •Распределение концентрации реагента в периодическом реакторе идеального смешения:
- •Реактор идеального вытеснения и зависимости концентрации реагента са и степени превращения ха от длины реактора
- •Изменение параметров процесса в рис-н:
- •Изменение концентрации реагента а в каскаде реакторов идеального смешения
- •Кривые отклика при ступенчатом вводе индикатора в рив:
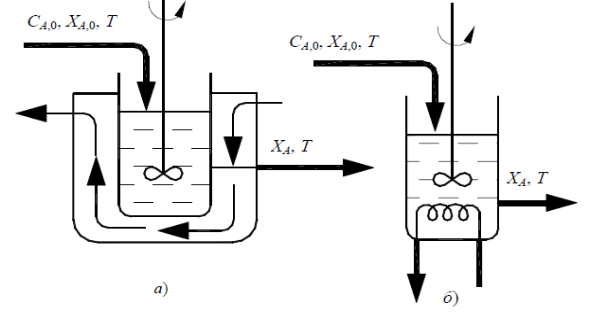
- •Политропические реакторы идеального смешения рис-н-п с отводом тепла через стенку (а) и отводом тепла с помощью охлаждающих элементов (б)
Кривые отклика при ступенчатом вводе индикатора в рив:
а – на входе в реактор; б – на выходе из идеального реактора; в – на выходе из реального реактора при наличии продольного перемешивания
Для РИВ кривая отклика представляет собой такую же ступенчатую прямую, как и для условий входа (рис. а и б), поскольку в РИВ отсутствует продольное перемешивание. В этом случае концентрация индикатора на входе жидкости в реактор мгновенно достигает некоторого постоянного значения по всему сечению реактора, которое сохраняется на всем пути движения жидкости.
Наличие индикатора в жидкости на выходе ее из реактора обнаруживается через некоторый промежуток времени (зависящий от скорости движения жидкости и высоты реактора) и его концентрация в дальнейшем не изменяется, так как он непрерывно вводится в жидкость на входе в реактор и выводится из него.
Для реального реактора вытеснения кривая отклика имеет вид S-образной кривой (рис. в), так как благодаря продольному перемешиванию, которое всегда наблюдается в реальном реакторе, часть индикатора выводится из реактора раньше, а часть – позже основной массы; постоянная концентрация индикатора устанавливается через более продолжительный промежуток времени, чем в РИВ.
Сравнение кривых отклика идеальных и реальных реакторов позволяет уточнить математическую модель реактора и, соответственно, повысить точность расчета.
Режимы работы реакторов
Температурные режимы. До сих пор при определении условий проведения процессов в реакторах влияние температуры не учитывалось, т.е. рассматривались процессы в изотермических условиях при Т = const. Между тем, в большинстве случаев температура в процессе изменяется и оказывает существенное влияние на кинетику, статику и селективность химических процессов. Поэтому в большинстве практических случаев в реакторе создают определенный температурный режим, обеспечивающий высокую эффективность процесса.
В зависимости от теплового эффекта протекающих реакций, а также от оптимального температурного режима, который необходимо поддерживать в реакторе, от реакционной смеси
-
либо отводят тепло,
-
либо к ней подводят тепло,
-
или же температурный режим в реакторе сохраняют таким, каким он самопроизвольно устанавливается в соответствии с тепловым эффектом реакции.
В связи с этим выбор теплового режима в реакторах и разработка методов его поддержания имеют большое практическое значение.
Уравнения, отражающие работу реактора с учетом влияния температуры, могут быть получены из уравнений материального баланса при условии, что в эти уравнения вместо постоянного значения константы скорости k (что справедливо для изотермических условий) вводят ее значение из уравнения (уравнение Аррениуса)
![]() (8)
(8)
Здесь R- универсальная газовая постоянная, T – температура, k0 – константа скорости химической реакции при стандартных условиях.
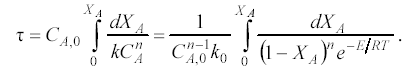 (9)
(9)
Каждый тип реактора может работать в трех режимах: адиабатическом, изотермическом и политропическом.
При адиабатическом режиме в реакторе отсутствует теплообмен с окружающей средой и тепло химической реакции полностью расходуется на изменение температуры реакционной смеси.
При изотермическом режиме путем подвода или отвода тепла в реакторе поддерживают постоянную температуру в течение всего процесса.
При политропическом режиме температура в реакторе непостоянна, при этом часть тепла может отводиться от реакционной смеси или подводиться к ней.
Адиабатический и изотермический режимы представляют собой предельные идеальные случаи, которые на практике почти не наблюдаются. Однако режим многих реакторов в производственных условиях приближается к этим крайним моделям, поэтому с достаточной для практических целей точностью эти реакторы могут быть рассчитаны по уравнениям, полученным для адиабатического и изотермического режимов.
УРАВНЕНИЕ ТЕПЛОВОГО БАЛАНСА РЕАКТОРА
Основой для расчета реакторов с учетом теплового режима служит уравнение теплового баланса, составленное обычно на единицу времени. В общем виде это уравнение может быть записано следующим образом:
![]() (9)
(9)
Для экзотермической реакции приход и расход тепла
![]() (10)
(10)
![]() (11)
(11)
где
Qпр – количество тепла, поступающего в единицу времени в тот реакционный объем, для которого составляется баланс;
Qрасх– количествотепла, расходуемого в единицу времени в реакционном объеме.
Qреаг – количество тепла, вносимого исходными реагентами;
Qх.р – количество тепла, выделяющегося при химической реакции; Qнак – количество тепла, накапливающегося в реакторе;
Qпрод – количество тепла, уносимого продуктами;
QT – количество тепла, выводимого в результате теплообмена.
Подставив значения Qпр и Qрасх в уравнение (9), находим
![]() (12)
(12)
![]()
Здесь Qконв – обозначает количество тепла, выносимого конвективным потоком, с учетом которого получим
![]() (13)
(13)
Полученное уравнение теплового баланса (13) может принимать различную форму в зависимости от типа реактора и теплового режима процесса.
В общем случае температура и другие параметры процесса изменяются как в объеме реактора, так и во времени, поэтому уравнения теплового баланса составляют в дифференциальной форме (подобно тому, как это было принято при составлении уравнения материального баланса).
Для этой цели используют дифференциальное уравнение конвективного теплообмена
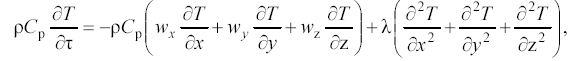 (14)
(14)
где
![]() ,
Сp – плотность
и удельная теплоемкость реакционной
смеси;
,
Сp – плотность
и удельная теплоемкость реакционной
смеси;
х, y, z – пространственные координаты;
wx, wy, wz – составляющие скорости движения потока в направлении осей;
λ – коэффициент теплопроводности реакционной смеси.
Чтобы использовать это уравнение по отношению к простой необратимой реакции A → R + Q,
его составляют по одному из компонентов реакционной смеси (любому) и
вводят в него дополнительные члены, учитывающие отвод тепла в результате теплообмена и тепло реакции.
Если составить
баланс по компоненту А
и ввести в
уравнение (14) дополнительные члены в
соответствии с уравнением (![]() (13)),
то дифференциальное уравнение
конвективного теплообмена
(уравнение теплового баланса) может
быть записано в виде
(13)),
то дифференциальное уравнение
конвективного теплообмена
(уравнение теплового баланса) может
быть записано в виде
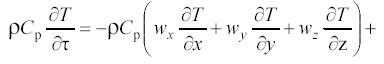
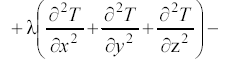
![]()
![]()
![]() (15)
(15)
Левая часть уравнения (15) характеризует скорость накопления тепла в элементарном объеме, для которого составляется тепловой баланс. Этому члену соответствует величина в уравнении (12)
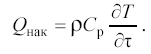
Первая группа членов правой части уравнения (15) определяет скорость конвективного переноса тепла по соответствующим координатам (х, у, z) в элементарном объеме.
Вторая – скорость отвода тепла в результате молекулярной и конвективной теплопроводности реакционной среды.
Первая и вторая группы членов правой части уравнения (15) соответствуют параметру Qконв в уравнении (12):
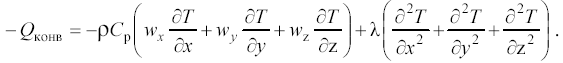 (16)
(16)
Новые, вводимые в уравнение (15) группы членов
характеризуют скорость отвода тепла путем теплообмена (третья группа)
![]() (17)
(17)
и скорость подвода тепла в результате химической реакции (четвёртая группа)
![]() (18)
(18)
где Fуд – удельная поверхность теплообмена;
К – коэффициент теплопередачи;
![]() ;
(Т, Тхл – температура
реакционной смеси и хладоагента);
;
(Т, Тхл – температура
реакционной смеси и хладоагента);
Н – тепловой эффект химической реакции.
Общее решение уравнения (15) затруднительно, поэтому в зависимости от характера реакции, теплового режима и режима движения реакционной среды (т.е. от гидродинамической обстановки в реакторе), в уравнение (15) вводят соответствующие упрощения. Это позволяет найти решение соответствующей задачи с достаточной для практических целей точностью.
Политропический режим представляет собой общий случай, т.е. при составлении теплового баланса такого реактора учитываются все виды подвода и отвода тепла.
Из уравнения теплового баланса для политропического реактора легко определить частные случаи:
• для адиабатического реактора – с учетом равенства Qт = 0;
• для изотермического реактора – с учетом равенства QКОНВ = 0.
Рассмотрим для примера реактор идеального смешения непрерывный РИС-Н-П, работающий в политропическом тепловом режиме (П).
Отвод или подвод тепла для РИС-Н-П осуществляется через стенку реактора или с помощью теплообменных элементов, расположенных внутри реактора