
- •1. Строение атома
- •1.1. Энергетическое состояние электронов в атоме
- •1.2. Основные принципы распределения электронов в атомах
- •В соответствии с этим правилом последовательность заполнения подуровней:
- •1.3. Периодический закон и электронные формулы атомов
- •1.4. Примеры решения и оформления заданий
- •1.5. Задания для самостоятельной подготовки
- •2. Классы неорганических веществ
- •2.1. Оксиды
- •Основные оксиды
- •Кислотные оксиды
- •Амфотерные оксиды
- •2.2. Гидроксиды
- •Основания
- •Кислоты
- •Амфотерные гидроксиды
- •2.3. Соли
- •Средние соли
- •Кислые соли
- •Основные соли
- •2.4. Примеры решения заданий
- •2.5. Задания для самостоятельной подготовки
- •3. Основы химической термодинамики
- •3.1. Энтальпия
- •3.2. Энтропия
- •3.3 Энергия Гиббса и ее изменение в ходе химических реакций
- •3.4. Примеры решения заданий
- •3.5. Задания для самостоятельной подготовки
- •4. Химическое равновесие
- •4.1. Константа химического равновесия
- •4.2. Принцип Ле Шателье
- •Влияние концентраций компонентов системы
- •Влияние температуры
- •Влияние общего давления в системе
- •4.3 Примеры решения заданий
- •4.4. Задания для самостоятельной подготовки
- •5. Растворы
- •5.1. Примеры решения заданий
- •5.2. Задания для самостоятельной подготовки
- •5.3. Электролиты
- •Теория электролитической диссоциации Степень диссоциации
- •5.4. Ионные реакции
- •5.5. Примеры решения заданий
- •5.6. Задания для самостоятельной подготовки
- •5.7. Диссоциация воды. Водородный показатель
- •5.8. Гидролиз
- •5.9. Примеры решения заданий
- •5.10 Задания для самостоятельной подготовки
- •6. Окислительно-восстановительные процессы
- •6.1. Степень окисления
- •6.2. Окислительно-восстановительные реакции
- •6.3. Составление уравнений окислительно-восстановительных реакций
- •Правила составления полуреакций в разных средах
- •Овр в кислой среде
- •Овр в щелочной среде
- •Овр в нейтральной среде
- •6.4. Примеры решения заданий
- •6.5. Задания для самостоятельной подготовки
- •6.6 Взаимодействие металлов с кислотами, водой и растворами щелочей
- •6.7. Примеры решения и оформления заданий
- •6.8. Задания для самостоятельной подготовки
- •6.9. Электрохимическая коррозия
- •Описание процесса гальванокоррозии
- •6.10. Примеры решения заданий
- •6.11. Задания для самостоятельной подготовки
- •6.12. Электролиз растворов
- •Катодные процессы
- •Анодные процессы
- •Законы фарадея
- •6.13. Примеры решения и оформления заданий
- •6.14 Задания для самостоятельной подготовки
- •Библиографический список Основная литература
- •Дополнительная литература
- •Стандартные энтальпии образования и энтропии
- •Названия некоторых кислот и их солей
- •Стандартные окислительно-восстановительные потенциалы металлов
- •Окислительно-восстановительные потенциалы водорода, кислорода и металлов в разных средах оглавление
Влияние температуры
Направление смещения равновесия в результате изменения температуры определяется знаком теплового эффекта реакции:
-
нагревание вызывает смещение равновесия в сторону процесса, протекание которого сопровождается поглощением теплоты, т.е. в сторону эндотермического процесса (ΔН > 0);
-
понижение температуры приводит к смещению равновесия в сторону процесса, сопровождающегося выделением теплоты, иначе говоря, в сторону экзотермического процесса (ΔН < 0).
Реакция синтеза аммиака
N2
+ 3 Н2
![]() 2NH3,
ΔН0Х.Р
=
– 92 кДж
2NH3,
ΔН0Х.Р
=
– 92 кДж
является экзотермической, поэтому при понижении температуры равновесие в системе смещается в сторону прямой реакции, так как этот процесс идет с выделением теплоты.
Влияние общего давления в системе
-
Повышение давления в системе смещает равновесие в направлении реакции, которая идет с уменьшением количества газообразных веществ, т.е. с уменьшением давления.
-
Уменьшение давления способствует смещению химического равновесия в сторону реакции, протекающей с увеличением количества газообразных веществ, т.е. с увеличением давления.
Например, в реакции
N
 2(г)
+ 3H2(г)
2(г)
+ 3H2(г)
![]() 2NH3(г)
2NH3(г)
4 моль 2 моль
увеличение давления приведет к смещению равновесия в сторону прямой реакции.
В реакции
F
 eO(к)
+ СO(г)
eO(к)
+ СO(г)
![]() CO2(г)
+ Fe(к)
CO2(г)
+ Fe(к)
1 моль 1 моль
количества моль газов в правой и левой части уравнения реакции равны реакция протекает без изменения объема, следовательно, изменение давления на равновесие системы не повлияет.
4.3 Примеры решения заданий
Для обратимой реакции
2 SO2(г) + O2(г)
![]() 2 SO3(г), ΔHХ.Р
= –196 кДж
2 SO3(г), ΔHХ.Р
= –196 кДж
-
напишите математическое выражение константы химического равновесия;
-
укажите направление смещения равновесия при изменении условий:
а) уменьшении концентрации одного из газообразных продуктов;
б) понижении давления в системе;
в) повышении температуры в системе.

а) снижение концентрации продукта реакции (SO3) приводит к смещению равновесия в сторону реакции, способствующей увеличению концентрации SO3, в данной системе – в сторону прямой реакции (→);
б) при понижении давления равновесие смещается в сторону увеличения количества газообразных веществ, в данном случае – в сторону обратной реакции (←);
в) при повышении температуры равновесие смещается в сторону эндотермической реакции, в данном случае – в сторону обратной реакции (←).
4.4. Задания для самостоятельной подготовки
Для предложенной обратимой реакции (табл. 1) напишите математическое выражение константы химического равновесия и укажите направление смещения равновесия при изменении условий:
а) уменьшении концентрации одного из газообразных продуктов;
б) понижении давления в системе;
в) повышении температуры в системе.
Таблица 1
-
Номер
Уравнение реакции
 ,
кДж
,
кДж1
2
3
1
SO3(г) + H2(г)
 SO2(г)
+ H2O(г)
SO2(г)
+ H2O(г)-144
2
2H2(г) + O2(г)
 2 H2O(г)
2 H2O(г)-484
3
FeO(к) + CO(г)
 Fe(к)
+ CO2(г)
Fe(к)
+ CO2(г)+400
4
2N2O(г) + O2(г)
 4NO(г)
4NO(г)+196
5
2NO(г)
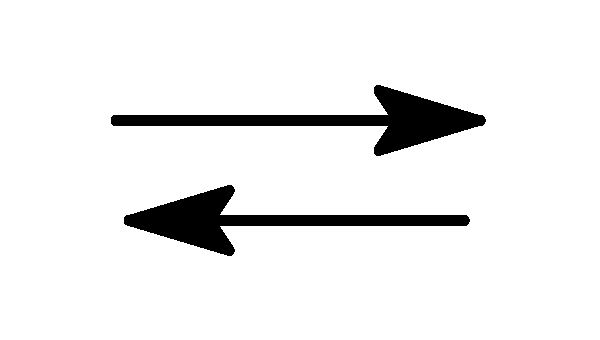 N2(г)
+ O2(г)
N2(г)
+ O2(г)-180
Окончание табл. 1
1
2
3
6
NH4Cl(к)
 NH3(г)
+ HCl(г)
NH3(г)
+ HCl(г)+63
7
2CH4(г) + 3O2(г)
 2CO(г)
+ 4H2O(г)
2CO(г)
+ 4H2O(г)-597
8
H2O(г) + CO(г)
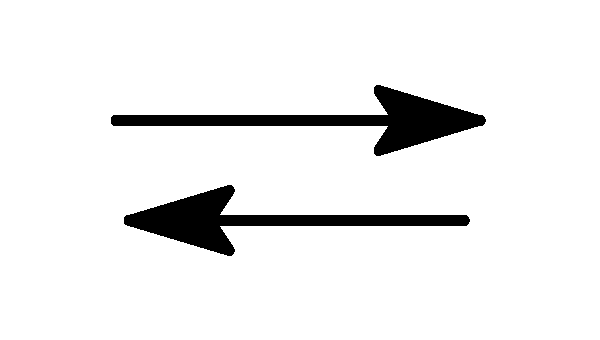 CO2(г)
+ H2(г)
CO2(г)
+ H2(г)-41
9
2Al2(SO4)3 (к)
 2Al2O3(к)
+ 6SO2(г)
+ 3O2(г)
2Al2O3(к)
+ 6SO2(г)
+ 3O2(г)+1740
10
ZnSO4(к)
 ZnO(к)
+ SO3(г)
ZnO(к)
+ SO3(г)+565
11
2N2O3(г)
 2NO(г)
+ N2O4(г)
2NO(г)
+ N2O4(г)+149
12
2H2S(г) + 3O2(г)
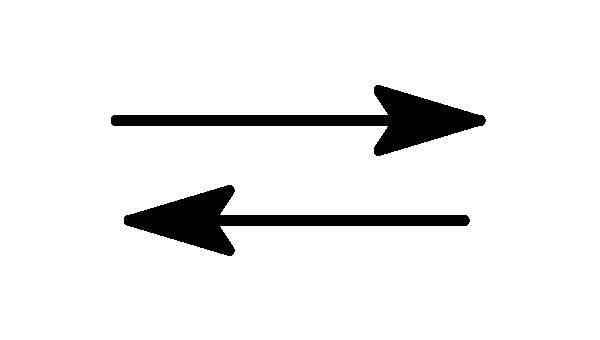 2H2O(г)
+ 2SO2(г)
2H2O(г)
+ 2SO2(г)-1038
13
S(к) + H2(г)
 H2S(г)
H2S(г)-21
14
CO2(г) + C(т)
 2CO(г)
2CO(г)+172
15
CH4(г) + H2O(г)
 3H2(г)
+ CO(г)
3H2(г)
+ CO(г)+206
16
PCl5(г)
 PCI3(г)
+ Cl2(г)
PCI3(г)
+ Cl2(г)+21
17
Fe3O4(к) + CO(г)
 3FeO(к)
+ CO2(г)
3FeO(к)
+ CO2(г)+21
18
N2O3(г)
 NO(г)
+ NO2(г)
NO(г)
+ NO2(г)+104
19
C(к) + O2(г)
 CO2(г)
CO2(г)-394
20
2AlCl3(к)
 2Al(к)
+ 3Cl2(г)
2Al(к)
+ 3Cl2(г)+338
21
2CO(г) + O2(г)
 2CO2(г)
2CO2(г)-566
22
2NH3(г)
 N2(г)
+ 3H2(г)
N2(г)
+ 3H2(г)+92
23
H2(г) + I2(г)
 2HI(г)
2HI(г)+12
24
BaCO3(к)
 BaO(к)
+ CO2
(г)
BaO(к)
+ CO2
(г)+251
25
4NO(г) + 6H2O(г)
 4NH3(г)
+ 5O2(г)
4NH3(г)
+ 5O2(г)+908
26
2МgCl2(к) + O2(г)
 2MgO(к)
+ 2Cl2(г)
2MgO(к)
+ 2Cl2(г)+82
27
Ca(OH)2(к)
 CaO(к)
+ H2O(г)
CaO(к)
+ H2O(г)+109
28
N2(г) + O2(г)
 2NO(г)
2NO(г)+180
29
NO(г) + NO2(г)
 N2O3(г)
N2O3(г)-149
30
3FeO(к) + CO2(г)
 Fe3O4(к)
+ CO(г)
Fe3O4(к)
+ CO(г)-21
