
- •Классификация ингибиторов коррозии
- •Основные виды тэ
- •Теплота сама собой не может переходить от более холодного тела к более нагретому
- •Невозможно превратить какое- либо количество теплоты в работу без того , чтобы часть тепла не была растрачена при более низкой температуре :
- •В изолированных системах самопроизвольно идут только те процессы , которые ведут к увеличению неупорядоченности системы ,т.Е к росту энтропии
- •28. Свойства истинных растворов. Способы выражения концентрации: массовая доля, молярная, молярная эквивалента, титр, моляльная, мольная доля, взаимосвязь между концентрациями.
- •29. Растворы электролитов. Механизмы электролитической диссоциации веществ с ионной и ковалентной полярной связью. Ступенчатая диссоциация.
- •30. Растворы слабых электролитов. Степень диссоциации. Константа диссоциации. Закон разбавления Оствальда.
- •32.Кислотно-основные свойства веществ с точки зрения электролитической диссоциации. Ионное произведение воды. Водородный и гидроксидный показатели. Индикаторы.
- •36. Общие закономерности электрохимических процессов. Возникновение электродного потенциала. Шкала стандартных электродных потенциалов. Типы электродов.
28. Свойства истинных растворов. Способы выражения концентрации: массовая доля, молярная, молярная эквивалента, титр, моляльная, мольная доля, взаимосвязь между концентрациями.
Концентрация раствора – это отношение количества или массы растворённого вещества к объёму или массе всего раствора (иногда растворителя). Существует несколько способов выражения концентрации растворов, основные из которых – массовая доля, молярная доля, титр, молярная концентрация, нормальная концентрация (молярная концентрация эквивалентов), моляльная концентрация.
Массовая доля вещества (ω) в растворе – отношение массы растворённого вещества к массе раствора, выражаемое в долях или процентах.
Моляльная концентрация (моляльность) – отношение количества растворённого вещества к массе растворителя:
Молярная доля вещества в растворе (χ) – отношение количества растворённого вещества к сумме количества растворённого вещества (веществ) и количества вещества растворителя. Молярная доля также выражается в долях единицы или в процентах:
Молярная
концентрация (молярность) (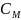 )
– это отношение количества растворённого
вещества к объёму раствора. Она выражается
в моль/л и показывает, сколько молей
растворённого вещества содержится в
1л раствора:
)
– это отношение количества растворённого
вещества к объёму раствора. Она выражается
в моль/л и показывает, сколько молей
растворённого вещества содержится в
1л раствора:
Раствор с молярной концентрацией 1 моль/л называют одномолярным и обозначают 1М; с молярной концентрацией 0,1 моль/л – децимолярным (0,1 М); с молярной концентрацией 0,01 моль/л – сантимолярным (0,01 М) и т. п.
Молярная
концентрация эквивалентов (нормальная
концентрация, нормальность) (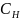 )
– это отношение количества вещества
эквивалентов растворённого вещества
к объёму раствора. Она показывает
сколько моль эквивалентов растворённого
вещества содержится в 1 л раствора, и
выражается также в моль/л. Аналогично
молярной концентрации, раствор с
нормальной концентрацией 1 моль/л
называют однонормальным и обозначают
1н, и т.д.
)
– это отношение количества вещества
эквивалентов растворённого вещества
к объёму раствора. Она показывает
сколько моль эквивалентов растворённого
вещества содержится в 1 л раствора, и
выражается также в моль/л. Аналогично
молярной концентрации, раствор с
нормальной концентрацией 1 моль/л
называют однонормальным и обозначают
1н, и т.д.
Титр раствора (Т) показывает, сколько граммов растворённого вещества содержится в 1 мл раствора:
