
- •Сафу им. М.В.Ломоносова, иИиКт
- •10 Июня 2011 г.
- •Вопрос 1. Механическое движение. Система отсчёта. Путь, перемещение, траектория. Расчёт пути при равноускоренном движении.
- •Вопрос 2. Кинематика поступательного движения. Скорость мгновенная, средняя. Модуль скорости. Ускорение и его составляющие.
- •Вопрос 3. Кинематика вращательного движения. Элементарный угол поворота, угловая скорость, угловое ускорение. Связь линейных и угловых величин. Псевдовекторы.
- •Вопрос 4. Масса, свойство массы. Сила. Инерция. Первый закон Ньютона.
- •Вопрос 5. Сила. Импульс тела. Второй закон Ньютона. Принцип независимости сил. Третий закон Ньютона.
- •Вопрос 6. Импульс механической системы. Внешние силы. Замкнутая система. Закон сохранения импульса. Центр масс.
- •Вопрос 7. Работа силы в механике. Работа силы тяжести, работа силы упругости.
- •Вопрос 8. Кинетическая энергия – функция состояния системы. Теорема о кинетической энергии.
- •Вопрос 9. Силовое поле. Консервативные силы и диссипативные силы. Работа консервативных сил. Потенциальная энергия. Связь потенциальной энергии и консервативной силы.
- •Вопрос 10. Силовое поле. Потенциальное поле. Полная механическая энергия. Закон сохранения энергии.
- •Вопрос 11. Момент инерции материальной точки, твёрдого тела. Теорема Штейнера. Кинетическая энергия вращающегося тела.
- •Вопрос 12. Момент силы материальной точки относительно точки, момент силы материальной точки относительно оси. Основное уравнение динамики вращательного движения.
- •Вопрос 13. Момент импульса материальной точки относительно точки, момент импульса материальной точки относительно оси.
- •Вопрос 14. Момент импульса твердого тела. Закон сохранения момента импульса.
- •Вопрос 15. Параметры состояния. Термодинамическое равновесие. Модель идеального газа. Уравнение состояния идеального газа. Изопроцессы идеального газа.
- •Вопрос 16. Основное уравнение молекулярно-кинетической теории идеальных газов. Молекулярно-кинетическое толкование температуры. Средняя квадратичная скорость.
- •Вопрос 17. Закон Максвелла для распределения молекул идеального газа по скоростям. Анализ функции распределения.
- •Вопрос 18. Закон Максвелла для распределения молекул идеального газа по скоростям. Наиболее вероятная скорость.
- •Вопрос 19. Барометрическая формула. Распределение Больцмана.
- •Вопрос 20. Степени свободы молекул. Закон равномерного распределения энергии по степеням свободы. Внутренняя энергия газа – функция состояния.
- •Вопрос 21. Первое начало термодинамики. Работа газа в адиабатном и изопроцессах.
- •Вопрос 22. Молекулярно-кинетическая теория теплоемкости идеальных газов. Недостатки классической теории теплоемкости идеальных газов.
- •Вопрос 23. Адиабатный и политропный процессы. Уравнение Пуассона.
- •Вопрос 24. Обратимые и необратимые процессы. Круговой процесс (цикл). Термический кпд цикла. Цикл Карно. Кпд цикла Карно.
- •Вопрос 25. Энтропия, её статистическое толкование и связь с термодинамической вероятностью. Расчет энтропии в процессах идеального газа.
- •Вопрос 26. Второе начало термодинамики. Второе начало термодинамики для необратимых процессов. Теорема Нернста.
- •Вопрос 27. Реальные газы. Уравнение Ван-дер-Ваальса и его анализ. Внутренняя энергия реального газа.
- •Вопрос 28. Постулаты Эйнштейна. Релятивистский импульс. Закон взаимосвязи массы и энергии.
- •Основные формулы.
- •1. Кинематика поступательного движения.
- •2. Кинематика поступательного и вращательного движения.
- •3. Динамика. Работа, энергия. Законы сохранения.
- •4. Динамика вращательного движения.
- •5. Динамика вращательного движения. Работа, энергия.
- •6. Теория относительности.
- •Молекулярная физика. Термодинамика Молекулярно-кинетическая теория
- •2. Распределение газовых молекул по скоростям
- •3. Элементы физической кинетики
- •4. Первое начало термодинамики. Внутренняя энергии. Работа и теплота
- •6. Второе начало термодинамики
Вопрос 18. Закон Максвелла для распределения молекул идеального газа по скоростям. Наиболее вероятная скорость.
– условие нормировки.
Интеграл
определяет площадь под кривой функции
распределения. Относительное число
молекул
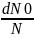 равно вероятности того, что молекула
имеет скорость в интервале от v до v+dv.
Функция имеет максимум при значении
скорости, которое называется «наиболее
вероятная» или «вероятнейшая». Это
означает, что максимальная доля молекул
обладает скоростями, близкими к значению
равно вероятности того, что молекула
имеет скорость в интервале от v до v+dv.
Функция имеет максимум при значении
скорости, которое называется «наиболее
вероятная» или «вероятнейшая». Это
означает, что максимальная доля молекул
обладает скоростями, близкими к значению
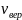 .
.
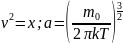

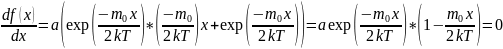
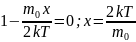
Вероятнейшая
скорость:
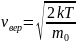 ,
,
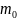 - масса молекулы.
- масса молекулы.
Вопрос 19. Барометрическая формула. Распределение Больцмана.
Молекулы
воздуха всегда находятся в поле тяготения
Земли, если бы не было хаотического
теплового движения, то они упали бы на
Землю, а если бы не было тяготения –
атмосфера бы рассеялась в космос. Найдём
закон изменения давления идеального
газа в зависимости от высоты в однородном
поле тяготения (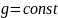 ).
).
Давление
убывает с ростом высоты:
p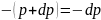
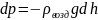
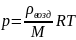
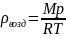
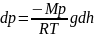
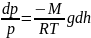
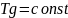
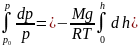
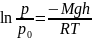
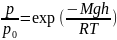
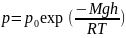
Распределение Больцмана - это распределение концентрации молекул в зависимости от высоты.
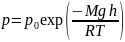
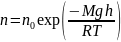 – распределение концентрации молекул
в поле силы тяжести Земли.
– распределение концентрации молекул
в поле силы тяжести Земли.
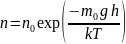 – потенциальная энергия одной молекулы
в поле тяжести.
– потенциальная энергия одной молекулы
в поле тяжести.
Больцман доказал, что эта формула справедлива в случае потенциального силового поля любой природы для совокупности любых одинаковых частиц, находящихся в состоянии хаотического движения.
Вопрос 20. Степени свободы молекул. Закон равномерного распределения энергии по степеням свободы. Внутренняя энергия газа – функция состояния.
Число степеней свободы тела называется наименьшее число независимых координат, которые необходимо задать для того чтобы полностью определить положение тела в пространстве.
Материальная точка, свободно движущаяся в пространстве, имеет три координаты (x,y,z) Одноатомную молекулу можно рассматривать как материальную точку и такая молекула имеет только три ст. св. поступательного движения. Двухатомную молекулу можно представить как гантель с невесомой ручкой, такая молекула имеет ещё 2 степени свободы (вращательное движение).
Таблица 1 – Степени свободы молекул газов
|
Поступательное движение |
Вращательное движение |
Всего |
Одноатомный газ |
3 |
- |
3 |
Двухатомный газ |
3 |
2 |
5 |
Трехатомный Многоатомный газ |
3 |
3 |
6 |
На
каждую степень свободы молекулы в
среднем приходится одинаковая кинетическая
энергия, равная
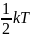 .
Средняя кинетическая энергия молекулы
имеющей
.
Средняя кинетическая энергия молекулы
имеющей
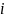 степеней свободы равна
степеней свободы равна
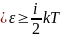
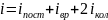
При колебательном движении учитывается две степени свободы с учётом потенциальной и кинетической энергии. Колебательные степени свободы учитываются только при T > 1000 K.
Внутренняя энергия состоит:
• Кинетическая энергия теплового, поступательного и вращательного движения молекул
• Кинетической и потенциальной энергии колебания атомов в молекулах
• Потенциальная энергия, обусловленная межмолекулярным взаимодействием
• Энергия электронных оболочек
• Энергия ядра
Внутренняя энергия – функция состояния. Изменение внутренней энергии идеального газа не зависит от процесса, по какому происходит это изменение. Изменение внутренней энергии равно разности внутренней энергии в конечном состоянии и начальном состоянии.
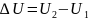
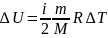
Если пройдя круговой процесс, мы вернем систему в первоначальное состояние, то изменение внутренней энергии равно 0. Поэтому внутренняя энергия является однозначной функцией состояния. Изменить состояние термодинамической системы, т.е. изменить внутреннюю энергию можно двумя способами: совершением работы или передачей теплоты.
