
5. Оптические методы:
1. Спектральный анализ - изучает эмиссионное илиатомное электромагнитное излучение. Каждый химический элемент имеет свой спектр испускания. Изучается с помощью специальных приборов, которые позволяют получать узкие спектральные линии. Каждый химический элемент имеет свой спектр. Так можно определять качественный и количественный элементарный химический состав вещества.
2. Адсорбционная спектроскопия: ультрафиолетовая сп., видимая сп., ИК-сп., рентгеноскопия, гамма-скопия , ЭПР-скопия, ЯМР-скопия . В основе адсорбционной сп. лежит взаимодействие квантов с веществом. Чаще встречается фотометрические методы: фотоколометрические, фотометрические, спектрофотометрические. Основан на измерении света вещества по которому определяется содержание вещества в пробе.
Фотоколометрический метод основан на определении интенсивности окрашивания по сравнению со стандартным. Производится визуально.
Фотометричесикй метод – определение светопоглощения производится с помощью фотоэлемента, т.е. используется диапазон длин волн ЭМИ.
Спектрофотометрический анализ – используется спектрофотометры, которые позволяют измерять светопоглощение при монохроматич. определённой длины волны света.
Сравнение: спектрофотометрия как физический метод используется для измерения концентрации веществ по их спектропоглощению. Физико-химические методы. Используется хим. реакция. Определяемое вещество с помощью реактивов в результате хим. реакции превращается в окрашиваемое соединение . анализ обладает чувствительностью 1-0,001 % .
Также используется люминисцентный анализ.
6.электрохимические методы
Электровесовой метод . Определённое вещество выделяет электролиз чаще на катоде. Электрод взвешивают до и после и по окончании опыта для обнаружения разницы в весе. Этот метод используется широко. Характеризуется высокой прочностью, однако полное осаждение требует длительного электролиза.
Потенциометрическое титрование. Основано на титровании раствора определённого вещества.
Потенциометрия. Измерение ЭДС, концентрации катионов и анионов.
Амперометрическое титрование. Это титрование можно рассматривать как вариант потенциометрического титрования , отличающегося тем, что в нём применятеся микроэлемент. Применяется , когда трудно подобрать индикатор и электрод.
Полярографиеский анализ. Для определения концентрации вещества.
Кондуктометрическое титрование с помощью прибора кондуктометра.
Недостатки: присутствие посторонних элементов увеличивающих электропроводность, что уменьшает чувствительность и прочность.
32.Рефрактометрия (от лат. refractus - преломленный и греч. metreo - измеряю) - метод анализа, основанный на явлении преломления света при прохождении из одной среды в другую. Преломление света, то есть изменение его первоначального направления, обусловлено различной скоростью распределения света в различных средах.
Рефрактометрический метод является одним из самых простых физико-химических методов анализа с затратой очень небольших количеств анализируемого вещества и проводится за очень короткое время. В фармацевтическом анализе этот метод применяется для идентификации лекарственных веществ, установления их чистоты и количественного анализа.
Рефрактометрический метод анализа основан на измерении показателя преломления анализируемого вещества. Показатель преломления - одно из основных физических свойств вещества: индивидуальное вещество, свободное от примесей, характеризуется определенным показателем преломления. Когда луч света переходит из одной прозрачной среды в другую, на границе сред направление его изменяется - луч преломляется.
При этом отношение синуса угла падения луча (α) к синусу угла преломления (β) для двух соприкасающихся сред есть величина постоянная, называемая показателем преломления (n).
Показатель преломления также равен отношению скоростей распространения света в этих средах:
![]()
Физический смысл показателя преломления n закл-ся в том, что он определяется отношением скорости света в вакууме к скорости света в данной среде n=c/v(скорость).
Величина показателя преломления зависит от природы вещества, длины световой волны, концентрации раствора, температуры.
Определение показателя преломления производят с помощью специального прибора, называемого рефрактометром. На практике применяются рефрактометры различных систем: лабораторный- РЛ, универсальный - РЛУ и др.
Показатель преломления обычно измеряют при 20 °С и длине волны 589,3 нм линии D спектра натрия (nD20). Пределы измерения показателей преломления 1,3-1,7.
33. Принцип работы на рефрактометрах основан на определении показателя преломления методом предельного угла (угол полного отражения света) (рис.2).
Главной деталью рефрактометра является измерительная призма из оптического стекла, показатель преломления которого известен. Входная грань измерительной призмы, соприкасающаяся с исследуемым веществом, служит границей раздела, на которой происходит преломление и полное внутреннее отражение луча. Через выходную грань измерительной призмы в зрительную трубу наблюдают преломление или отражение света.
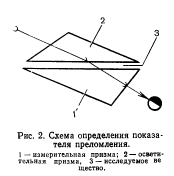
Луч света попадает на призму, на которую наносится слой исследуемой жидкости, преломляясь в ней рассеивается. При этом рассеянные лучи распр-ся во всех направлениях, в том числе параллельно измерительной призме. Далее эти лучи пройдя сквозь эту призму попадают в отсчетное устройство. Если граница свет-тень оказалась окрашенной и размытой, то с помощью компенсатора добиться четкой черно-белой границы. Путем поворота спец рычага необ-мо совместить границу свет-тень с маркером отчетного устройства, при этом маркер показывает на встроенной шкале непосредственно значение коэф-та преломления.
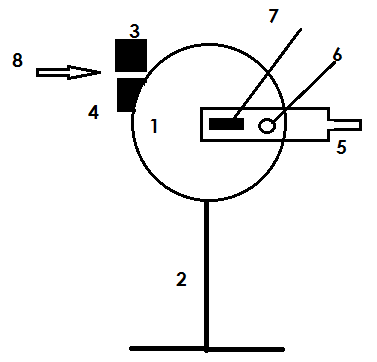
Конструкция рефрактометра РПЛ-3:
1-корпус, 2-штатив, 3-вспомогательная откидная призма с матовой нижней гранью, 4-измерительная призма, 5-рукоятка отчетного устройства, 6-окуляр, 7- рукоятка компенсатора, 8-луч света.( попадает на призму из окна или от спец-го осветителя.
34.Дипольный момент–важ.молекул. константа, хар-щая электр. симметрию мол-лы.Знание вел-ны дип.мом.необходимо для из природы химсвязи, оценки прочности дон-акцепт.и межмолекул.св., для квантово-хим. расчетов. По величине дипольного момента мож. судить об изомерии и конформации органсоединений, конфигурации координац. узлов комплексов, о взаимном вл. атомов и св.в мол.
Величина
электрического дипольного момента(μ)
опред.соотношением:
![]() ,где
l - радиус-вектор, напр.от центра
тяжести(-)электр.зарядак центру тяжести
(+)заряда, абсолют. вел.каж.заряда q.
Принято изм.дипмом.в ед. Дебая: 1 D =
1·10-18 эл.-ст.ед.В системе единиц СИ
1D= 3.34·10-30 Кл*м.
Причиной
появ.дип.мом. явл.:1–это разл. в природе
состав молекулу атомов. В простейшем
случае для двухатомной молμ = 0,если
она сост. из 2одинак.атомов. Это относится
к H2,
O2,
N2 и
т.д. В двухатомной мол. с атом. Разн.
природы прояв.пост. дип.мом,т.к.,
вследст.разн.электроотрицательности,харак.спос-сть
ат.оттягивать электроплотность,появл.асимметрия
электр. плотности.2– раз. гибрид.сос-ния
орбиталей атомов.например, для связи
H-Cl, образ.1s-орбит.Н и 3p-орбитальюCl,
вслед.разл. формы s- и p-орбиталей, центр
тяжести заряда перекрывания смещен в
сторону Нна ΔL, засч. чего возн. допол.,
т.н.гомеополярный дип.мом.
,где
l - радиус-вектор, напр.от центра
тяжести(-)электр.зарядак центру тяжести
(+)заряда, абсолют. вел.каж.заряда q.
Принято изм.дипмом.в ед. Дебая: 1 D =
1·10-18 эл.-ст.ед.В системе единиц СИ
1D= 3.34·10-30 Кл*м.
Причиной
появ.дип.мом. явл.:1–это разл. в природе
состав молекулу атомов. В простейшем
случае для двухатомной молμ = 0,если
она сост. из 2одинак.атомов. Это относится
к H2,
O2,
N2 и
т.д. В двухатомной мол. с атом. Разн.
природы прояв.пост. дип.мом,т.к.,
вследст.разн.электроотрицательности,харак.спос-сть
ат.оттягивать электроплотность,появл.асимметрия
электр. плотности.2– раз. гибрид.сос-ния
орбиталей атомов.например, для связи
H-Cl, образ.1s-орбит.Н и 3p-орбитальюCl,
вслед.разл. формы s- и p-орбиталей, центр
тяжести заряда перекрывания смещен в
сторону Нна ΔL, засч. чего возн. допол.,
т.н.гомеополярный дип.мом.
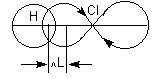
Сх.происхождения гомеополярного диполя.
Мол.HCl, HBr, HI им.пост. дип.мом= соответственно,1.95 D, 0.79 D, 0.40 D. Др.вклады в сумдип. мом.возн.из-за асимметрии связ.и несвяз. атомных орбиталей вслед. их гибр-ции. Так, дипмом.NH3=1.46 D,в осн.обуслов. мом.несвяз. пары е азота. Мол.рефракция-это произв.мол. массы М на удел.рефракцию R,т.е. молек.рефракция=MR. Удельная рефракция R вычисл.на основ.эксперим. опр.показ.преломления и плотности. Мол.рефракция яв.аддитивным (суммарным) св-вом,она=сумме атом.реф-ций эл.,вход.в состав мол-лы. При этом ат.ре-ции нек.эл-ов, напр.»О», им.разл.вел-ны в завис.от того, как св.дан. атом:атом «О», вход.в состав гидроксил. группы -О-Н и в состав эфира R-О-R,буд. Им.разл. ат. рефракцию. Наличие в мол.2-ых и 3-ыхсв.увел.мол.рефракцию на опр.вел-у. Пок.преломления-решающ.физ. конст.- явл.пок. чистоты в-ва. Опред.пок. прелом.произв.при пом.рефрактометров. Рефрактометры дол.обесп. точность опред. пок.преломления не менее чем до 0,0005при t=20 С и длине волны линии D спектра Na(589,3 нм) Точность пок.рефрактометров пров. по дистил.воде или эталонным жидкостям. Реф-ция не зав.от t, поскольку умен.пок.прелом. при повыш.t ком-тся одновр. Умен.пло-ти. Рефракция не зав. также от агр.с-ния в-ва.
41. Электрофорез в полиакриламидном геле (сокр. электрофорез в ПААГ, ПААГ электрофорез; англ. PAGE, Polyacrylamide Gel Electrophoresis) — метод молекулярной биологии и биохимии, используемый для разделения белков и нуклеиновых кислот, основанный на движении заряженных биологических макромолекул в постоянном электрическом поле. Разделение в полиакриламидном геле происходит за счёт различий заряда разделяемых молекул и отличий молекулярных масс, а также от конфигурации молекул. Разделяют т. н. неденатурирующий, или нативный ПААГ-электрофорез (при котором разделяемые биологические макромолекулы в процессе электрофореза остаются в нативном состоянии) и денатурирующий ПААГ-электрофорез (при котором пробы предварительно денатурируют, в случае нуклеиновых кислот используют непродолжительное нагревание пробы с формамидом либо глиоксалем, для денатурации белков обычно используют кипячение пробы в буфере, содержащем сильный ионный детергент (обычно додецилсульфат натрия) и агент, разрушающий четвертичную структуру белка за счёт разрушения дисульфидных мостиков между глобулами белка и внутри полипептидной цепи — бета-меркаптоэтанолом). В процессе денатурирующего ПААГ-электрофореза молекулы сохраняются в денатурированном состоянии за счёт наличия в геле хаотропных агентов (обычно мочевины) в случае ПААГ-электрофореза нуклеиновых кислот и белков и наличия ионных (например додецилсульфата натрия, цетилтриметиламмоний бромида) и неионных (например tween-20) детергентов.
В случае электрофореза белков в полиакриламидном геле метод обычно используют в модификации Леммли (Laemmli)[1]
Также электрофорез в полиакриламидном геле применяют для разделения коротких фрагментов нуклеиновых кислот, например, ДНК-электрофорез, например, при секвенировании по Сэнгеру. Кроме этого, ПААГ-электрофорез применяют для визуализации в методах ПДРФ и ПЦР методе.
Различают также т. н. диск-электрофорез (от англ. discontinious), при котором в геле в процессе электрофоретического разделения белков на границе между концентрирующим и разделяющим гелями создаётся градиент pH, за счёт чего достигается лучшее разделение белковых молекул.
4.ФХМИ
Все ФХМ подразделяются на 3 группы:
-оптические
-электрохимические
-хроматографические
Главной особенностью этих методов является оч высокая чувствительность и точность.
Чувствительность этих методов
К оптическим методам относятся : спектральный анализ, адсорбционная спектроскопия,фотометрия,фотоколометрия, спектрофотометрия,люминисцентный анализ.
К электрохим. Отн.:электровесовой анализ,потенциометрическое титрование , потенциоменрия,амперометрическое титрование,полярографический анализ, кондуктометрическое титрование
Хроматографические методы: ионообменная хр., газовая или газожидкостная хр., жидкостнораспределительная хр., гель-хр., хр. по сродству, хр. на бумаге и т.д.
др. методы: масс-спектральный, радиометричекие, метод изотропной метки.
29.Основ цель рентгеноструктурного анализа(Р.А) кристаллов закл-ся в том, чтобы путем соотв-го рассмотрения картины рассеяния рентг лучей получить изоб-е структуры, рассеивающей рентг лучи. Эта задача решается в два этапа: сначала измеряют интенсивности излучения, рассеянного объектом, после чего путем преобразования картины рассеяния получают изображение. В аналогичном оптическом случае, когда объект, рассеивающий свет, наблюдают с помощью микроскопа. 2-м аспектом Р.А. кристаллов явл прецизионное измерение межатомных расстояний и углов между направлениями химических связей.Из изложенного следует, что рентгеноструктурный анализ кристаллов далеко не всегда дает правильное представление о строении соответствующих индивидуальных молекул или ионов.Закон Брэгга Вульфа определяет зависимость угла отраж-я рентг лучей(α) от длины волны излучения(λ) и межплоск-го расстояния, от кот-го происх отражение,-явл-ся основным законом дифракции рентг лучей в кристалле.Если исп-ть монохроматич изл-е, тоЗ.Брегга Вульфа м/записать:2 d/n sin α=λ, где n- порядок отражения.
