
- •Влияние температуры
- •Влияние концентрации
- •Ядро атома
- •Изотопы
- •Характерные кристаллические решётки
- •15. Растворы
- •Значение понятия
- •Понижение температуры кристаллизации растворов
- •[Править]Повышение температуры кипения растворов
- •19. Гидролиз
- •Степень гидролиза
- •20. Гидролиз солей многоосновных кислот и оснований
- •22. Понятие о протолизе
- •Вывод значения ионного произведения воды
- •Реакция ионного обмена — одна из видов химической реакции, характеризующаяся выделением в продукты реакции воды, газа илиосадка. Изображение реакций ионного обмена
- •Правила написания реакций двойного обмена
- •2. Если в результате реакции выделяется нерастворимое в воде вещество.
- •3. Если в результате реакции выделяется газообразное вещество.
- •Реакция нейтрализации
- •24. Виды окислительно-восстановительных реакций
- •[Править]Вывод уравнения Нернста
- •Первый закон Фарадея
- •Вывод закона Фарадея
- •Второй закон Фарадея
Значение понятия
Смысл параметра ясен из определения каждого из коллигативных параметров: они зависят от концентрации в растворе частиц растворённого вещества. Неэлектролиты в растворе недиссоциируют, стало быть, каждая молекула неэлектролита образует в растворе лишь одну частицу. В свою очередь, электролиты в растворе под влиянием сольватации частично или полностью распадаются на ионы, образуя при этом несколько частиц на одну диссоциировавшую молекулу. Соответственно, и коллигативные свойства данного раствора (аддитивные величины) зависят от содержания в нём частиц (ионов) каждого типа из тех, которым принадлежат частицы, образовавшиеся в растворе в результате диссоциации исходной молекулы, — раствор представляется как бы смесью растворов каждого из типов частиц. Например, раствор хлорной извести содержит три типа частиц — катионыкальция, хлорид-анионы и гипохлорит-анионы. Итак, изотонический коэффициент показывает, насколько в растворе электролита больше частиц по сравнению с раствором неэлектролита аналогичной концентрации, и связан со способностью вещества распадаться в растворе на ионы, то есть, со степенью диссоциации. Если формульная единица или молекула содержит n ионов (или атомов при полярных связях, в растворе превращающихся в ионы), количество исходных молекул равно N, а степень диссоциации соединения —α, то количество диссоциировавших молекул равно N·α (при этом образуются N·α·n ионов), а общее количество частиц в растворе равно ((N — N·α) + N·α·n).
Изотонический же коэффициент равен отношению:
![]() .
.
17.
Понижение температуры кристаллизации растворов
Условием кристаллизации является равенство давления насыщенного пара растворителя над раствором давлению пара над твёрдым растворителем. Поскольку давление пара растворителя над раствором всегда ниже, чем над чистым растворителем, это равенство всегда будет достигаться при температуре более низкой, чем температура замерзания растворителя. Так, океанская вода начинает замерзать при температуре около минус 2 °C.
Разность между температурой кристаллизации растворителя T°fr и температурой начала кристаллизации раствора Tfr есть понижение температуры кристаллизации.
Понижение температуры кристаллизации бесконечно разбавленных растворов не зависит от природы растворённого вещества и прямо пропорционально моляльной концентрациираствора.
![]()
Поскольку по мере кристаллизации растворителя из раствора концентрация последнего возрастает, растворы не имеют определённой температуры замерзания и кристаллизуются в некотором интервале температур.
[Править]Повышение температуры кипения растворов
Жидкость кипит при той температуре, при которой общее давление насыщенного пара становится равным внешнему давлению. Если растворённое вещество нелетуче (то есть давлением его насыщенных паров над раствором можно пренебречь), то общее давление насыщенного пара над раствором равно парциальному давлению паров растворителя. В этом случае давление насыщенных паров над раствором при любой температуре будет меньше, чем над чистым растворителем, и равенство его внешнему давлению будет достигаться при более высокой температуре. Таким образом, температура кипения раствора нелетучего вещества Tb всегда выше, чем температура кипения чистого растворителя при том же давлении T°b.
Повышение температуры кипения бесконечно разбавленных растворов нелетучих веществ не зависит от природы растворённого вещества и прямо пропорционально моляльной концентрации раствора
![]()
Криоскопия (от греч. κρύο — холод и греч. σκοπέω смотрю) — метод исследования растворов, в основе которого лежит измерение понижения температуры замерзания раствора по сравнению с температурой замерзания чистого растворителя. Был предложен Ф. Раулем в 1882 году.
Давление пара над раствором нелетучего вещества практически полностью определяется давлением пара растворителя и может быть выражено уравнением (согласно закону Рауля):
![]()
где x1 — мольная доля растворителя.
Видно, что оно ниже, чем давление пара над чистым растворителем, и снижается с ростом концентрации растворенного вещества.
В то же время при замерзании раствора давление пара над твердой фазой должно быть равно давлению пара над жидкостью. Если при замерзании раствора выделяется чистый растворитель, то давление пара над жидким раствором должно быть равно давлению пара над твердым чистым растворителем. Как было показано выше, давление пара над раствором ниже давления пара над чистым жидким растворителем, а следовательно, и соответствующее температуре замерзания равновесие для раствора будет устанавливаться при меньших температурах, чем для чистого растворителя. Это явление имеет важное значение в природе и технике.
Из приведенного выше выражения (закона Рауля), с учетом уравнения Клапейрона — Клаузиуса можно показать[1], что изменение температуры замерзания ΔTcr для разбавленных растворов может быть рассчитано по формуле:
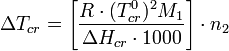
где ΔHcr — энтальпия замерзания (кристаллизации);
M1 — молярная масса растворителя;
n2 — моляльная концентрация растворенного вещества.
Здесь выражение в квадратных скобках зависит только от природы растворителя — это так называемая криоскопическая постоянная растворителя k:
![]()
Для воды k = 1,84 K, для железа 110 K[1].
Измеряя ΔTcr, можно определить молярную массу растворенного вещества, в соответствии с выражением:
![]()
где a — число граммов растворенного вещества, приходящееся на 1000 граммов растворителя.
Криоскопия может быть использована для определения активности растворителя, в соответствии с соотношением[2]:
![]()
Кроме того, с помощью криоскопии можно определять степень диссоциации слабых электролитов, чистоту вещества, изучать комплексообразование в растворах и пр.
Эбулиоскопия (от лат. ebulio — вскипаю) — метод исследования растворов, основанный на измерении повышения их температуры кипения по сравнению с чистым растворителем. Используется для определения молекулярной массы растворенного вещества, активности растворителя, степени диссоциации (или изотонического коэффициента).
Температура кипения жидкости — такая температура, при которой давление пара над жидкостью равно внешнему давлению. В то же время давление пара над растворомнелетучего вещества практически полностью определяется давлением пара растворителя и, в соответствии с законом Рауля, может быть выражено уравнением:
где x1 — мольная доля растворителя.
Видно, что при повышении концентрации растворенного вещества давление пара над раствором будет снижаться, а следовательно, при неизменном внешнем давлении, будет расти температура кипения.
С учетом уравнения Клапейрона — Клаузиуса можно показать[1], что изменение температуры кипения раствора (ΔTboil) может быть рассчитано по формуле:
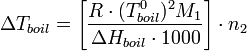
где ΔHboil — энтальпия испарения;
M1 — молярная масса растворителя;
n2 — моляльная концентрация растворенного вещества.
Дробь в квадратных скобках в этом выражении зависит только от свойств растворителя — это так называемая эбулиоскопическая константа растворителя ε. Она равна повышению температуры кипения одномоляльного раствора.
Если известны изменение температуры кипения и концентрация раствора, можно определить молярную массу растворенного вещества:
![]()
где a — число грамм растворенного вещества на 1000 г растворителя. Этот метод применим для разбавленных растворов нелетучих веществ и неэлектролитов.
Эбулиоскопический метод позволяет судить о состоянии вещества в растворах электролитов, так как для последних:
![]() ;
;
где i — изотонический коэффициент.
С помощью эбулиоскопии можно определить и активность растворителя, в соответствии с формулой[2]:
![]()
О́смос (от греч. ὄσμος — толчок, давление) — процесс односторонней диффузии через полупроницаемую мембрану молекул растворителя в сторону бо́льшей концентрации растворённого вещества (меньшей концентрации растворителя).
Осмотическое давление (обозначается π) — избыточное гидростатическое давление на раствор, отделённый от чистого растворителя полупроницаемой мембраной, при котором прекращается диффузия растворителя через мембрану. Это давление стремится уравнять концентрации обоих растворов вследствие встречной диффузии молекул растворённого вещества и растворителя.
![]() ,
,
где i — изотонический коэффициент раствора; C — молярная концентрация раствора, выраженная через комбинацию основных единиц СИ, то есть, в моль/м3, а не в привычных моль/л; R — универсальная газовая постоянная; T — термодинамическая температура раствора.
Обратный осмос — прохождение воды или других растворителей через полупроницаемую мембрану из более концентрированного раствора в менее концентрированный в результате воздействия давления, превышающего разницуосмотических давлений обоих растворов.[1] При этом мембрана пропускает растворитель, но не пропускает некоторые растворённые в нём вещества.
Обратный осмос используется в различных технологиях очистки воды от примесей, в том числе для опреснения воды и очищения питьевой воды для различных целей с начала 1970-х годов.
18. По степени диссоциации электролиты делят на сильные, слабые, средней силы.
Сильные:
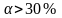 .
Неорганические к-ты (HCl,
HBr, HI,
H2SO4,HClO4,HMnO4),
основания щелочных и щелочноземельных
металлов (Ca, Sn,
Ba) и почти все соли.
.
Неорганические к-ты (HCl,
HBr, HI,
H2SO4,HClO4,HMnO4),
основания щелочных и щелочноземельных
металлов (Ca, Sn,
Ba) и почти все соли.Слабые:
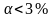 .
Неорганические кислоты (HSO3,
HF, HCN, HCNS,
H2S,
H2Se,
H3PO3),
органические кислоты, основания (NH4OH,
AlO3, PO3,d-элементы),
соли (Fe(CNS)3,
Hg2Cl2)
.
Неорганические кислоты (HSO3,
HF, HCN, HCNS,
H2S,
H2Se,
H3PO3),
органические кислоты, основания (NH4OH,
AlO3, PO3,d-элементы),
соли (Fe(CNS)3,
Hg2Cl2)Средние:
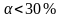 .
Неорганические кислоты (H2CrO4,
MnO4, HCOOH,
H3PO4,
H2SO3),
основания (Mn(OH)2).
.
Неорганические кислоты (H2CrO4,
MnO4, HCOOH,
H3PO4,
H2SO3),
основания (Mn(OH)2).
С разбавлением раствора
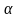 увеличивается.
увеличивается.
Слабые электролиты
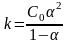 - разведение Оствальда, где С0 –
число образовавшихся ионов.
- разведение Оствальда, где С0 –
число образовавшихся ионов.
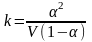 .
.
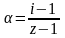 .
(Z – число частиц,
образующихся из 1 молекулы).
.
(Z – число частиц,
образующихся из 1 молекулы).
Чем меньше , тем слабее электролит.
Слабые многоосновные кислоты и многоосновные основания в водных растворах диссоциируют ступенчато.
Сильные электролиты.
В виду высокой концентрации ионов в растворах сильных электролитов образуются частицы (ассоциаты или ионные пары).
В ионных парах ионы разделены одним или более слоями.
Для растворов электролитов в качестве Д.М. применяется активность ( - термоядерная характеристика (эффективная концентрация, в соответствии с которой, ионы проявляют себя в действии))
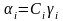 ,
где
,
где
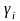 - коэффициент активности. Этот коэффициент
характеризует отклонение поведения
реального раствора от идеального. Для
учета действия всех ионов на активность
каждого из них Льюис и Рендел в 1918 году
ввели характеристику – ионная сила
раствора.
- коэффициент активности. Этот коэффициент
характеризует отклонение поведения
реального раствора от идеального. Для
учета действия всех ионов на активность
каждого из них Льюис и Рендел в 1918 году
ввели характеристику – ионная сила
раствора.
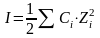 ,
где
,
где
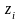 - заряд i-ого иона.
- заряд i-ого иона.
Ввиду того, что нельзя
экспериментально определить коэффициент
активности отдельного иона, используют
средний коэффициент активности.
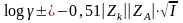 - уравнение Де-Бойля и Хюпкеля.
- уравнение Де-Бойля и Хюпкеля.
Для растворов сильных электролитов в уравнение З.Д.М. включают не аналитические концентрации, а соответствующие активности ионов.
