
Опиатные анальгетики
В течение многих лет опиум – млечный сок, выделяющийся при повреждении зеленых семенных коробочек мака, – использовался в меди-цине в качестве снотворного и общего обезболивающего средства (аналь-гетика). Еще в ХIХ и в начале двадцатого века во всех домашних аптечках были опийные капли, которые принимали при болях в желудке и при кишечных расстройствах, а в аптеках середины ХХ века можно было купить один из алкалоидов опиума кодеин в таблетках от кашля. При изучении химического состава опиума из него было выделено основное действующее вещество, получившее название морфин. Обезболивающее действие морфина сопровождается целым рядом побочных эффектов, среди которых эйфория, развитие толерантности (при длительном приеме доза должна постоянно увеличиваться), запоры и подавление дыхатель-ного рефлекса, поэтому для снятия часто повторяющихся или постоянных болей морфин непригоден. Однако в начале ХХ связанные с этим опас-ности недооценивались и многие пациенты и даже врачи (М.Булгаков) стали наркозависимыми от частого использования морфина, тем более что других средств для эффективного обезболивания тогда просто не сущест-вовало.
После установления химического строения морфина были предприня-ты многочисленные попытки по синтезу его структурных аналогов с целью получения средства для обезболивания, которое было бы лишено нежела-тельных побочных эффектов, сопровождающих лекарственное использо-вание этого вещества. Алкалоиды мака и их производные представляют собой классический пример для демонстрации биоактивности через хеморецепцию. Они взаимодействуют с соответствующими рецепторами стереоспецифично и их оптические изомеры могут очень сильно отли-чаться по биоактивности. Еще одним следствием этого является возмож-ность получения антагонистов в результате сравнительно небольших изменений в строении молекул. Так, например, замена в молекуле морфина группы NСН3 на группу NСН2СН=СН2 приводит к антагонисту морфина, налорфину, который использовался для спасения наркоманов, принявших слишком высокую дозу наркотика. Сейчас от налорфина отказались из-за его галлюциногенных свойств.
Молекула морфина не имеет подвижных структурных элементов, она жестко фиксирована в виде буквы Т. При упрощении структуры морфина было установлено, что обезболивающий эффект сохраняется до тех пор, пока в молекуле остается фрагмент, в котором ароматическое ядро связано с четвертичным атомом углерода, а к этому атому углерода мостиком из двух атомов углерода присоединена третичная аминогруппа.

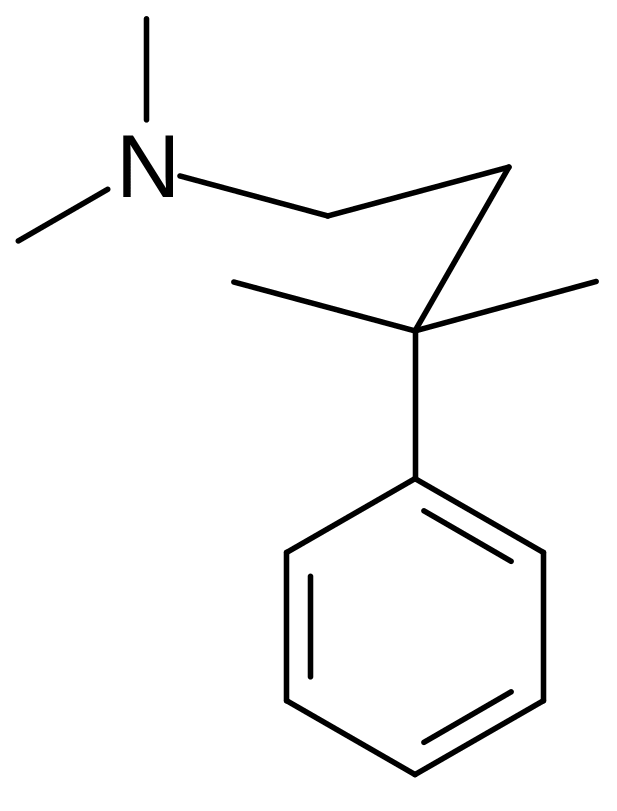
Эффективность веществ заметно возрастает в тех случаях, когда атом азота включен в пиперидиновый цикл и в фенильном остатке в мета-поло-жении к заместителю с атомом азота находится гидроксильная группа. В качестве примера можно привести петидин, у которого гидрофильный участок молекулы морфина (гидроксильная группа и атом кислорода дигидрофуранового фрагмента) заменен на этоксикарбонильную группу:
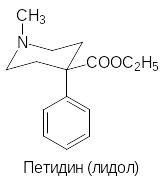
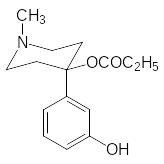
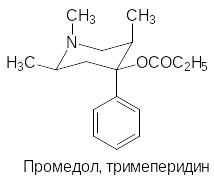
Переход к пропионилоксигруппе с введением гидроксильной группы в мета-положение увеличивает активность петидина в тридцать раз, но более доступным и эффективным средством оказался промедол.
Определенная жесткость молекулы может поддерживаться и за счет электрофильно-нуклеофильных взаимодействий структурных элементов молекулы. Так, очевидно, что в молекуле метадона и пропоксифена нук-леофильный атом азота и электрофильный углерод карбонильной группы создают условия для стабильного расположения этих функциональных групп в непосредственной близости друг от друга.
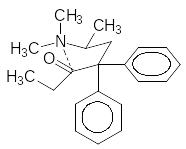
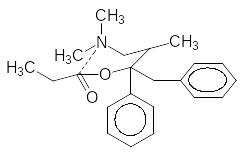
Метадон Пропоксифен
Из двух оптических изомеров метадона активен только L-изомер, пре-восходящий по анальгетической активности морфин в два раза. Это соеди-нение предлагается использовать для лечения щадящим способом наркоза-висимых больных путем замены героина метадоном с постепенным сниже-нием вводимой в стационарных условиях дозы. Однако индивидуальный подбор методики очень проблематичен и часто при этом героиновый наркоман становится метадоновым наркоманом, а лечение метадоновой зависимости дается еще труднее, чем лечение героиновой зависимости.
Еще одна иллюстрация зависимости анальгетической активности от строения представлена леворфанолом и декстрометорфаном:
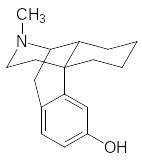
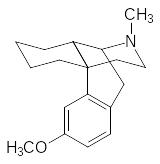
Первое из этих соединений – леворфанол – в четыре раза превосходит по анальгетической активности морфин, тогда как второе может быть использовано только для успокоения кашля.
Замена в структуре леворфанола метильной группы у атома азота на аллильную и циклопропилметильную приводит к мощным антагонистам морфина, но они являются галлюциногенами и отмечены многими други-ми недостатками, присущими морфину.
И все же опыты по модификации заместителей у атома азота привели к получению эффективных анальгетических препаратов. Одним из них является близкий по свойствам к промедолу просидол:
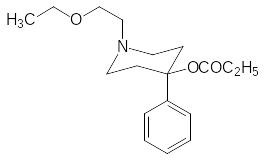
Другое направление поисков привело к получению пентазоцина с диметилаллильным заместителем у атома азота и с гидроксигруппой в фенильном ядре и к еще более эффективному феназоцину:

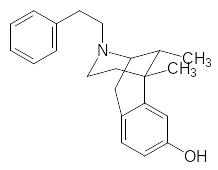
А модификация структуры феназоцина с целью получения соедине-ний с остатком пропионовой кислоты, который оказался важным структур-ным элементом многих опиатных анальгектиков, привела к одному из самых эффективных обезболивающих средств фентанилу:
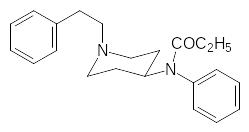
Его эффективная доза (ЕД50) составляет около 0,01 мг/кг при ЛД50 = 3,5 мг/кг. Фентанил отличается очень быстрым наступлением анальгезии-рующего действия (при внутривенном введении максимальный эффект достигается через 1-3 минуты), при разовом введении анальгезирующее действие непродолжительно, около 30 минут. У других структурных аналогов фентанила эффективная доза может быть в пределах 0,0001-0,0007 мг/кг.
Очень быстрым действием отличается ремифентанил:
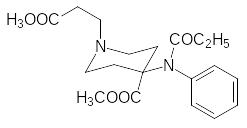
Его получают из N-бензилпиперидона по схеме:

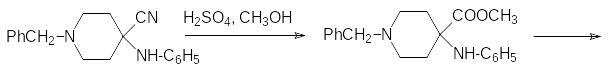
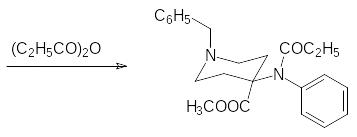
Для перевода нитрильной группы в метоксикарбонильную можно также использовать реакцию образования иминоэфира (хлористый водород в метаноле) с последующим гидролизом иминогруппы. Затем гидрированием на палладии снимают бензильную защиту и алкилируют метиловым эфиром акриловой кислоты:
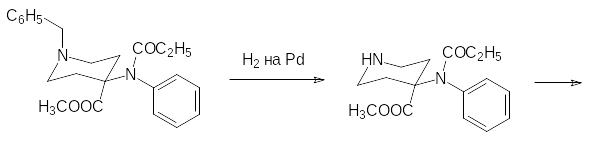
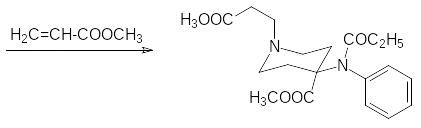
Очень сильным опиоидным анальгетиком является соединение, в котором отсутствует пиперидиновый цикл:
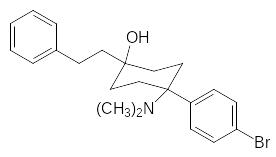
Экзоциклическая диметиламинная группа есть в еще одном обез-боливающем средстве со свойствами опиатных анальгетиков трамадоле (трамале), у которого цис-изомер (вторая формула) неактивен:
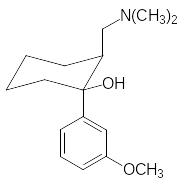
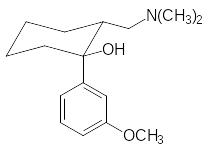
Как обезболивающее средство трамадол слабее морфина, но, тем не менее, его часто используют для купирования послеоперационных болей и для облегчения состояния раковых больных, так как отрицательные побочные эффекты морфина у него выражены не столь ярко.
Наряду с морфином в опиуме содержатся другие алкалоиды, которые были использованы в качестве исходных продуктов для получения анта-гонистов морфина и опиатных анальгетиков с усложненной по сравнению с морфином структурой. В качестве примера можно привести получение налоксона, используемого для лечения героиновой передозировки. Для его получения используют тебаин:
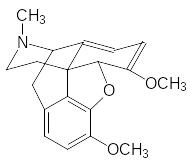
Этот алкалоид содержится в опии в количестве около 0,5%, он очень токсичен и в отличие от морфина не обладает наркотическим действием. При окислении тебаина пероксидом водорода образуется кетопроизводное, которое деметилируют по атому азота действием бромциана, гидролизуют образующийся цианамид и алкилируют вторичную аминную группу аллилбромидом, после этого переводят метоксигруппу в гидроксильную группу действием трибромида бора:
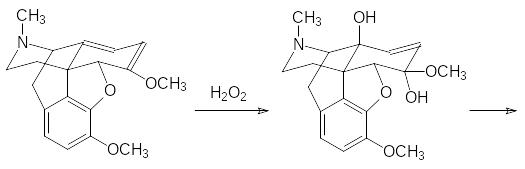
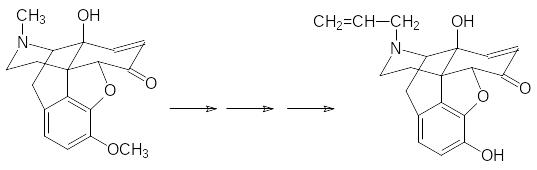
Налоксон является «чистым» опиатным антагонистом, то есть он полностью лишен морфиновой активности.
Используя в качестве исходного соединения тебаин, получают также бупренорфин, эффективный в качестве опиатного анальгетика в дозе 0,2 мг (таблетка пентазоцина содержит 50 мг субстанции). При взаимодействии тебаина с трет-бутил-винил-метил-карбинолом по реакции Дильса-Альдера получают аддукт, который деметилируют по атому азота по анна-логии с предыдущим, алкилируют образовавшийся вторичный амин циклопропилметилбромидом, переводят связанную с ароматическим ядром метоксигруппу в гидроксигруппу и гидрируют двойную связь. Бупренорфин имеет следующее строение:
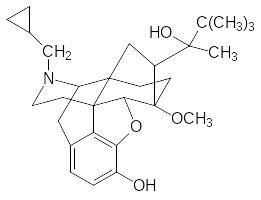
По интенсивности связывания с выделенным из ткани мозга опиат-ным рецептором бупренорфин превосходит морфин примерно в 20 раз, тогда как по анальгетической активности он лучше его в несколько тысяч раз. Это расхождение легко объясняется повышенной липофильностью бупренорфина по сравнению с морфином, что обеспечивает ему более легкое прохождение гематоэнцефалического барьера. Различие в липо-фильности лежит также в основе более сильного обезболивающего и наркотического эффекта героина, который представляет собой диацетиль-ное производное морфина.
Пример фентанила показывает насколько далеко различаются иногда строение прототипа и модифицированной в результате многочисленных проб и ошибок структуры. После того, как была показана роль пипериди-нового цикла в проявлении анальгетической активности, были проведены многочисленные опыты по синтезу различных замещенных пиперидинов, увенчавшиеся разработкой нескольких препаратов, сохраняющих значе-ние до настоящего времени и препаратов, которые очень скоро пришлось запретить. Здесь нельзя не назвать препарат фенциклидин (сернил, РСР), который был получен в 1954 году и после непродолжительных клини-ческих испытаний внедрен в фармакологическую практику в качестве внутривенного анестетика (он будет рассмотрен в разделе, относящемся к психотическим средствам):
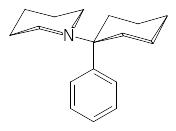
При изучении механизма действия алкалоидов мака было установ-лено, что они являются агонистами эндогенных веществ пептидной приро-ды, выполняющих функции нейромедиаторов и нейрогормонов. В работе мозга участвуют около 15 таких олиго- и полипептидов, но они продуци-руются и многими другими клетками организма теплокровных. В част-ности, клетки слизистой оболочки желудка также генерируют значитель-ные количества одного из главных представителей эндогенных веществ этой группы – Мет-энкефалина. Чаще всего структура Мет-энкефалина включена в более крупные пептидные молекулы (динорфины, эндорфины) и в нужное время он выделяется из этих пептидов в результате их гидро-лиза высокоизбирательными ферментами. Роль опиоидных пептидов многогранна, и полной картины, отражающей все особенности этих регу-ляторов высшей нервной деятельности, еще не существует. В то же время можно предполагать, что они предназначены для модуляции болевого сигнала (их действие противоположно эффекту усиливающих болевой сигнал простагландинов), кроме того, они являются нейромедиаторами внутреннего подкрепления, например, это чувство удовлетворения от вкусного и сытного обеда.
Известны два пентапептидных энкефалина: Тир-Гли-Гли-Фен-Мет (Мет-энкефалин) и менее активный Лей-энкефалин, у которого С-концевая гидрофобная аминокислота представлена лейцином. Большая и гибкая молекула энкефалина на первый взгляд очень сильно отличается от моле-кулы морфина, особенно когда ее представляют без учета пространст-венного расположения функциональных групп в пептидной молекуле:
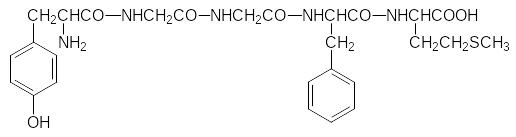 и
и
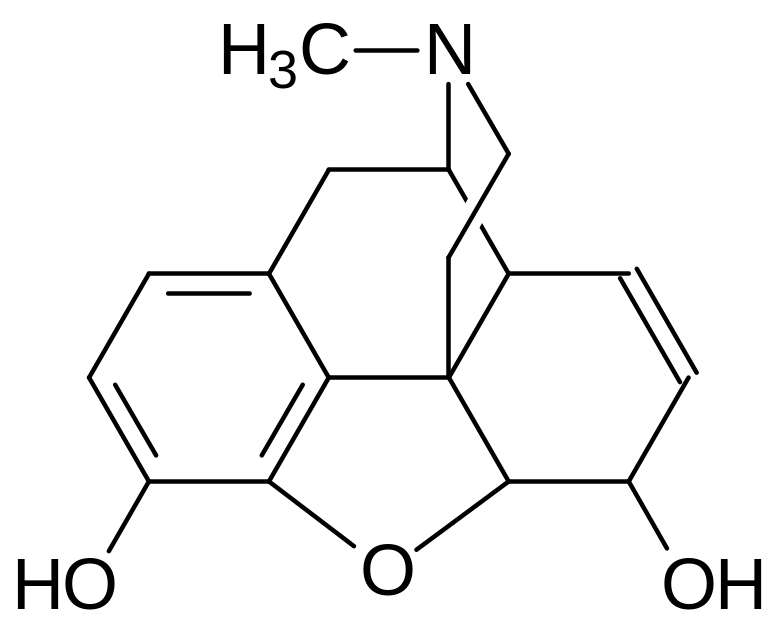
или ближе к реальной структуре:
В то же время видно, что у этих двух молекул есть общий структур-ный элемент – гидроксифенильная группа, отделенная от аминогруппы двумя атомами углерода (это характерно для подавляющего большинства нейромедиаторов). С помощью меченного морфина были выделены глико-протеины, с которыми он связывается в прочный комплекс, а изучение их естественных лигандов и привело к открытию опиоидных пептидов. При связывании с ними происходит структурная перестройка этих рецепторов, приводящая к блокировке калиевых каналов (-рецептор), кальциевых каналов (-рецептор) и аденилатциклазы (-рецептор). То есть этими веществами может быть одновременно заблокирована проводимость сиг-нала на уровне нервного волокна, на уровне высвобождения нейромеди-атора возбуждения и на метаболическом уровне.
Опиаты, как лекарственные средства, отмечены целым рядом недо-статков. Они не могут быть использованы для снятия хронических болей, так как их поступление в организме в течение продолжительного времени приводит к болезненному пристрастию и к привыканию, когда для дости-жения того же самого эффекта требует постоянное увеличение дозировки. В основе этого явления лежит ответ организма на блокировку активности аденилатциклазы (-рецептор). В присутствии блокаторов этот участвую-щий в энергетике клеток фермент перестает генерировать циклический аденозинмонофосфат и клетки организма отвечают на это выработкой новых молекул катализатора. Увеличенное содержание аденилатциклазы нуждается в повышенной дозе его блокатора, и так идет постепенное нара-щивание содержания фермента в клетках. При отказе от приема наркоти-ческого вещества происходит высвобождение активной аденилатциклазы в количествах, которые значительно превышают ее нормальное содержание. В клетках образуется слишком много цАМФ и АТФ (оба эти вещества алгогены), а избыток источника химической энергии приводит к непроиз-вольным сокращениям мышц, повышенной двигательной активности, а в серьезных случаях и к сильнейшим судорогам, сопровождающимся тяже-лейшими болями во всем теле (это и есть синдром абстиненции или так называемая «ломка» наркоманов). Кроме того, алкалоиды мака вызывают рвоту и запоры, а в больших дозах они могут привести к смерти из-за бло-кировки дыхательного центра, реагирующего на присутствие диоксида углерода в легких.
После обнаружения естественных лигандов опиатных рецепторов казалось, что проблему избирательных анальгетиков, действующих на уровне центральной нервной системы можно будет легко решить. Стоит только найти их пептидные аналоги, которые устойчивы к действию гид-ролаз, и будут получены совершенные обезболивающие средства. Важно отметить, что такие вещества образуются в естественных процессах. Так, например, при ферментативном гидролизе содержащегося в коровьем молоке казеина образуются сравнительно устойчивые к действию пептидаз фрагменты этого белка со свойствами опиатных анальгетиков: ‑казомор-фин-5 (Тир-Про-Фен-Про-Гли) и -казоморфин-7 (Тир-Про-Фен-Про-Гли-Про-Иле), материнское молоко также содержит казеин, из которого образуется активный пептид Тир-Про-Фен-Вал-Глу-Про-Иле. Их вса-сывание в таком виде объясняет мягкий успокаивающий и снотворный эффект молока, который особенно хорошо проявляется у детей, желудочно-кишечный тракт которых более проницаем для олигопептидов. Кроме того, гептапептид материнского молока регулирует и высшую нервную деятельность ребенка. Его влияние на ранней стадии развития детского организма играет важнейшую роль в формировании характера и умственных способностей ребенка. Входящий в состав казоморфинов С‑концевой фрагмент Про-Гли-Про хорошо защищает небольшие пептиды от действия пептидаз. Это было использовано, например, при разработке нового лекарственного средства «Семакс». Было известно, что аминокис-лотная последовательность 4-7 в гипофизарном адренокортикотропном гормоне (АКТГ, 39 аминокислот) оказывает очень хороший стимули-рующий эффект на высшую нервную деятельность. Этот тетрапептид с биохимической формулой Мет-Глу-Гис-Фен улучшает восприятие, обучаемость и другие характеристики высшей нервной деятельности, но его действие слишком непродолжительно из-за гидролиза протеазами. Аналогичными свойствами обладает и более длинный фрагмент АКТГ гептапептид 4-10. Исходя из этого можно было предположить, что допол-нение тетрапептида с С-конца фрагментом Про-Гли-Про сохранит его био-логическую активность и сделает его более устойчивым к ферментатив-ному гидролизу. Детальное изучение терапевтического эффекта этого гептапептида подтвердило эти предположения и показало, что он может приниматься не только здоровыми людьми для улучшения работы головного мозга. У больных с нарушениями функций головного мозга, например, после инсульта, семакс значительно ускоряет выздоровление и улучшает течение болезни. Отмечено также положительный эффект семакса на течение некоторых глазных болезней.
Подобный способ модификации молекулы можно было использовать и для стабилизации структуры энкефалина, но в этом случае был исполь-зован более распространенный в химии пептидов подход, основанный на замене L-аминокислот с небольшими радикалами их D-изомерами, фраг-мента фенилаланина его тиенильным аналогом и введением аминоизо-масляной кислоты вместо аланина или других аминокислот. Такое незна-чительное изменение пространственного расположения структурных элементов может оказаться незначимым для соответствующего рецептора, но протеазы, гидролизующие только пептидные связи, построенные из белковых L-аминокислот, не гидролизуют пептидные связи с небелковыми аминокислотами. В случае энкефалина можно было использовать замену глициновых фрагментов на D-аланиновые. Были, конечно, проведены и другие модификации структуры энкефалина, которые можно представить в следующем виде:
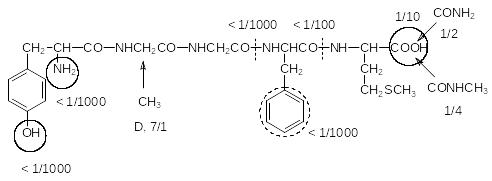
На схеме представлены изменения структуры и их влияние на актив-ность в сравнении с исходной нативной структурой. Чаще всего биологи-ческая активность измененного пептида снижалась, но в других вариантах были получены соединения, которые сохраняли присущую энкефалину активность и были значительно более устойчивы к биотрансформации. При этом оказалось, что использование таких стабильные пептиды в ка-честве лекарственных средств не дает никаких преимуществ, поскольку им присущи все недостатки морфина. Это означает, что морфин является настоящим пептидомиметиком, то есть веществом, которое повторяет все свойства соответствующего пептида.
Успех в области получения обезболивающих средств был достигнут при ином подходе к вмешательству в функционирование энкефалина. Было получено вещество, которое блокирует предназначенный для разло-жения избытка и выполнившего медиаторную функцию энкефалина фермент энкефалиназу. По аналогии с другими блокаторами пептидаз, в частности, с используемыми для лечения гипертонии блокаторами ангио-тензинконвертирующего фермента (каптоприл), был получен тиорфан:
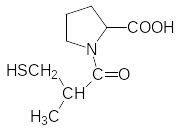
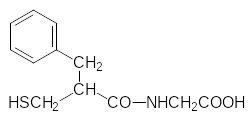
Каптоприл Тиорфан
Такие подобные пептидам соединения занимают в каталитическом центре пептидазы место естественного субстрата, прочно связываются за счет сульфгидрильной группы с участвующим в работе каталитического центра ионом цинка и блокируют фермент.

На схеме представлен возможный вариант соответствия строения ак-тивного центра энкефалиназы структуре энкефалина с участками связыва-ния карбонильной группы второй молекулы глицина с ионом цинка, с гидролизуемым участком в пептидной цепочке, с центром узнавания последней пептидной связи и катионоидным участком для связывания карбоксилатной группы. В молекуле тиорфана место пептидной связи между второй молекулой глицина и остатком фенилаланина -СO-NH- занимает группа HS-CH2-, образующая прочную связь с ином цинка.
Тиорфан является эффективным обезболивающим средством за счет повышения концентрации энкефалина только там, где он образуется для регуляции интенсивности болевого сигнала. Поэтому он не вызывает болезненного пристрастия и его действие не сопровождается состоянием эйфории, запорами, блокировкой аденилатциклазы и другими побочными эффектами, возникающими при приеме морфина или его структурных аналогов.
Еще один способ обезболивания основан на использовании структур-ных аналогов нейролипинов, которые также вовлечены в регуляцию интенсивности болевых сигналов. Одно из возможных обезболивающих средств этой группы представлено ванилиламидом олеиновой кислоты:
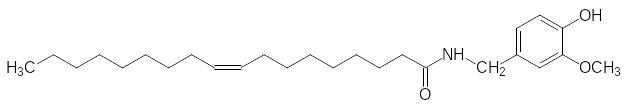
Сообщения об опытах по использованию этого вещества в качестве внутривенного средства для обезболивания появлялись в литературе, но соответствующего этому активному веществу лекарственного средства пока нет.
Разработки в этом направлении связаны с тем, что
