
- •Предисловие
- •Часть 1. Молекулярные основы наследственности
- •Введение в молекулярную биологию.
- •1.2. Макромолекулы как обьекты изучения молекулярной биологии
- •1.2.1. Белки.
- •1.2.2. Строение, функции и свойства днк.
- •Молекулярная организация генов.
- •Рнк и её роль в сохранении и реализации наследственной информации.
- •Лекарственные средства, влияющие на синтез нуклеиновых кислот и белков.
- •1.3. Экспрессия генов и её регуляция
- •1.4. Организация геномов неклеточных и клеточных организмов
- •Геном бактерий
- •Организация генома эукариот.
- •Часть 2. Молекулярные основы наследственных заболеваний
- •2.1. Молекулярные механизмы генных, хромосомных и геномных мутаций
- •2.2. Регуляция клеточного цикла. Апоптоз. Онкогенетика.
- •Часть 3. Современные вопросы генных технологий
- •3.1 Исследование нуклеиновых кислот. Методы днк-диагностики
- •3.2 Методы генной инженерии
- •3.3 Клонирование организмов и клеток.
- •Приложения контрольно-обучающие вопросы
- •Ответы на контрольно – обучающие вопросы
- •Терминологический словарь
- •Литература
- •Содержание
- •Часть 1. Молекулярные основы наследственности 4
- •Часть 2. Молекулярные основы наследственных заболеваний 120
- •Часть 3. Современные вопросы генных технологий 167
1.3. Экспрессия генов и её регуляция
Механизмы генной экспрессии. Понятие об экспрессии генов. Современное состояние центральной догмы молекулярной генетики. Свойства генетического кода. Этапы биосинтеза белка. Ферментативные механизмы и этапы транскрипции. Процессинг первичных транскриптов. Альтернативный процессинг, РНК-редактирование. Активация аминокислот. Молекулярная организация рибосом. Инициация, элонгация и терминация синтеза полипептидной цепочки. Посттрансляционная модификация белков.
Регуляция экспрессии генов. Регуляция экспрессии генов у прокариотов. Катаболические и анаболические опероны бактерий. Контроль экспрессии генов у эукариотов. Регуляция на уровне транскрипционных процессов. Белки – факторы транскрипции. Понятие об эпигенетической регуляции экспрессии генов. Метилирование ДНК, геномный импринтинг. Гормональная регуляция экспрессии генов. Контроль на уровне трансляции и посттрансляционных процессов.
Механизмы генной экспрессии. Хотя не все клетки млекопитающего выглядят и ведут себя одинаково, они имеют идентичный генетический материал. Сегодня мы знаем, что около 200 различных клеточных фенотипов в организме человека отличаются тем, какие гены в них экспрессируются, а также сигналами, определяющими время экспрессии определенного гена или набора генов.
Генная экспрессия – это совокупность молекулярных механизмов реализации наследственной информации, благодаря которым ген проявляет свой потенциал в конкретном фенотипическом признаке организма.
Процесс экспрессии гена состоит из нескольких этапов:
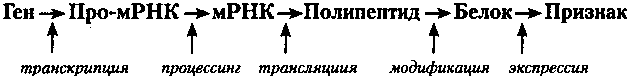
Каждый этап, в свою очередь, имеет начало (инициация), продолжение (элонгация) и конец (терминация), где также осуществляется контроль генной экспрессии *
а) на основе гена ДНК синтезируется про-мРНК. Первый этап экспрессии называется «транскрипцией»; б) крупная молекула про-мРНК подвергается «процессингу», в результате этого значительно уменьшается в размерах. Образуется «зрелая» мРНК, считывание информации с которой упрощается. Биологический смысл процессинга - облегчение доступа к генетической информации; в) мРНК при участии тРНК «выбирает» необходимые аминокислоты, которые связываются на рибосоме в строго определенную последовательность полипептида. Процесс переноса информации с мРНК на полипептид называется «трансляцией»; г) синтезированный полипептид подвергается «модификации» и превращается в активный белок; д) функционируя, белок делает свой вклад в морфологический или функциональный признак (фенотип) клетки или организма. Это процесс называется «экспрессией».
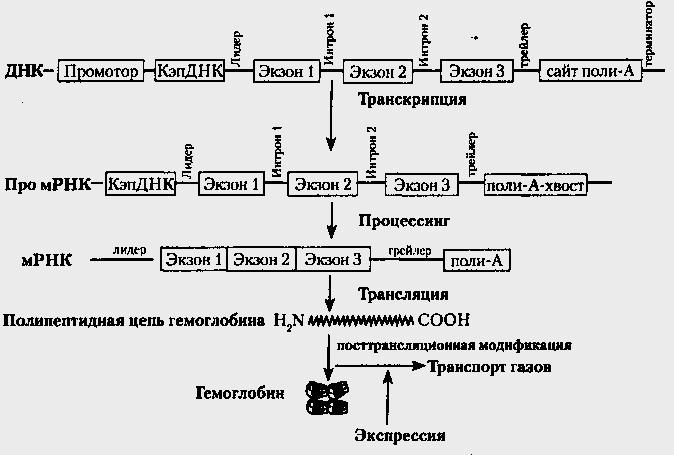
Рис.18. Схема этапов экспрессии гена ß - цenu гемоглобина
Схема механизма экспрессии представлена на рис.18 на примере экспрессии гена β-цепи гемоглобина. В процессе транскрипции участвует не только смысловая часть гена, но и другие регуляторные и структурные части. Образуемая про-мРНК содержит все элементы, характерные для гена ДНК. Процессинг существенно модифицирует про-мРНК, которая превращается в мРНК и содержит намного меньше структурно-функциональных элементов. На основе мРНК трансляция создает молекулы совершенно другой природы — полипептиды, ничего не имеющие общего с нуклеиновыми кислотами и обладающими совершенно другими свойствами и организацией. Модификация полипептидов приводит к еще одному природному явлению — появлению сложной пространственной организации молекулы белка. Происходит переход линейной информации ДНК и РНК в пространственную организацию протеина, которая, в свою очередь, является основой специфического пространственного взаимодействия молекул в живом организме, что и лежит в основе жизни и всех жизненных явлений. В данном случае процесс модификации обеспечивает пространственную организацию – объединение четырех субъединиц гемоглобина в единый комплекс. В результате всех этапов экспрессии проявляется признак — способность к транспорту газов (О2 и СО2).
Современное состояние центральной догмы молекулярной биологии. Хромосомные ДНК содержат полную информацию обо всех белках, синтезируемых в клетке. Эта информация закодирована в ДНК в виде особой последовательности азотистых оснований, называемой генетическим кодом. Специфическая последовательность нуклеотидов гена транскрибируется в мРНК и затем транслируется на рибосомах, обеспечивая строгий порядок аминокислот в полипептидной цепи. Представление о том, что информация хранится в ДНК и реализуется путем ее передачи от ДНК к мРНК, а затем к полипептиду, а при размножении путем репликации из одного поколения в другое, считается основной догмой (основным законом) молекулярной биологии. Она была предложена Ф. Криком в 1958 г. Схематически ее можно представить следующим образом:
Репликация транскрипция трансляция ДНК ► ДНК ► РНК ► Белок
В 1970 г. Темин сообщил о том, что РНК, функционирующая как генетический материал в некоторых вирусах, может синтезировать комплементарную копию ДНК для внедрения в геном клетки-хозяина. Значит, у вирусов информация поступает не обязательно от ДНК к РНК, но может также и от РНК к ДНК (обратная транскрипция). Осуществляется она с помощью ферментов — ревертаз (лат. rever-sio — возврат). Это свойство нуклеиновых кислот используется в генной инженерии.
Передача информации «запрещена» от белков обратно к нуклеиновым кислотам. Это означает, что модификации белков - генных продуктов не наследуются. Центральная догма отвергает ламаркизм. Все типы передачи генетической информации осуществляются на основе комплементарных межмолекулярных взаимодействий: А=Т, Ц=Г.
Однако история с клонированием в 1996 году знаменитой ныне овечки Долли в шотландской фирме PPL Therapeutics (коммерческого отделения Розлин Института в Эдинбурге) позволяет взглянуть на центральную догму совсем по-иному. Коллектив ученых, возглавляемый Иэном Уилмутом, продемонстрировал, что им удалось, используя соматические клетки взрослого животного, получить клональное животное. Это значит, что биологические часы могут быть повёрнуты вспять, и развитие организма может начаться из генетического материала взрослой дифференцированной клетки, что полностью противоречит ранее общепринятой биологической догме.
Свойства генетического кода. Уникальность разнообразных клеток обусловлена уникальностью их белков. Клетки способны синтезировать индивидуальные белки за счет использования информации, записанной в молекуле ДНК. Эта информация существует в виде особой последовательности азотистых оснований нуклеотидов в нитях ДНК и называется генетическим кодом. Порядок азотистых оснований в мРНК, которая построена по матрице ДНК, определяет порядок связывания аминокислот в синтезируемом полипептиде (табл.3). Каждая аминокислота кодируется последовательностью трех азотистых оснований (триплетом, или кодоном). Таким образом, генетический код представляет собой определенную строгую последовательность триплетов в молекуле ДНК, контролирующую порядок расположения аминокислот в молекулах белков.
В ДНК имеются четыре основания, а в белках-20 аминокислотных остатков; синглетный код мог бы кодировать только четыре аминокислотных остатка, дублетный-4-4 = 16 аминокислот, а триплетный образует 4 - 4 • 4 = 64 разных кодона.
Код не перекрывается, т.е. в последовательности оснований АВСDЕFGНI первые три основания, АВС, кодируют аминокислоту 1, DЕF- аминокислоту 2 и т.д. Если бы код был перекрывающимся, то последовательность АВС кодировала бы аминокислоту 1, СDЕ-аминокислоту 2 и т.д. Неперекрывающийся характер кода относится только к случаю, когда рамка считывания не меняется. В коде отсутствуют запятые, т.е. нет знаков, отделяющих один кодон от другого.
Направление чтения закодированной записи - от 5'-кoнцa к З'-концу мРНК, являющейся транскриптом « + »-цeпи ДНК, считанным с нее в направлении 5' -» 3'. Первый с 5'- кoнцa кодон отвечает N-концевой аминокислоте полипептидной цепи. Следовательно, белки синтезируются от N-конца к С-концу.
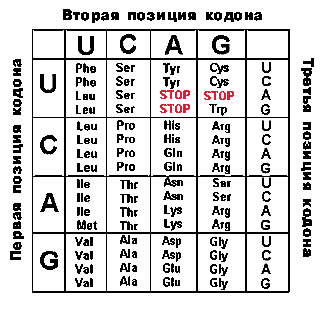
Табл.3. Генетический код
Таблица кода указывает, какая аминокислота кодируется тем или иным кодоном. В таблице 5 первый (с 5'-кoнцa) нуклеотид помещен в левом столбце, второй - в верхней строке, а третий (на 3'-кoнцe)-в правом столбце. Из представленных в таблице 64 кодонов 61 кодон детерминирует ту или иную аминокислоту (например, СUА отвечает лейцину Lеu), а три остальных кодона являются сигналами терминации. Эти три кодона называются нонсенс-кодонами, поскольку они не определяют никакой аминокислоты. Помимо этого, когда кодоны АUG для Меt и иногда GUG для Vаl находятся в начале последовательности и соответствующие аминокислоты должны быть помещены в начале белковой цепи, эти аминокислоты обычно присутствуют в виде N-формильных производных. Когда же эти кодоны находятся в любом другом месте последовательности, то в пептидную цепь включаются нормальные Меt и Vаl.
Код вырожден, т.е. большинство аминокислот кодируется более чем одним кодоном. Например, Рhе кодируется двумя кодонами -UUU и UUС. Кодоны, которые определяют одну и ту же аминокислоту, называются кодонами- синонимами. Вырожденность кода, как правило, выражается в том, что у кодонов, определяющих одну и ту же аминокислоту, первые два основания фиксированы, а третье положение может занимать одно из двух, трех или четырех разных оснований. В частности, кодоны с одним из двух пиримидинов (С или U) в третьем положении всегда являются синонимами, в то время как кодоны с одним из двух пуринов (А и G) в третьем положении бывают синонимами лишь иногда. Различия по всем трем положениям наблюдаются лишь в некоторых случаях (например, UСG и АGU оба кодируют Sеr).
Каждая тРНК может узнавать до трех кодонов. Химические свойства разных аминокислот находят отражение в структуре кода. Все кодоны с U во втором положении кодируют аминокислоты с гидрофобной боковой цепью (Рhе, Lеu, Не, Меt и Vаl). Если исключить терминирующие кодоны, то наличие А во втором положении определяет полярную или заряженную боковую цепь (Туг, Нis, Glп, Аsп, Lуs, Аsр и Glu). Рамка считывания задает положение первого основания кодона мРНК (или гена). Поскольку код триплетен, число возможных рамок считывания равно трем. Обычно функциональный белок синтезируется только при одной рамке считывания, но некоторые вирусы используют две или даже три рамки считывания, при этом синтезируются разные белки.
Мутация- это изменение в последовательности оснований генетического материала данного организма. Знание генетического кода позволяет объяснить эффект некоторых мутаций.
Молчащая мутация- это такое изменение в нуклеотидной последовательности, которое приводит к образованию синонимичного кодона, и в результате аминокислотная последовательность кодируемого белка не изменяется. Структура кода такова, что молчащие мутации часто бывают, обусловлены изменениями оснований лишь в третьем положении кодона.
Замена (миссенс-мутация) ведет к замещению одной аминокислоты другой в результате такого изменения последовательности оснований, которое не приводит к образованию синонимичного кодона. Так, заболевание серповидно-клеточная анемия возникает в результате замены Glu на Vаl в шестом положении ß-цепи гемоглобина человека. Это обусловлено изменением кодона GАА на GUА, т.е. заменой А на U во втором положении.
Мутация со сдвигом рамки обусловлена вставкой или удалением (делецией) одного или большего числа оснований в последовательности, так что при этом изменяется рамка считывания. Это приводит к изменению аминокислотной последовательности белка от точки мутации до С-конца молекулы.
Универсальность генетического кода означает, что все живые организмы-эукариоты, прокариоты и вирусы - используют один и тот же код. Хотя, вообще говоря, это положение справедливо, проведенные сравнительно недавно (1981 г.) определения нуклеотидной последовательности митохондриальных ДНК человека и дрожжей выявили некоторые необычные факты. Например, триплет UGА не является терминирующим кодоном, а кодирует Тгр, а триплеты АGА и АGС не кодируют Аrg, а являются терминаторами.
Генетический код был расшифрован в начале 60-х годов Ниренбергом, Кораной и их сотрудниками. Ниренберг получил клеточный экстракт Е. соli, содержавший все компоненты, необходимые для синтеза белка, включая рибосомы, все тРНК и аминоацил-тРНК-синтетазы. В систему добавляли полинуклеотид poly(U) (т.е. UUUUU UU...), функционировавший как искусственная мРНК. Оказалось, что poly(U) детерминирует синтез poly(Phe) (т.е. Рhе Рhе Рhе ...); следовательно, триплет UUU кодирует Рhе. Аналогичные опыты показали, что триплет ССС кодирует Рrо, а триплет ААА-Lуs. Следующий шаг заключался в использовании полирибонуклеотидов, содержавших два, три или четыре разных основания, расположенных в случайном порядке. В результате этих исследований удалось определить состав других кодонов, но не последовательность оснований в них; так, было показано, что кодон, содержащий 2U и 1G, детерминирует Суs, но порядок оснований оставался неизвестным. Корана использовал полирибонуклеотиды не со случайной, а с заранее заданной последовательностью и определил структуру нескольких кодонов. Эти исследования получили дальнейшее развитие с помощью другого подхода, разработанного Ниренбергом. Он обнаружил, что тринуклеотиды вызывают связывание специфических аминоацил-тРНК с рибосомой. Например, в присутствии UGU с рибосомой связывается только аминоацил-тРНК для Суs. Следовательно, UGU кодирует Суs. Три кодона, UАА, UАG и UGА, не кодируют никаких аминокислот и определяют терминацию синтеза.
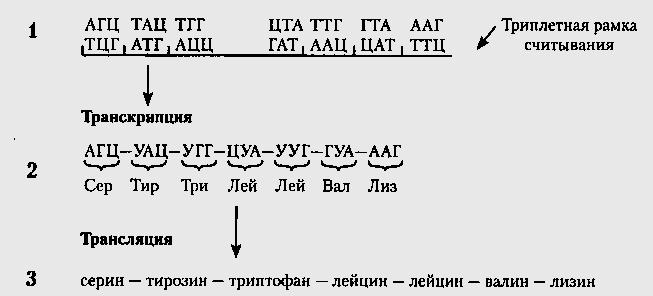
Рис.19. Схема организации генетического кода и процесса реализации наследственной информации: 1 — ДНК, 2 — мРНК, 3 — полипептид.
Строгая последовательность нуклеотидов в молекуле ДНК кодирует определенную последовательность нуклеотидов в мРНК. Каждый триплет нуклеотидов кодирует одну конкретную аминокислоту. В результате трансляции, на основе генетического кода, на рибосомах синтезируется необходимый белок (рис.19).
Таким образом, генетический код ДНК имеет следующие фундаментальные характеристики:
Триплетность. Три соседствующих азотистых основания, называемые кодоном, кодируют одну аминокислоту.
Специфичность. Каждый отдельный триплет кодирует только одну определенную аминокислоту.
Неперекрываемость. Азотистое основание определенного триплета никогда не входит в состав другого кодона.
Отсутствие знаков препинания. Генетический код не имеет «пунктуационных отметок» между кодирующими триплетами в структурных генах.
Универсальность. Кодон в ДНК или мРНК определяет одну и ту же аминокислоту в белковых системах всех организмов от вируса до человека.
Избыточность. Одна аминокислота часто имеет более чем один кодовый триплет.
Коллинеарность. ДНК — линейная полинуклеотидная цепь, а белок — линейная полипептидная. Последовательность аминокислот в белке соответствует последовательности триплетов в его гене (у прокариот).
Однонаправленность — процесс считывания информации генетического кода с матричной цепи молекулы ДНК идет только в одном направлении — от 5 '- конца к 3 '-концу.
Этапы биосинтеза белка. Транскрипция ДНК и процессинг РНК. Транскрипция - процесс переноса генетической информации от ДНК к РНК. Все виды РНК- мРНК, рРНК и тРНК - синтезируются в соответствии с последовательностью оснований в ДНК, служащей матрицей. Транскрибируется только одна (смысловая), так называемая « + » - цепь ДНК. Процесс транскрипции у прокариот и эукариот существенно различается.
Транскрипция у прокариот. ДНК-зависимая РНК-полимераза - это фермент, катализирующий синтез РНК. Он состоит из 4 субъединиц. Их комплекс называется холоферментом. Для инициации транскрипции необходимы холофермент, нуклеозидтрифосфат (всегда АТР или GTP) и наличие специального участка в ДНК, называемого промотором. Когда полимераза связывается с промотором, происходит локальное расплетание двойной спирали ДНК и образуется открытый промоторный комплекс.
Промотор- это участок молекулы ДНК, имеющий размер около 40 пар оснований и расположенный непосредственно перед участком инициации транскрипции. Синтез РНК всегда начинается с оснований А или G в « + »- цепи ДНК. Участок связывания холофермента расположен выше сайта инициации (т. е. в направлении 3' -> 5' в «+ »-цепи) на расстоянии примерно 10 оснований. Если сравнить последовательности оснований « + »-цепи ДНК у разных промоторов, то мы обнаружим, что они весьма близки, хотя и не идентичны. Эта так называемая последовательность Прибнова имеет вид ТАТРuАТРu, где Рu означает пурин (А или G). Таким образом, холофермент связывается со специфической последовательностью или группой последовательностей. Обычно на расстоянии около 40 оснований выше участка инициации находится второе место связывания РНК-полимеразы.
Элонгация цепи РНК- это та стадия транскрипции, которая наступает после присоединения примерно восьми рибонуклеотидов. В этот момент РНК-полимераза претерпевает некоторые структурные изменения, при котором от комплекса отделяется одна субъединица, а остающиеся три (кор-фермент) катализируют дальнейшее удлинение цепи РНК. При этом к цепи присоединяются те рибонуклеотидтрифосфаты, которые обеспечивают правильное спаривание с « —»- цeпью ДНК. Движущийся вдоль ДНК кор-фермент действует подобно застежке-молнии, «раскрывая» двойную спираль, которая замыкается позади фермента по мере того, как соответствующие основания РНК спариваются с основаниями ДНК в « —»-цeпи. «Раскрытая» ферментом область простирается только на несколько пар оснований. Терминация (прекращение роста) цепи РНК происходит на специфических участках ДНК, называемых терминаторами. Начало этих участков обычно обогащено GС-парами, а остальная последовательность -АТ-парами. GС-богатый участок часто представляет собой палиндром. Это означает, что при движении вдоль « + »-цeпи в одном направлении, а вдоль « — »-цeпи- в противоположном, читается одна и та же последовательность оснований. В остановке синтеза РНК именно на терминаторе важную роль играет р-белок.
Посттранскрипционный процессинг - это процесс созревания, при котором первичный РНК-транскрипт модифицируется и превращается в зрелую РНК. Характер и степень модификации РНК зависят от типа РНК.
Молекулы мРНК у прокариот не подвергаются процессингу. У некоторых бактерий транскрипция и трансляция сопряжены, т.е. происходят одновременно. 5'-кoнeц мРНК может транслироваться на рибосоме и затем подвергаться деградации еще до завершения синтеза ее З'-конца. Молекулы тРНК вначале синтезируются в виде про-тРНК, которая примерно на 20% длиннее, чем соответствующая тРНК. Лишние последовательности, расположенные у 5'- и З'-концов, удаляются с помощью таких ферментов, как рибонуклеазы Q и Р. Иногда молекула про-тРНК состоит из двух или более молекул тРНК, соединенных между собой. Их разделение также осуществляется с помощью рибонуклеаз. Если З'-конец тРНК не несет концевой последовательности ССА, то эти основания присоединяются при постсинтетической модификации. Все тРНК содержат минорные основания, которые являются химически модифицированными формами четырех главных оснований (А, С, G и U). Эта модификация происходит после завершения транскрипции.
Гены рРНК прокариот расположены в транскрипционных блоках. Три гена рРНК Е. соli (16S, 23S и 5S) располагаются вместе с генами нескольких тРНК в одном таком блоке и транскрибируются в виде одной молекулы РНК. Эти молекулы рРНК и тРНК отделены друг от друга спейсерной РНК. Расщепление первичного транскрипта на отдельные составляющие катализирует рибонуклеаза Q; поскольку этот фермент специфичен к двухцепочечной РНК, предполагают, что в области спейсеров образуются двухцепочечные шпильки, которые фермент узнает и вырезает.
Транскрипция у эукариот. У эукариот для транскрипции используются три ДНК-зависимых РНК-полимеразы. Полимераза I локализована в ядрышке, где она катализирует синтез рРНК в виде большого первичного транскрипта, содержащего молекулы рРНК 18S, 5,8S и 28S. Полимераза II находится в нуклеоплазме и, вероятно, участвует в синтезе первичного транскрипта мРНК. Полимераза III также локализована в нуклеоплазме и участвует в синтезе тРНК и 5S-pPHK.
Синтез РНК (рис. 20) включает стадии инициации, элонгации и терминации, но в этих процессах часто принимают участие другие ферменты и последовательности оснований, чем у прокариот. Например, промоторные последовательности у эукариот отличаются от таковых у прокариот. Однако первыми основаниями, включаемыми в РНК при инициации, являются, как и у прокариот, А или G.
Молекулы мРНК обычно образуются из больших по размеру молекул-предшественников, называемых гетерогенной ядерной РНК (гяРНК). Для образования зрелой мРНК эти молекулы подвергаются модификации по 5'- и З'-концам и сплайсингу. После такой модификации транскрипты переносятся из ядра в цитоплазму.
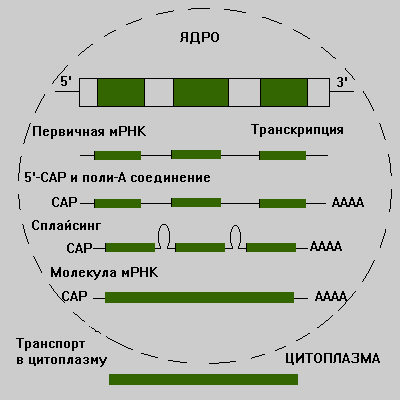
Рис.20. Схема синтеза мРНК
Сплайсинг мPHK-этo удаление последовательностей РНК, соответствующих интронам ДНК, и соединение участков, которые транскрибированы с кодирующих последовательностей (экзонов). Место сплайсинга должно быть определено с высокой точностью, поскольку ошибка даже в одно основание приведет к синтезу белка с неправильной аминокислотной последовательностью. Такая специфичность сплайсинга обеспечивается строго определенной последовательностью оснований в интроне, отвечающей обычно основаниям GU или GА в начале соответствующей РНК и основаниям АG-в конце.
Модификация 5'-кoнцa мРНК приводит к образованию особой последовательности, называемой кэп-структурой. При модификации З'-конца к нему присоединяется последовательность poly(A) длиной 150-200 нуклеотидов.
Благодаря альтернативному сплайсингу число синтезируемых белковых продуктов, очевидно, в 1,5-2 раза больше, чем число генов. Явление альтернативного сплайсинга заключается в следующем. Из одного и того же первичного РНК-транскрипта в процессинге РНК в разных тканях образуется не один, а несколько разных по длине мРНК-транскриптов. Соответственно синтезированные полипептиды также будут различными. Таким образом, одна и та же ДНК-последовательность может кодировать не один, а несколько разных полипептидов.
Роль сплайсинга:
Создание новых генов в ходе эволюции.
Более полное экономичное использование записанной в геноме информации.
Регуляция активности генов.
Мутации, ведущие к нарушению сплайсинга на границе экзон-интрон (внутри интрона они бесследны) играют существенную роль в возникновении ряда наследственных болезней человека. Очевидно, что раз они так сильно меняют функциональную организацию гена, то им может принадлежать существенная роль и в процессах создания новых генов в ходе эволюции.
Процессинг тРНК у эукариот протекает примерно по такому же механизму, как и у прокариот. Функционально активные молекулы образуются из более длинного предшественника, который подвергается расщеплению и модификации с включением минорных оснований.
Процессинг рРНК также аналогичен соответствующему процессу у прокариот. Первичный транскрипт содержит участки, отвечающие 18S-, 5,8S- 28S-pPHK, разделенные спейсерами. Как и у прокариот, эти три рРНК образуются при расщеплении спейсерных последовательностей.
Молекулярная организация рибосом. Субъединицы рибосом образуются в ядрышке, а затем через ядерные поры по отдельности поступают в цитоплазму. Их количество в цитоплазме зависит от синтетической активности клетки и может составлять от сотни до тысяч на одну клетку. Их функцией является синтез белков. Наибольшее количество рибосом обнаружено в клетках, интенсивно синтезирующих протеины. Встречаются также в митохондриальном матриксе и хлоропластах.
Рибосомы любых организмов — от бактерий до млекопитающих, характеризуются сходством структуры и состава, хотя клетки прокариот имеют рибосомы меньших размеров и в меньшем количестве. Каждая состоит из нескольких разновидностей молекул рРНК и десятков разновидностей белков примерно в одинаковой пропорции. Маленькая и большая субъединицы находятся в цитоплазме по отдельности, пока не вовлечены в белковый синтез. Они объединяются друг с другом молекулой мРНК при необходимости синтеза и вновь разъединяются с прекращением процесса (рис.21).
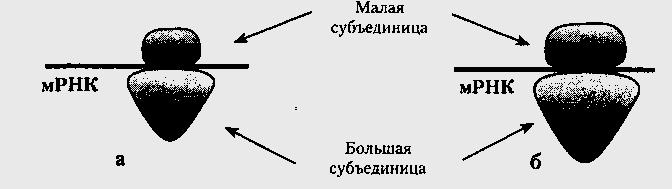
Рис.21. Субъединицы прокариотических (а) и эукариотических (б) рибосом
Различные размеры и отличающийся состав белков и рРНК обусловливает разную чувствительность к некоторым антибиотикам. Например, тетрациклин действует только на рибосомы бактерии и подавляет синтез белков в этих клетках, не влияя на эукариотические клетки хозяина.
Молекулы мРНК, синтезированные в ядре, поступают в цитоплазму к рибосомам. Из цитозоля молекулами тРНК к рибосомам доставляются аминокислоты, где с участием ферментов и АТФ синтезируются белки. Если с одной молекулой мРНК соединяются несколько рибосом, то образуются полисомы, которые содержат от 5 до 70 рибосом.
Механизм трансляции у прокариот (Е. соli). Стартовым сигналом к началу синтеза белка служит расположенный на мРНК кодон АUG, кодирующий метионин (Меt) [иногда это кодон GUС для валина (Vаl)]. В растущей полипептидной цепи первым аминокислотным остатком всегда будет либо Меt, либо Vаl. Тогда возникает законный вопрос: каким образом клетка отличает стартовый сигнал от кодонов АUG или GUС, расположенных в середине молекулы мРНК? Эта проблема решается с помощью модифицированной формы Меt (или Vаl) и специальной инициирующей тРНК. Формилметионин (fМеt) и является той модифицированной формой Меt, с которой начинается синтез белка. Он присоединяется к молекулам тРНК определенного типа (тPHKf), отличным от тPHKMet, посредством которых Меt включается в срединную часть полипептидной цепи. И тPHKf, и тPHKMet узнают кодон АUG, но лишь тPHKf способна присоединяться к стартовому кодону АUG. Инициация синтеза белка начинается с момента образования инициирующего комплекса на 30S-субчастице, состоящего из мРНК, ЗОS-субчастицы рибосомы и молекулы aминoaцил-тPHKf с присоединенным fМеt, которая связывается с участком Р. Следующим шагом является присоединение 50S-cyбчacтицы, в результате чего образуется 70S-инициирующий комплекс. Источником энергии для инициации синтеза белка служит реакция гидролиза GТР до GDР и Рj. На этом этапе необходимы еще несколько белков, называемых факторами инициации (IF1, IF2 и IFЗ).
Элонгация - это последовательное включение аминокислотных остатков в состав растущей полипептидной цепи. Каждый акт элонгации состоит из трех этапов: 1) узнавание кодона, 2) образование пептидной связи и 3) транслокация.
Узнавание кодона заключается в связывании антикодона очередной молекулы аминоацил - тРНК с кодоном свободного участка А на рибосоме. Чтобы прикрепиться к рибосоме, тРНК с присоединенной к ней аминокислотой должна сначала образовать комплекс с белком, называемым фактором элонгации ЕF-Тu, или EF1, который предварительно должен быть активирован с помощью GТР. После того как произойдет связывание всего комплекса тРНК-ЕFl -GТР с участком А рибосомы, осуществляется гидролиз GТР до GDР и Рj, удовлетворяющий энергетические потребности на этом этапе элонгации. Фактор EF1 • GDР, неспособный более связываться с тРНК, покидает рибосому, на которой остается аминоацил-тРНК. Регенерацию активированного фактора EF1 катализирует второй фактор элонгации, ЕF-Тs, или EF2, который замещает GDР в неактивированном комплексе, в результате чего образуется комплекс EF1 • EF2.
Образование пептидной связи происходит лишь тогда, когда оба участка, А и Р, заняты молекулами аминоацил-тРНК. Часть 50S-cyбчacтицы представляет собой фермент пептидилтрансферазу, катализирующий образование пептидной связи. В результате этой реакции растущая полипептидная цепь оказывается присоединенной к тРНК участка А, а тРНК участка Р высвобождается из комплекса с пептидом и несет на З'-конце группу —ОН.
Транслокация включает три акта, катализируемых еще одним фактором элонгации, EF-G(EFЗ), и энергетически сопряженных с гидролизом GТР. Сначала тРНК участка Р, не связанная с пептидом, покидает рибосому, затем молекула полипептидил-тРНК переходит с участка А на Р и, наконец, рибосома перемещается вдоль мРНК на три нуклеотидных остатка в сторону З'-конца. В результате этих трех актов освобождается участок А и экспонируется очередной кодон, что позволяет начаться следующему циклу элонгации.
Терминация, т.е. окончание синтеза, происходит по команде кодонов UАА, UGА или UАG. В природе не существует таких молекул тРНК, антикодоны которых соответствовали бы этим кодонам. Вместо продолжения синтеза цепи происходит терминация, катализируемая специальными белками, которые названы факторами терминации (RF1 и RF2) и которые узнают терминирующие кодоны, когда свободен участок А. Эти факторы изменяют специфичность фермента пептидилтрансферазы таким образом, что происходит гидролиз связи между концевым пептидом и тРНК, а освобожденная полипептидная цепь диффундирует от рибосомы. Вслед за этим происходит диссоциация комплекса мРНК- рибосома. Далее рибосома диссоциирует на 30S- и 50S-cyбчacтицы. После реассоциации этих субчастиц с другой молекулой мРНК весь цикл синтеза белка начинается сначала.
Трансляция у эукариот, осуществляющаяся в цитоплазме, включает такие же этапы, что и трансляция у прокариот. Основным отличием здесь является то, что первым остатком в растущей полипептидной цепи является Меt, а не fМеt. Тем не менее и в этом случае есть два типа молекул тРНК, узнающих кодон АUG: один- когда кодон инициирующий, а другой- когда он кодирует Меt, который должен быть присоединен в середине растущей полипептидной цепи. В роли факторов инициации и элонгации выступают различные белки. Еще одно существенное отличие состоит в том, что в цитоплазме эукариот рибосомы более крупные (80S).
У митохондрий и хлоропластов трансляция осуществляется в самих этих органеллах. Рибосомы, которые они содержат, представляют собой 70S-частицы и похожи на рибосомы бактерий. При инициации используется fМеt. Последовательность событий при трансляции у эукариот такова:
информосомы переносят мРНК в цитоплазму,
образуется комплекс старта трансляции: мРНК + малая субъединица рибосомы + стартовая тРНК,
присоединение большой субъединицы рибосомы и начало синтеза белка от 5’ к 3’,
в это же время происходит активация аминокислот путем их взаимодействия с АТФ,
присоединение активированных аминокислот к специфической тРНК,
собственно трансляция или полимеризация аминокислотных остатков на рибосоме в полипептидную цепь,
окончание синтеза (терминация) – рибосома дошла до кодона-терминатора и весь комплекс – мРНК, малая и большая части рибосомы, тРНК, белок – распадается и при необходимости он снова может собираться к новому синтезу белка.
Весь процесс трансляции идет с помощью дополнительных приблизительно 50 специальных белков: факторов инициации, элонгации, терминации. В общих чертах процесс трансляции одинаков у всех организмов.
Посттрансляционная модификация белков. Синтезированный из аминокислот полипептид — это практически прямолинейная молекула, не обладающая метаболической активностью. Далее белок самопроизвольно и с помощью шаперонов принимает II, III и другие структуры. Новая полипептидная цепь высвобождается в цитоплазму, эндоплазматическую сеть или комплекс Гольджи, где завершается построение белковой молекулы. В процессе «созревания» она может терять некоторые концевые аминокислоты при помощи фермента экзопептидазы, а затем образовывать вторичную и третичную структуры. Молекулы могут объединяться с другими полипептидами для образования четвертичной структуры. Синтезированные макромолекулы могут объединяться с углеводными или липидными молекулами, а также встраиваться в биомембраны или другие комплексы клетки. Процессы изменения первоначальной линейной структуры полипептида и формирования пространственной структуры белковых молекул называются пострансляционной модификацией. В результате этого белки приобретают специфические свойства и функциональную активность.
Роль шаперонов в формировании бактериофагов. Для фолдинга вирусных белков тоже нужны шапероны. Рассмотрим это на примере бактериофага Т4, который размножается в клетках E.Coli. Вирион Т4 включает три компонента – головку, хвост и хвостовые фибрилы (короткие и длинные). Головка представляет собой белковую полую капсулу (капсид) в виде многогранника и плотно упакованную в ней линейную молекулу ДНК. По последним данным, ДНК фага Т4 содержит около 250 генов. В состав же собранной фаговой частицы входит не более сотни различных белков. Остальные белки, кодируемые фаговой ДНК, играют вспомогательную роль: обеспечивают протекание разных стадий фаговой инфекции, в том числе и сборку готовых вирионов.
Среди этих вспомогательных белков имеются и шапероны. Т. е. фаг приносит с собой в клетку, помимо прочего, информацию о своих собственных шаперонах, которые будут обеспечивать фолдинг его собственных структурных белков. Совершенно поразительная «предусмотрительность »!
В то же время при фолдинге ряда фаговых белков используются и бактериальные шапероны.
Регуляция экспрессии генов.
Контроль экспрессии генов осуществляется на следующих уровнях:
на уровне транскрипции (контролируется время и характер транскрипции гена)
на уровне процессинга первичного транскрипта
при отборе зрелых мРНК для их транспорта в цитоплазму
на уровне трансляции - отбор в цитоплазме мРНК для трансляции на рибосомах
на уровне деградации - избирательная дестабилизация определенных типов мРНК в цитоплазме
на уровне активности белка - селективная активация, инактивация или компартментация молекул белка после их синтеза.
Экспрессия генов как у прокариот, так и у эукариот регулируется при помощи целого ряда механизмов. Некоторые из механизмов такого рода, действующие в бактериальных системах, изучены довольно хорошо, и два из них будут рассмотрены ниже, но о том, как действует реrуляторные механизмы в клетках эукариот, известно немного.
Концепция оперона в регуляции экспрессии генов у прокариот. Ген обычно неактивен, но когда необходим определенный белок, конкретный ген «активируется», что обусловливает производство этого белка. Таким образом, клетки имеют механизм, контролирующий количество любого белка в определенное время. Синтез белков регулируется генетическим аппаратом, а также факторами внутренней и внешней среды.
Структура оперона прокариот. В 1961 г. два французских биолога Ф. Джакоб и Ж. Моно предложили механизм регуляции генов, названный гипотезой оперона.
Оперон — это последовательность специальных, функциональных сегментов ДНК, а также структурных генов, которые кодируют и регулируют синтез определенной группы белков одной метаболической цепи, например, ферментов гликолиза. Оперон (регулируемая единица транскрипции) состоит из следующих структурных частей (специальных пocлeдoвaтeльноcтей нуклeoтидoв) (риc.22):
Промотор — участок ДНК, к которому присоединяется РНК- полимераза и начинается транскрипция.
Оператор — участок промотора, связывающий белок-регулятор.
Структурные гены (цистроны) — участки ДНК, кодирующие мРНК конкретных белков.
Терминаторный участок ДНК несет сигнал об остановке транскрипции.
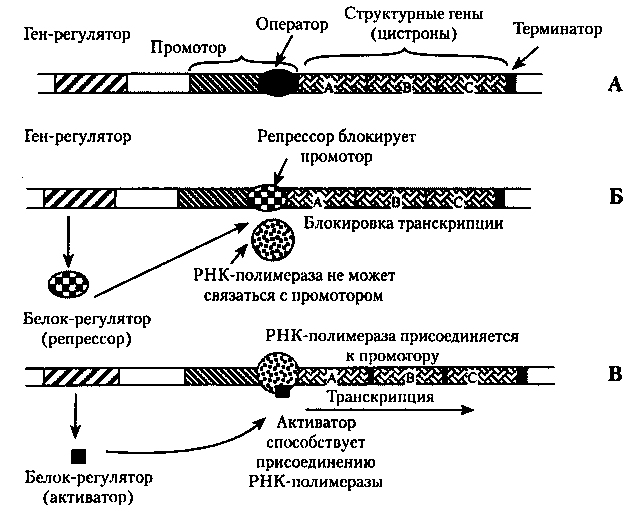
Рис.22. Схема структуры оперона (А): негативный контроль (Б) и позитивный контроль (В) экспрессии генов.
Основные механизмы регуляции функционирования оперона прокариот. Гены-регуляторы под действием клеточных факторов обусловливают синтез регуляторных белков. Такие белки, соединяясь с определенными нуклеотидными последовательностями ДНК (оператором), могут способствовать или препятствовать присоединению РНК-полимеразы к промотору. В случае если белок регулятор не дает возможность ферменту присоединяться к промотору, он называется репрессором (рис. 22, Б). В этом случае осуществляется негативный контроль транскрипции со стороны гена-регулятора. В случае если белок-регулятор способствует присоединению РНК-полимеразы к промотору и началу процесса транскрипции, его называют белком-активатором, и осуществляется позитивный контроль со стороны гена-регулятора (рис. 22, В). В процессах регуляции экспрессии генов принимают участие также вещества небелковой природы {эффекторы), взаимодействующие с белками-регуляторами и изменяющими их способность связываться с опероном. Например, конечный продукт метаболической цепи. В зависимости от результатов такого воздействия среди эффекторов различают индукторы, способствующие транскрипции, и корепрессоры, препятствующие ей.
Функционирование лактозного оперона Е. coli. В своих эксперементах Джакоб и Моно обнаружили, что добавление лактозы к культуре E.coli индуцирует образование сразу трех белков-ферментов: галактозидазы, пермеазы и трансацетилазы, необходимых клетке для расщепления лактозы до глюкозы и галактозы. Гены, кодирующие эти ферменты, соседствуют друг с другом в хромосоме. Их назвали структурными генами, или цистронами. Они одновременно транскрибируются РНК-полимеразой в длинную одиночную мРНК, которая имеет кодоны для всех трех ферментов. мРНК, трансрибируемая из нескольких генов, называется полицистронной. Способность к транскрипции этих цистронов контролируется участком молекулы ДНК — оператором. Операторный локус — это определенный участок оперона, имеющий определенную последовательность нуклеотидов, длиной 27 пар оснований. Этот сегмент ДНК располагается в области промотора, к которому перед началом транскрипции присоединяется РНК-полимераза. Промотор расположен перед началом первого структурного гена β-галактозидазы. Цистрон «синтезирует» мРНК, когда оператор включен и прекращает синтез, когда он «выключен». Оператор включается или выключается белком, называемым репрессором. Его синтез контролируется регуляторным геном. Репрессор либо связывается с оператором, подавляя его активность, либо не связывается с ним, позволяя проявление активности структурных генов. Таким образом, репрессор является негативным регулятором.
На рисунке 23 представлена схема функционирования лактозного оперона. Репрессия (I). При отсутствии индуктора (лактозы), репрессор связывается с оператором и блокирует транскрипцию, в этом случае ферменты не образуются. Индукция (II). Лактоза индуцирует транскрипцию генов, т.к. инактивирует репрессор. К промотору присоединяется РНК-полимераза и начинается транскрипция генов А, В и С. В результате образуются необходимые в данных условиях ферменты. Синтез ферментов может не только индуцироваться, но и подавляться.
Например, в результате какой-то цепи реакций в клетке образуется конечный продукт Д в большем, чем это необходимо клетке, количестве. Это может нарушить нормальный ход реакций обмена, поэтому в клетке возникает необходимость остановить данный процесс. Тогда вещество Д вступает в реакцию с соответствующим белком-репрессором и переводит его в активное состояние. После этого происходит присоединение репрессора к оператору, тем самым выключается вся система оперона и синтез ферментов прекращается. В данном случае, торможение синтеза производится конечным продуктом, образующимся в результате реакции. Такой механизм действия называется регуляцией по принципу обратной связи.
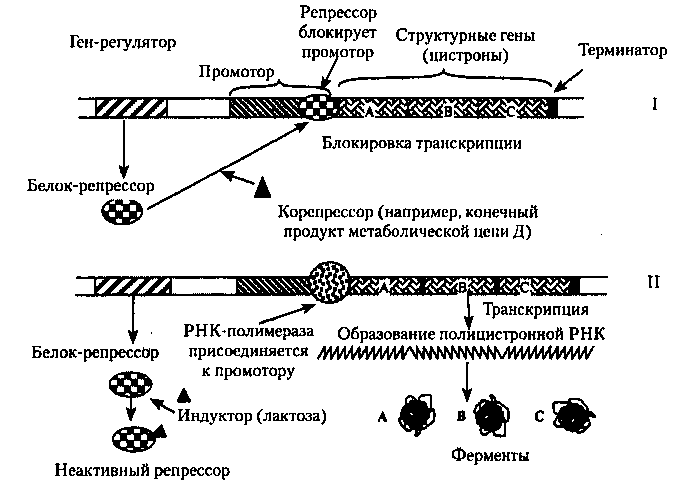
Рис.23. Схема функционирования лактозного оперона Е. соli
Описанный механизм регуляции имеет большое приспособительное значение. Например, согласно имеющейся генетической программе, кишечная палочка может синтезировать несколько десятков ферментов, расщепляющих различные вещества, так как состав среды, окружающей бактерии, очень изменчив. В этих условиях постоянное образование всего набора ферментов было бы неэкономичным для клетки, так как нецелесообразно продуцировать одновременно 60-80 ферментов, из которых в данных условиях среды могут понадобиться лишь 6-8. Поэтому синтез ненужных в этих условиях ферментов блокирован, а клетки образуют лишь несколько необходимых белков.
Еще одной разновидностью негативной регуляции является так называемая катаболитная репрессия. Репрессия происходит тогда, когда репрессор связывается с оператором не иначе, как в комплексе с низкомолекулярным кофактором (корепрессором). Таким корепрессором часто бывает конечный продукт белкового синтеза, кодируемый опероном. Тогда, если концентрация этого продукта становится слишком высокой, он связывается с репрессором и дальнейший его синтез прекращается. Примером такой системы может служить триптофановый оперон.
Триптофановый оперон состоит из оператора и пяти структурных генов (А-Е). Последние кодируют ферменты, участвующие в биосинтезе триптофана, одной из незаменимых аминокислот. По мере увеличения концентрации триптофана наступает момент, когда дальнейший его синтез становится нежелательным и транскрипция прекращается. «Выключение» транскрипции происходит следующим образом. Триптофан связывается с димерным репрессором (trр-репрессором), который кодируется отдельным, не входящим в оперон регуляторным геном. При этом происходит конформационное изменение, и открывается участок, способный связываться с операторной последовательностью в ДНК. Весь комплекс связывается далее с ДНК и блокирует место связывания с РНК-полимеразой (промотор). Это пример регуляции с помощью репрессии.
Вариация длины транскрипта - еще один механизм, посредством которого может осуществляться регуляция экспресии оперонов в бактериях. Так, в trр-опероне помимо репрессии используется и другая система регуляции. Она связана с наличием в ДНК участка, расположенного непосредственно перед первым структурным геном {trрЕ) и называемого аттенуатором. Аттенуатор представляет собой нуклеотидную последовательность, содержащую команду, по которой происходит преждевременная терминация транскрипции. В случае trр-оперона при высокой концентрации триптофана 90% всех транскриптов терминируется после транскрипции всего лишь 140 нуклеотидов и до начала транскрипции структурных trр-генов. Позитивная регуляция - еще один способ регуляции экспрессии гена (на рисунке не показан). Он отличается от негативной регуляции тем, что транскрипция «включается», а не «выключается» после присоединения регуляторного белка к оперону. Корепрессор, или скорее коактиватор, присоединяется к белку-активатору; далее весь комплекс связывается с соответствующим участком на ДНК, и лишь после этого может происходить транскрипция. Примером регуляции такого типа может служить процесс, происходящий при участии катаболитного белка-активатора, коактиватором которого является сАМР (см. дополнительную литературу). В отсутствие (или при низкой концентрации) сАМР, что имеет место при размножении бактерий в присутствии глюкозы, блокируется, таким образом, транскрипция некоторых оперонов, включая lαс-оперон. Такое явление называется катаболитной репрессией.
Контроль экспрессии генов у эукариот. Эукариотические организмы в значительной части представлены многоклеточными формами с высокой специализацией клеток. Все клетки многоклеточного организма возникают из зиготы путем митоза и получают полноценный набор генетической информации. Однако они отличаются друг от друга по морфологии, биохимическим и функциональным свойствам. Эти различия основаны на функционировании в разных клетках неодинаковых частей генома. Большая часть генома человека находится в клетках организма в неактивном, репрессированном, состоянии, и только 7-10 % активно транскрибируются. Функциональная активность генов зависит от тканевой принадлежности клетки, от периода ее, жизненного цикла и стадии индивидуального развития организма. Из активно функционирующих генов в большинстве клеток основная масса генов обеспечивает синтез белков общего назначения (белки рибосом, гистоны, тубулины и т.д.), тРНК и рРНК. Транскрибирование этих генов происходит путем присоединения РНК-полимеразы к промотору и называются они конститутивными генами. Существует еще одна группа генов, функционирование которых, а также скорость и продолжительность их транскрипции зависит от различных регулирующих факторов, стимулирующих или запрещающих соединение РНК-полимеразы с промотором гена. Называют эти гены - регулируемые. Хотя во всех клетках человека содержится совершенно одинаковая ДНК, в разных тканях происходит экспрессия далеко не одинаковых наборов генов. Таким образом, должны существовать какие-то механизмы, при участии которых одни гены работают (т.е. экспрессируются), а другие нет. Для этой цели используется целый ряд механизмов: регуляция на уровне транскрипции и на уровне трансляции, посттранскрипционная и посттрансляционная регуляция и регуляция с помощью гормонов.
Регуляция на уровне транскрипции осуществляется при синтезе мРНК. Средние концентрации индивидуальных мРНК, транскрибируемых с разных генов, сильно отличаются друг от друга. Это обусловлено тем, например, что мРНК-копии одних генов разрушаются быстрее других, либо тем, что их синтез происходит медленнее. Регуляция может осуществляться при помощи белков, способных связываться с ДНК, и даже при помощи коротких фрагментов РНК, которые спариваются с ДНК, предположительно блокируя места прикрепления РНК-полимеразы. Таким образом, скорость транскрипции может снижаться или, наоборот, повышаться.
Кроме более или менее постоянного статуса экспрессии, активность многих генов может быстро меняться под действием специальных регуляторов. Например, интенсивность транскрипции матричной рибонуклеиновой кислоты (мРНК) может временно увеличиваться или уменьшаться под влиянием белков, которые связываются с регуляторными зонами гена. Активность регуляторных белков, в свою очередь, контролируется рецепторами, локализованными или внутри клетки, или на ее поверхности. Разнообразные рецепторы распознают специфические молекулы, такие как стероидные гормоны, пептидные факторы роста и нейромедиаторы, и передают молекулярные сигналы внутрь клетки, что контролирует активность регуляторных белков, действующих на дезоксирибонуклеиновую кислоту (ДНК).
В транскрибируемой матрице ДНК выделяют две главные функциональные области — кодирующую и регуляторную. Матричная РНК транскрибируется с ДНК (кодирующей белок) с помощью фермента РНК-полимеразы II. Регуляторная область гена обычно находится перед началом кодирующей области. Регуляторные элементы ДНК располагаются рядом с кодирующей областью (примыкают к ней), они называются cis-регуляторными элементами. Напротив, факторы транскрипции регуляторных белков, связывающихся с субэлементами, являются trans-регуляторами по отношении к гену-мишени, поскольку кодирующие их гены находятся далеко (например, на другой хромосоме).
Регуляторная область структурного гена содержит участок, называемый промотором. Этот участок примыкает к точке начала транскрипции и в большинстве случаев содержит участок около 8 пар оснований, которые включают несколько адениновых (А) и тимидиновых (Т) нуклеотидов. Этот элемент, называемый ТАТА-блоком, окружен участками, богатыми гуанином (Г) и цитозином (Ц).
Белки – факторы транскрипции. ТАТА- блок и соседние элементы ДНК промотора указывают РНК-полимеразе точку, с которой должна начаться транскрипция мРНК. К ТАТА- блоку прикрепляется комплекс белков, называемых ТАТА-блок-связывающими белками. Полагают, что эти белки взаимодействуют непосредственно с РНК-полимеразой II, и их связывание направлено на область ДНК, прилежащую к точке начала транскрипции. Другие регуляторные элементы ДНК часто находятся рядом с ТАТА- блоком. К ним относятся СААТ-блок и G-C-богатые участки, которые, вероятно, способствуют начальному связыванию полимеразы. Другие регуляторные зоны ДНК называются энхансерами («усилительными»).
Энхансеры могут располагаться внутри нескольких сот оснований промотора, но обычно находятся далеко от него. Каждый отдельный сегмент энхансера имеет длину около 7-20 пар оснований и служит местом прикрепления белков, которые контролируют возможность транскрипции гена с помощью РНК-полимеразы II. Интересно, что энхансеры не специфичны ни к последовательности- мишени, ни к своей ориентации. Последовательности энхансера или промотора ДНК, к которым прикрепляются тканеспецифичные регуляторные молекулы, называются респонсивными элементами. Например, респонсивный элемент циклического аденозинмонофосфата (сАМР) состоит из последовательности ACGTCA; именно эту последовательность узнают молекулы сАМР (сАМР — элемент-связывающиеся белки), которые активируются путем фосфорилирования с помощью сАМР-зависимой протеинкиназы. Известны и другие респонсивные элементы. Например, внутриклеточные рецепторы стероидных гормонов, гормон роста и другие белки связываются с особыми последовательностями ДНК и контролируют транскрипцию генов, лежащих рядом (правее) с местом прикрепления этих белков. Некоторые гены, так называемые конститутивно экспрессирующиеся гены, имеют регуляторные белки, которые всегда связаны с их промоторами; таким образом, устанавливается постоянный уровень транскрипции. Промоторы других генов связаны с регуляторными белками только периодически, что обеспечивает временную индукцию или репрессию гена соответствующими регуляторами транскрипции. Свяжется ли РНК-полимераза II с геном, начнется ли транскрипция, и сколько раз в единицу времени это произойдет, определяется регуляторами транскрипции, которые соединяются с различными участками промоторов и энхансеров. Факторы транскрипции, которые связываются с регуляторными областями генов, как правило, имеют три функциональных отдела (домена):
ДНК-связывающий домен, который содержит много щелочных аминокислотных остатков и позволяет белку распознавать и избирательно связываться со специфической последовательностью ДНК.
Активаторный домен, имеющий кислую реакцию, который позволяет белку контактировать и активировать основной транскрипционный механизм (ТАТА-блок- связывающие белки и РНК-полимеразу II).
Один или более лиганд-связывающих или фосфорилирующих доменов, которые требуются для активации факторов транскрипции. Факторы транскрипции ДНК служат ключевыми регуляторами экспрессии гена, поэтому их биохимические свойства являются предметом интенсивного изучения.
Мы знаем на данный момент три основных семейства белков – факторов транскрипции:
Белки «спираль-поворот-спираль» (helix-tum-helix). Эта группа ДНК-связывающих белков представлена в большинстве случаев гомодимерами. Каждая субъединица белка содержит альфа-спираль, которая подходит к большой бороздке спирали ДНК. Это «узнающий домен». Остальная часть белка всегда выгибается из молекулы ДНК и обвивает ее, а вторая альфа-спираль белка входит в большую бороздку на следующем витке ДНК. Когда такие белки соединяются с участком ДНК, они изменяют конформацию ДНК и делают ее либо более доступной для транскрипции (и тогда они служат «индукторами»), либо менее доступной (тогда они работают как «репрессоры»).
Белки типа «цинковый палец». Белки этой группы названы так потому, что они имеют участок приблизительно из 23 аминокислот, который содержит чередующиеся остатки цистина и гистидина и формирует пальцевидные выступы, чья структура поддерживается благодаря связанным ионам цинка. Такие белки взаимодействуют с ДНК с помощью петлевидных участков. Рецепторы глюкокортикоидов, эстрогенов, витамина А, прогестерона, гормонов щитовидной железы и ретиноевой кислоты содержат по два «цинковых пальца».
Амфифильные спиральные белки. Эта группа включает две подгруппы: белки «спираль-петля-спираль» (helix-loop-helix) и белки типа «лейциновой молнии». Белки-регуляторы, имеющие структуру типа «лейциновых молний», могут формировать либо гомодимеры, в которых обе субъединицы идентичны, либо гетеродимеры, в которых субъединицы не похожи друг на друга. Гетеродимеры состоят из двух различных белков с разной специфичностью к ДНК, поэтому способность определенных факторов транскрипции к формированию функциональных димеров значительно увеличивает разнообразие ДНК- связывающих белков и, следовательно, вариабельность контроля гена. Образование гетеродимеров и даже олигомеров ДНК- связывающих белков (т.е. комбинационный контроль) — один из важнейших механизмов, используемых эукариотической клеткой для регуляции экспрессии генов. Также важно, что не все факторы транскрипции формируют гетеродимеры. Иначе перекрестный контроль и специфичность регуляции генов в клетке были бы невозможны.
Очевидно, что уровень транскрипции генов — главный фактор в регуляции жизнедеятельности и морфологии клетки. Однако это не единственная возможность воздействовать на клеточный фенотип. Как показали многочисленные исследования, другие события также важны для контроля экспрессии генов. Например, в дополнение к транскрипции гена, создающей мРНК, молекулярный аппарат должен воспринимать сигналы самого гена; то есть должны быть вырезаны интроны (сплайсинг мРНК) и добавлены другие компоненты, обеспечивающие функциональность мРНК. После такого процессинга мРНК должна быть перенесена из ядра в цитоплазму. В цитоплазме на мРНК должна начаться трансляция белка. Механизмы трансляции мРНК требуют участия большого количества регуляторных молекул; недостаток или снижение активности любой из этих молекул может оказать сильное влияние на цитоплазматическую экспрессию продукта гена. В цитоплазме мРНК может быть быстро разрушена или защищена от деградации цитоплазматическими белками; стабильность и период полужизни мРНК — особый механизм генной регуляции. Окончательный продукт гена, белок, также должен быть функционально активным для проявления активности гена.
Посттранскрипционная регуляция осуществляется на уровне процессинга мРНК. Даже в том случае, если транскрипция двух разных генов проходит с одинаковой скоростью, дальнейший процессинг мРНК, включающий модификацию 5'- и 3'-концов и сплайсинг экзонов, может протекать по-разному у разных мРНК.
Регуляция на уровне трансляции осуществляется за счет того, что исключается возможность использования мРНК в качестве матрицы для синтеза белка, хотя она и присутствует в цитоплазме. В ооците морского ежа, например, много мРНК, но сколько-нибудь заметного синтеза белка не происходит до тех пор, пока ооцит не будет оплодотворен. Лишь после этого молекулы мРНК подвергаются модификации, т.е. «приобретают» шпильку на 5'-кoнцe (так называемый кэп, или «шапочку») и «шлейф» из роlу А на З'-конце, и могут далее включиться в нормальный трансляционный процесс, который завершается построением молекулы белка.
Посттрансляционная регуляция основана на том, что многие белки синтезируются в неактивной форме и должны еще пройти стадию модификации. Так, в ß-клетках поджелудочной железы синтезируется не инсулин как таковой, а его предшественник, полипептидная цепь которого длиннее инсулиновой и содержит еще некоторую добавочную последовательность аминокислотных остатков. Лишь после того, как эта последовательность вырезается протеолитическим ферментом, получается собственно гормон в своей функциональной форме. Таким образом, производство активного гормона может регулироваться посттрансляционным путем через регуляцию активности протеолитического фермента.
Эпигенетическая регуляция экспрессии генов. Процессы, управляющие программой развития, называются эпигенетическими. Как известно, слияние одного сперматозоида с единственной яйцеклеткой приводит к рождению полностью сформированного индивида, со всем набором функционально различных тканей и органов.
Очевидно, программа развития, заложенная в генах зародыша, «включает» или «выключает» их (на время или навсегда) в заранее заданной последовательности. При этом изменяется состав белков во вновь формирующихся клетках и тем самым изменяются свойства клеток. Наличие программы развития не объясняет, почему судьба первых клеток различна. На ДНК должен действовать какой-то процесс, управляющий развертыванием программы, отбирающий те или иные гены для включения или выключения в данной клетке в данное время. Без этого все соматические клетки тела, имеющие одни и те же хромосомы, развивались бы одинаково. Кроме того, что-то должно управлять передачей распределения состояний «включен-выключен» между генами от одного поколения клеток к другому. Дочерним клеткам предназначается сохранить уровень дифференцировки родительской клетки или же продвинуться дальше по пути специализации.
С генетической точки зрения вопрос о причинах дифференцировки 100 триллионов (1014) клеток организма человека, имеющих единый геном, сводится к проблеме дифференциальной экспрессии генов в разных клетках развивающегося организма. Становится все более очевидным, что стабильное поддержание этих различий обусловлено эпигенетическим контролем генной экспрессии. В настоящее время под эпигенетической изменчивостью понимается изменение экспрессии генов без изменения первичной последовательности нуклеотидов в ДНК. В более узком смысле слово «эпигенетика» означает модификацию генной экспрессии, обусловленную наследственными, но потенциально обратимыми изменениями в структуре хроматина и/или в результате метилирования ДНК. Интенсивные исследования регуляции активности генов различных видов микроорганизмов, растений, насекомых, животных и человека и секвенирование геномов, выполненные в последние десятилетия XX в., ознаменовались открытием ряда эпигенетических феноменов, к которым можно отнести эффект положения, парамутацию, трансвекцию, РНК-интерференцию, явление прионизации, супрессию транспозонов, геномный импринтинг и инактивацию Х-хромосомы.
Под эффектом положения понимают изменение фенотипического эффекта гена в зависимости от расположения соседних с ним генов. Этот эффект был обнаружен А. Стертевантом в 1925 г. у дрозофилы. У данного объекта часто наблюдается изменение экспрессии эухроматинового гена в результате его перемещения в гетерохроматиновую область генома. Эффект положения был обнаружен впоследствии у многих организмов, включая человека. Следует отметить, что корректная экспрессия генов зависит от ряда факторов: 1) состояния промоторной области, где фиксируется транскрипционный комплекс; 2) состояния энхансеров и сайленсеров - коротких областей ДНК, обеспечивающих присоединение тканеспецифичных транскрипционных факторов и помогающих сборке транскрипционного комплекса на промоторе; 3) локального состояния хроматина, окружающего промоторы и энхансеры, которое обеспечивает их доступность для белков, участвующих в контроле транскрипции. Нарушение любого из этих факторов, а также изменение взаиморасположения отдельных элементов, контролирующих работу транскрипционного комплекса, могут привести к изменению транскрипции гена.
Под парамутацией понимают такое взаимодейстие аллельных генов, находящихся в гетерозиготном состоянии, которое приводит к наследуемому изменению экспрессии одного из аллелей. Термин «парамутация» был введен Р.А. Бринком в 1956 г. для описания обнаруженного им нарушения I закона Менделя, согласно которому генетические факторы сегрегируют в неизмененном виде от гетерозиготных носителей. Предполагается, что парамутация также связана с наследственными изменениями структуры хроматина, проявляющимися через дистантные цис- и транс- взаимодействия генов.
Под трансвекцией понимают взаимодействие гомологичных генов, при котором один ген оказывает прямое влияние на функцию другого путем спаривания гомологов. В качестве примера трансвекции служит локус уеllou у дрозофилы - энхансер одного аллеля этого локуса в трансположении влияет на промотор другого гомолога. Модели трансвекции включают прямое влияние гомологичных последовательностей ДНК друг на друга в результате образования петельных структур, трансдействующих энхансеров, диффундирующих регуляторных молекул РНК, прыгающих полимераз, транссплайсинга и т.д.
Эпигенетическую наследственность можно разделить на ядерную и внеядерную (цитоплазматическую). У растений, например, известно явление косупрессии, или посттранскрипционное выключение гена, связанное с посттранскрипционной цитоплазматической модификацией двуспиральной РНК. Двуспиральная РНК с помощью пока еще не ясного биологического превращения распадается на короткие кусочки - интерферирующую РНК, которая запускает деградацию соответствующей матричной РНК. Процесс такой специфической деградации определенных последовательностей информационной РНК, инициированный двуспиральными молекулами РНК, гомологичными к выключаемому гену, и приводящий к выключению его экспрессии, получил название «РНК-интерференции» (см. 1.2.4).
РНК-интерференция часто приводит к неблагоприятным последствиям для организма, формируя аномальный фенотип, что позволяет идентифицировать функцию данных генов.
Другое явление цитоплазматической наследственности - прионизация - связано уже с модификацией белков. Это явление привлекает внимание исследователей в связи с тяжелыми нейродегенеративными заболеваниями с поздним проявлением, возникающими в результате воздействия приона - инфекционного агента белковой природы, лишенного нуклеиновой кислоты. Эти болезни характеризуются атаксией, деменцией, дегенерацией нейронов и отложением амилоидных бляшек в центральной нервной системе. Установлено, что они возникают в результате накопления конформационно измененного аномального прионового белка в мозге при мутациях гена РККР (20р12). К числу таких заболеваний принадлежит болезнь Крейнцфельда-Якоба, куру, семейная фатальная бессонница и трансмиссивная губчатая энцефалопатия - болезнь бешеных коров.
У многих организмов эпигенетическое выключение генов связано с повторяющимися последовательностями ДНК, локализованными преимущественно в гетерохроматиновых областях генома. Гетерохроматин включает как простые повторы, так и неактивные мобильные генетические элементы - транспозоны. Число транспозонов в геноме человека достаточно велико – известно более 106 элементов. Поскольку транспозоны дестабилизируют геном путем инсерционного мутагенеза и способствуют хромосомным перестройкам через рекомбинацию между неаллельными повторами, то предполагается, что роль эпигенетической супрессии транспозонов в геноме млекопитающих заключается в защите хозяина против паразитических последовательностей ДНК.
Геномный импринтинг - это эпигенетический процесс, дифференциально маркирующий материнские и отцовские гомологичные хромосомы, приводящий к разному фенотипическому проявлению мутаций у потомства, унаследованных от матери или отца.
В генетическом смысле термин «импринтинг» (от английского «отпечаток») впервые был применен в 1960 г. Хелен Кроуз для описания селективной элиминации отцовских хромосом у насекомых.
В 80-х годах в экспериментах с трансплантацией ядер половых клеток у мышей было показано, что андрогенетические или гиногенетические эмбрионы не могли нормально развиваться в ходе эмбриогенеза.
В участках генома, подверженных импринтингу, экспрессируется только один из двух аллелей - отцовский или материнский. Второй аллель импринтирован (выключен или подавлен) и не экспрессируется.
Такой способ регуляции работы генов свидетельствует о неэквивалентном вкладе родителей в геном потомков. Все мы получаем один набор генов от матери, другой - от отца. У большинства генов работают обе копии. Но есть такие гены, у которых работает только материнская. У некоторых других только отцовская копия. Другая копия в этом случае не действует, «молчит»; говорят что она «находится под импринтингом». Известно около 40 таких генов.
Обычно для синтеза любого белка организму достаточно одной копии гена. Если в геноме развивающегося зародыша есть и материнские и отцовские гены, то любой импринтированный, «молчащий» ген имеет свою работающую копию. Тогда все в порядке. Однако если составить геном зародыша только из материнских или отцовских хромосом, то «молчать» будут обе копии.
У человека известно около 30 таких генов и транскриптов и предполагается, что их число может достигать 200-500. Импринтированные гены и транскрипты обнаружены на многих хромосомах человека- 1,5,6,7 и 13,15,19,20.
В настоящее время хорошо изученным является кластер импринтированных генов, расположенный на длинном плече хромосомы 15 человека. Нарушение работы данных генов приводит к двум классическим болезням геномного импринтинга – синдром Прадера-Вилли (СПВ) и синдром Ангельмана (СА). Эти заболевания имеют разные клинические признаки (гипотонсиндромия, ожирение, умственная отсталость, гипогонадизм при СПВ и атаксия, гиперкинезы, пароксизмальный смех, отсутствие речи при СА), но при цитогенетическом исследовании в обоих случаях у большинства больных выявляется делеция общего участка д11- д13 хромосомы 15. При анализе родительского происхождения хромосом обнаружено, что СПВ возникает в результате делеции отцовской хромосомы- 15, а СА- материнской.
Известно, что проявление умственных и социальных качеств человека (поведение в социуме) обусловлено разным функционированием определенных генов, передаваемых от отца или от матери своим потомкам в зависимости от пола последних. Судя по исследованиям больных детей с нарушением строения Х-хромосомы, именно в ней находятся гены, от которых зависят познавательные способности человека и его социальное поведение. Так как сын получает только одну, материнскую, Х-хромосому, его умственные и социальные возможности, в первую очередь наследуются от матери. Иное дело дочери, геном которых формируется Х-хромосомами обоих родителей. Здесь вступает в силу механизм импринтинга: материнские или отцовские копии генов, определяющих интеллект и социальное поведение, выключаются. Следовательно, социальное поведение женщины зависит от отцовской Х-хромосомы, которая всегда наследуется дочерьми. Информация, которая хранится в материнской Х-хромосоме и проявляется у сыновей, не будет считываться в организме дочери. В передаче интеллекта участвуют и другие гены той же хромосомы. Материнские копии некоторых из них активируют рост коры головного мозга, а отцовские наоборот - тормозят.
В настоящее время предложены, по крайней мере, две теории, объясняющие функцию геномного импринтинга. Первая из них - конфликтная теория отцовского и материнского геномов в регуляции роста плода. Увеличение плаценты и массы плода может обеспечить преимущественное размножение потомков по линии отца, но истощит ресурсы матери. Однако если рост плаценты и плода находится под контролем со стороны матери, то она сможет обеспечить воспроизводство большего числа потомков по своей линии. Отсюда можно предполагать, что мать будет импринтировать или выключать гены, способствующие росту плаценты и плода, тогда как отец будет выключать гены, препятствующие этому росту.
Вторая (защитная) теория объясняет роль геномного импринтинга с точки зрения защиты генома хозяина от проникновения в него чужеродных элементов. Согласно этой теории, импринтинг, и в частности метилирование ДНК, это защитный механизм, обеспечивающий инактивацию паразитических последовательностей ДНК, таких как транспозоны и провирусная ДНК.
Определение импринтированной экспрессии какого-либо гена в отдельной ткани вовсе не означает, что этот ген будет импринтирован во всех остальных. И наоборот, отсутствие импринтированного статуса гена в некоторых тканях вовсе не исключает его наличия в других. Эти данные подтверждают предположение о том, что тканеспецифичная эпигенетическая модификация генов является одним из основных механизмов, обеспечивающих дифференциальную экспрессию генов клеток разных тканей в ходе развития.
Установлено, что в основе эпигенетической «маркировки» отдельных участков генома и явления геномного импринтинга в частности лежат специфические структурно-молекулярные изменения отдельных участков хромосом, происходящие во время формирования мужских и женских половых клеток, которые приводят к стойким функциональным различиям экспрессии гомологичных генов у потомства. Основную роль в этом процессе отводят специфическому для особей разного пола метилированию цитозиновых оснований в ЦГ-динуклеотидах ДНК, которое устанавливается во время гаметогенеза и выключает транскрипцию генов.
Специфические для родителей эпигенетические отпечатки, подавляющие транскрипцию генов, стираются в примордиальных половых клетках плода и вновь устанавливаются в зрелых половых клетках потомка в соответствии с его полом, обеспечивая дифференциальную экспрессию отцовских или материнских генов в следующем поколении.
Тканеспецифичное метилирование цитозиновых остатков ДНК у млекопитающих осуществляется с помощью 4-х ДНК-метилтрансфераз и поддерживает специфический рисунок метилирования (рис. 24) в митотически размножающихся клетках. После репликации две полуметилированные дочерние молекулы ДНК распознаются этим ферментом и конвертируются в полностью метилированные.
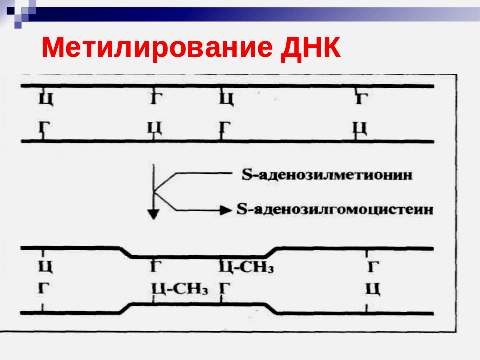
Рис.24. Метилирование ДНК
Более того, существует предположение, что нарушение эпигенетической регуляции генов может определять развитие комплексных (мультифакториальных) заболеваний, Поддержка нужного статуса метилирования генома является непременным условием нормального развития у мышей, а аберрантное метилирование связано с возникновением опухолей и аномалий развития у человека.
В последние годы стало ясно, что механизм компактизации- декомпактизации хроматина напрямую связан с репрессией- дерепрессией локализованных в нем генов, и установлен особый класс заболеваний человека, обусловленный дефектами структуры и модификации хроматина - так называемые «хроматиновые болезни». Показано, что к метилированной ДНК присоединяются белки, распознающие метилированные основания благодаря наличию в них особых метил-ЦГ-связывающихся доменов. Известны 4 вида таких белков. Они взаимодействуют с гистонами.
Деацетилирование гистонов, ремоделирует структуру хроматина, повышая степень его компактизации, что приводит к репрессии транскрипции. Ацетилирование гистонов, наоборот, снимает репрессию.
Процессы метилирования тесно связаны с возникновением опухолей. Предполагается, что в процессе эволюции метилирование возникло уже у одноклеточных как средство защиты от проникновения в клетку чужих ДНК, например вирусных. Метилирование могло бы инактивировать гены инфекционных агентов, проникающих в клетку. Метилирование могло бы также препятствовать размножению так называемых подвижных элементов генома, которые часто рассматриваются как геномные паразиты, цель которых состоит лишь в распространении по геному собственной ДНК.
Система метилирования генов и геномный импринтинг возникли у позвоночных. У беспозвоночных метилирование цитозина, как правило, отсутствует.
По своей сути, метилирование - событие эпигенетическое. Нарушение регуляции метилирования в эмбриогенезе может приводить к гибели организма. Изменение степени метилирования в соматических клетках взрослого организма наблюдается при некоторых патологических состояниях у человека, в том числе и злокачественных новообразованиях.
Проблема геномного импринтинга из общебиологической перешла в практическую область исследований клинической генетики. Дальнейшее его изучение позволит улучшить диагностику и профилактику целого ряда наследственных заболеваний.
Многие исследователи считают, что у высших организмов важным эпигенетическим процессом может быть химическая модификация ДНК. В частности, в управлении генетическим переключением в развивающихся клетках может участвовать присоединение метильной (СН3) группы к цитозину, т.е. метилирование ДНК.
Очевидно, от одного поколения клеток к другому передаются без изменения не какие-либо регуляторные белки, а метильные группы в составе ДНК. Возможно, что наличие или отсутствие метильных групп служит сигналом для регуляторных белков и в результате эти белки взаимодействуют с ДНК в дочерних клетках так же, как в родительской клетке. Эксперименты по активации генов в культурах клеток весьма убедительно свидетельствует в пользу связи между генной экспрессией и метилированием ДНК.
Так, исследование половых хромосом женского организма (ХХ) показало, что они метилированы неодинаково. В частности, в неактивной Х-хромосоме оказались метилированными участки регуляторных генов «внутреннего употребления» (т.е. гены, активные во всех клетках). В активной же гомологичной хромосоме эти участки не метилированы. Таким образом, метилирование ДНК – важный эпигенетический фактор в развитии высших организмов. Функции генов взаимосвязаны и могут изменяться вплоть до дифференциального выключения одного из аллелей на протяжении всего онтогенеза. Такие случаи наследования объясняют генетическим импринтингом.
Генетический импринтинг может проявляться не только на уровне гена или кластера генов. Он может затрагивать целую хромосому (однородительские дисомии) и даже геномы. Эффекты геномного импринтинга у человека изучены на примере пузырного заноса (табл.4).
Табл.4. Последствия разных вариантов импринтинга целого генома у человека
Генетическая «композиция» |
Последствия |
1.Хромосомный набор 2n. Яйцеклетка без ядра. Два сперматозоида с Х-хромосомами (андрогенез)
2.Хромосомный набор 2n. Яйцеклетка с двойным набором хромосом. Сперматозоиды не участвуют в оплодотворении (гиногенез) 3.Хромосомный набор Зn. Андроид (2 отцовских + 1 материнский)
4.Хромосомный набор Зn. Гиноид (2 материнских + 1 отцовский) |
1.Ранний эмбриогенез нормальный. Далее ткани собственно эмбриона не формируются. Бурно разрастается трофобласт с образованием полного пузырного заноса 2.Образуется тератома, включающая все 3 зародышевых листка. Плацентарная ткань отсутствует
3.Большая голова плода. Маленькое веретенообразное тело. Отставание в росте и развитии. Частичный пузырный занос 4.Плацента недоразвита. Эмбрион и плод не развиваются (недифференцированная клеточная масса) |
Из представленных в таблице данных можно сделать вывод, что развитие плаценты обеспечивается геномом отца, а раннее развитие эмбриональных структур обеспечивается геномом матери.
Гормональная регуляция экспрессии генов. Регуляция с помощью гормонов - это частный случай регуляции на уровне транскрипции. Таким путем организм заставляет клетку «включить» определенные гены в ответ на внешний стимул. Так, стероидные гормоны из тех клеток, где они были синтезированы, попадут, в конечном счете, в цитоплазму соответствующих клеток-мишеней, откуда специальный транспортный белок перенесет их в ядро, где они смогут активировать те или иные гены путем прямого взаимодействия с хроматином в соответствующих местах. Каждый гормон активирует свой набор генов. Таким способом обеспечивается соответствие реакции клетки роду сигнала, который клетка воспринимает через посредничество соответствующего гормона. Гормоны связываются с особыми белками рецепторами, образуя с ними комплекс. Активированный гормоном рецептор приобретает способность узнавать определенные последовательности ДНК, в результате ген инактивируется.
Например: влияние тестостерона на развитие тканей организма по мужскому типу при наличии специфического белка-репрессора.
Установлено, что одно лишь присутствие гена Y-хромосомы, который определяет дифференцировку половых желез по мужскому типу и синтез гормона тестостерона, не способно обеспечивать развитие организма мужского типа. Для этого необходим также белок-рецептор, обеспечивающий проникновение гормона в клетки тканей-мишеней. 3а синтез такого белка отвечает особый ген, расположенный в другой хромосоме. Его мутация, нарушающая образование нормального белка-фермента, делает ткани-мишени невосприимчивыми к гормону, направляющему их развитие по мужскому типу. В результате гормон не проникает в клетку-мишень и не включается определенный набор генов. Не использовав такую возможность на определенном этапе онтогенеза, организм осуществляет развитие по женскому типу. В результате появляется особь с кариотипом ХY, но внешне более сходная с женщиной. Такие люди не способны иметь потомство, так как половые железы (семенники) недоразвиты, а их выводные протоки часто формируются по женскому пути (недоразвитая матка, наличие влагалища). Т. о., вторичные половые признаки формируются такие же, как и у женщины. Эта патология называется тестикулярная феминизация или синдром Морриса.
Контроль на уровне трансляции и посттрансляционных процессов.
Регуляция на уровне трансляции осуществляется за счет того, что исключается возможность использования мРНК в качестве матрицы для синтеза белка, хотя она и присутствует в цитоплазме. В ооците морского ежа, например, много мРНК, но сколько-нибудь заметного синтеза белка не происходит до тех пор, пока ооцит не будет оплодотворен. Лишь после этого молекулы мРНК подвергаются модификации, т.е. «приобретают» шпильку на 5'-кoнцe (так называемый кэп, или «шапочку») и «шлейф» из роlу А на З'-конце, и могут далее включиться в нормальный трансляционный процесс, который завершается построением молекулы белка.
Регуляция основана на том, что многие белки синтезируются в неактивной форме и должны еще пройти стадию модификации. Так, в ß-клетках поджелудочной железы синтезируется не инсулин как таковой, а его предшественник, полипептидная цепь которого длиннее инсулиновой и содержит еще некоторую добавочную последовательность аминокислотных остатков. Лишь после того, как эта последовательность вырезается протеолитическим ферментом, получается собственно гормон в своей функциональной форме. Таким образом, производство активного гормона может регулироваться посттрансляционным путем через регуляцию активности протеолитического фермента.
Роль пептидов вилона и эпиталона в генной экспрессии. Изучение молекулярно-генетических механизмов геропротекторного действия коротких пептидов позволило разработать показания для их медицинского применения при возрастной патологии и ускоренном старении. Для этого у животных и людей исследовали в динамике уровень экспрессии различных генов, интенсивность синтеза ДНК в клетках и показатели внутриклеточного метаболизма Результаты экспериментальных исследований коротких пептидов подтвердили предположение о том, что пептидные биорегуляторы обладают свойством контролировать экспрессию генов и процессы синтеза белка в клетках.
Так, при изучении действия пептидов вилона и эпиталона установлено, что они меняют профиль генной экспрессии в миокарде при введении мышам in vivo. Влияние вилона и эпиталона на экспрессию генов IL-2 и c-fos обусловливает иммуномодулирующие, онкомодифицирующие и стресс-протекторные свойства этих пептидов.
Данные, полученные при изучении влияния вилона и эпиталона на канцерогенез у трансгенных мышей, подтверждают это предположение и также свидетельствуют о воздействии исследуемых пептидов на экспрессию гена рака молочной железы HER-2/neu. Впервые установлены механизмы геропротекторного действия коротких пептидов, связанные с активацией хроматина в лимфоцитах крови пациентов старческого возраста.
Эффекты эпиталона, связанные с увеличением ферментативной активности теломеразы, удлинением теломер в различных клетках и увеличением продолжительности жизненного цикла диплоидных человеческих клеток за счет преодоления лимита Хейфлика являются крупнейшим достижением современной биогеронтологии и подтверждают перспективность разработки пептидных геропротекторных средств. На основании изучения влияния пептидов на экспрессию различных генов и синтез ДНК в различных экспериментальных моделях, выдвинуто предположение, что, короткие пептиды являются активаторами и агонистами факторов транскрипции. Следует полагать, что первичным стартовым сигналом для связывания фактора транскрипции с промотором является сайт-специфическое связывание пептида в большой канавке ДНК.
Дальнейшее развитие этого направления позволит по-новому подойти к изучению механизмов старения и выяснению многих вопросов геронтологии. Расширение представлений о молекулярно-генетических механизмах действия пептидов может привести к пересмотру традиционных подходов к созданию геропротекторных средств и методов профилактики ускоренного старения и возрастной патологии.
