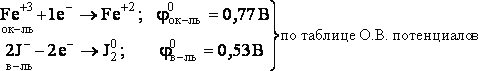- •8. Окислительно-восстановительные процессы
- •8.1 Окислительно-восстановительные реакции
- •8.1.1. Степень окисления элементов
- •8.1.2. Составление уравнений окислительно-восстановительных реакций
- •8.2. Типы окислительно-восстановительных реакций
- •8.3. Направление окислительно-восстановительных реакций
- •8.4. Электрохимические процессы
- •8.4.1. Электродный потенциал
- •8.4.2. Уравнение Нернста
- •8.4.3. Гальванические элементы
- •8.4.4. Электродвижущая сила гальванического элемента
- •8.4.5. Измерение э.Д.С. Гальванического элемента
- •8.5. Химические источники тока
- •8.5.1. Гальванические первичные элементы
- •8.5.2. Аккумуляторы
- •8.5.3 Топливные элементы и электрохимические энергоустановки
- •8.6. Электролиз
- •8.6.1. Электролиз расплавов
- •8.6.2. Электролиз водных растворов
- •8.6.3. Законы электролиза
- •8.6.4. Электрохимическая поляризация при электролизе
- •8.6.5. Перенапряжение. Потенциал разложения
- •8.6.6. Выход по току
- •8.6.7. Применение электролиза
- •8.7. Коррозия металлов
- •8.7.1. Химическая коррозия
- •8.7.2. Электрохимическая коррозия
- •8.7.3. Методы защиты металлов от коррозии
8.2. Типы окислительно-восстановительных реакций
1. Межмолекулярные – изменяются С.О. атомов элементов, входящих в состав разных веществ:
![]()
2. Внутримолекулярные – окислитель и восстановитель - атомы одной молекулы:
tº
![]()
3. Самоокисления – самовосстановления (диспропорционирования) – один и тот же элемент повышает и понижает С.О.
![]() .
.
Cl2 - является окислителем и восстановителем.
8.3. Направление окислительно-восстановительных реакций
О направлении ОВР можно судить по изменению энергии Гиббса ∆G. Если ∆G < 0 – реакция возможна, если ∆G > 0 - невозможна. Из термодинамики известно, что ∆G = -n·F·E; E = φок-ля -φв-ля или φок-ля > φв-ля, что возможно при Е > 0 и ∆G < 0.
Рассмотрим реакцию:
![]() .
.
Она состоит из двух полуреакций:
|
|
|
|
|
|
.
Т.к. φок-ля > φв-ля, то возможно самопроизвольное протекание реакции слева направо.
2FeCl3 + 2KJ → 2FeCl2 + J2 + 2KCl
Из всех возможных при данных условиях О.В.Р. в первую очередь протекает та, которая имеет наибольшую разность окислительно – восстановительных потенциалов.
О.В.Р. протекают в сторону образования более слабых окислителей и восстановителей из более сильных.
Роль окислительно-восстановительных процессов. О.В.Р. играют важную роль в природе и технике. О.В.Р. – это процессы фотосинтеза у растений, процессы дыхания у животных и человека, процессы горения топлива. Иногда О.В.Р. наносят ущерб природе и человеку, например, при коррозии металлов, лесных пожарах, образовании токсичных диоксинов.
При помощи О.В.Р. получают металлы, органические и неорганические соединения, проводят анализ различных веществ, очищают природные и сточные воды, газовые выбросы.
8.4. Электрохимические процессы
Электрохимические процессы это окислительно-восстановительные реакции, которые сопровождаются возникновением электрического тока или вызываются электрическим током.
В электрохимических процессах окислительная и восстановительная полуреакции пространственно разделены, а электроны переходят от восстановителя к окислителю не непосредственно, а по проводнику внешней цепи, создавая электрический ток. В О.В.Р этого типа наблюдается взаимное превращение химической и электрической форм энергии.
Выделяют две группы электрохимических процессов:
процессы превращения электрической энергии в химическую (электролиз);
процессы превращения химической энергии в электрическую (гальванические элементы).
Простейшая электрохимическая система состоит из двух электродов – проводников первого рода с электронной проводимостью, находящихся в контакте с жидким (раствор, расплав) или твердым электролитом - ионным проводником второго рода. Электроды замыкаются металлическим проводником, образующим внешнюю цепь электрохимической системы.
8.4.1. Электродный потенциал
При погружении в раствор электролита или воды активного металла его поверхностные ионы, находящиеся в узлах кристаллической решетки, вступают в различные взаимодействия с компонентами электролита. В результате на границе металл – раствор возникает разность потенциалов, называемая электродным потенциалом.
Если активный металл (Zn, Fe, Ca) погрузить в раствор его соли, полярные молекулы H2O, действуя своими отрицательными полюсами на положительные ионы кристаллической решетки, «извлекают» их, переводят в раствор, который заряжается положительно. На поверхности металла остаются электроны, заряжая ее отрицательно. Между гидратированными катионами в растворе и поверхностью металла устанавливается подвижное равновесие:
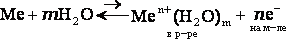
При погружении малоактивного металла (Cu, Ag, Pt) в раствор электролита протекает обратный процесс. Ионы из раствора переходят в кристаллическую решетку, заряжая металл положительно, а раствор за счет избытка анионов заряжается отрицательно.
На границе металл-жидкость возникает двойной электрический слой, характеризующийся определенным скачком потенциала - электродным потенциалом.
Абсолютные
значения электродных потенциалов
экспериментально определить невозможно.
Потенциал каждого электрода зависит
от природы металла, от концентрации
ионов металла в растворе, от температуры.
Поэтому электродные потенциалы измеряют,
сравнивая с потенциалом электрода
сравнения. Обычно применяют
газовый стандартный
водородный электрод,
потенциал которого стабилен и принимается
равным нулю.
Водородный электрод (рис. 21) представляет собой платиновую пластину 2, покрытую высодисперсной платиной (платиновой чернью). Пластина погружается в 1 М раствор серной кислоты 5,заливаемой в сосуд 1 трубку 3 с краном 4. Через трубку 6 с краном в раствор подается водород при давлении 101,3 кПа и температуре 25 ºС, омывающий электрод и насыщающий пористое покрытие платины. Из сосуда водород выводится через водяной затвор 7.
Платина, контактирующая с молекулами адсорбированного водорода, катализирует распад молекул на атомы. Атомы водорода, взаимодействуя с молекулами воды, переходят с поверхности в раствор в виде ионов. При этом платина заряжается отрицательно, а раствор – положительно. Наряду с переходом ионов в раствор на электроде идет обратный процесс восстановления ионов H+. Полуреакция этого процесса имеет вид:
![]()
![]()
Измеряя значение потенциалов металлов относительно водородного электрода в стандартных условиях, получают ряд стандартных электродных потенциалов или ряд напряжений:
![]()
Из ряда стандартных электродных потенциалов можно сделать следующие выводы:
-
Чем меньше величина электродного потенциала металла, тем сильнее выражены восстановительные свойства атомов, то есть тем активнее металл.
![]()
-
Чем больше величина потенциала, тем сильнее выражены окислительные свойства ионов металлов.
![]()
-
Более активный металл вытесняет менее активный из раствора его соли.
![]()
-
Металл, стоящий до водорода, вытесняет водород из растворов кислот
![]()