- •Основы теории горения топлив
- •1. Топливо
- •1.1. Состав топлива
- •1.2. Теплота сгорания топлива
- •1.3. Влага твердого топлива
- •1.4. Минеральные примеси твердого топлива
- •1.5. Выход летучих веществ и характеристика коксового остатка
- •1.6. Характеристики и классификация твердого топлива
- •1.7. Жидкое топливо
- •1.8. Газовое топливо
- •2. Материальный и тепловой баланс процессов горения
- •2.1. Теоретически необходимое количество воздуха
- •2.2. Объем продуктов сгорания
- •2.3. Энтальпия продуктов сгорания
- •2.4. Виды топочных устройств
- •2.5. Тепловой баланс процесса горения
- •2.6. Определение избытка воздуха
- •3. Горение газовых и жидких топлив
- •3.1. Скорость химического реагирования
- •Закон действующих масс
- •Влияние давления на скорость реакции
- •Зависимость скорости реакции от состава смеси
- •3.2. Цепные реакции
- •Цепное горение водорода
- •Горение оксида углерода и углеводородов.
- •3.3. Распространение пламени
- •Пределы воспламенения
- •3.4. Определение кинетических констант горения
- •3.8. Горелка Бунзена
- •3.5. Условия устойчивой работы кинетических горелок
- •Стабилизация процесса горения
- •3.6. Турбулентное горение предварительно подготовленных смесей
- •3.7. Диффузионное горение газов
- •3.8. Горелки промышленных агрегатов
- •Инжекционные горелки
- •5 Диффузор
- •Газовые струи в поперечном потоке
- •Вентиляторные горелки [14]
- •Вертикально-щелевая горелка
- •Горелочные устройства энергетических котлов
- •Газомазутные горелки гмг
- •Диффузионные горелки
- •3.9. Горение жидких топлив
- •3.10. Конструкции мазутных форсунок Механические форсунки
- •Ротационная форсунка
- •Пневматические форсунки
- •4. Горение твердых топлив
- •4.1. Основы кинетики горения углерода
- •Основные химические реакции горения углерода
- •Теория гетерогенного горения углерода
- •Роль вторичного реагирования
- •Время выгорания частицы углерода
- •4.2. Слоевые топки
- •Топки с цепной решеткой
- •4.3. Моделирование слоевого сжигания угля
- •4.4. Горение угольной пыли в факеле
- •4.5. Свойства угольной пыли
- •Затраты энергии на размол топлива
- •4.6. Системы пылеприготовления
- •4.7. Пылеприготовительное оборудование Шаровая барабанная мельница
- •Молотковые мельницы
- •Среднеходные мельницы
- •Мельницы-вентиляторы
- •Сепараторы пыли
- •4.8. Сжигание высокореакционных топлив
- •Топки с прямым вдуванием и фронтальными горелками
- •Топки с плоскими параллельными струями
- •Вихревые топки низкотемпературного сжигания
- •Сжигание сильношлакующих углей
- •4.9. Сжигание низкореакционных топлив
- •Сжигание углей с тугоплавкой золой
- •Сжигание антрацитов
- •Двухкамерные топки с жидким шлакоудалением
- •Библиографический Список
- •620002, Г. Екатеринбург, ул. Мира, 19
- •620002, Г. Екатеринбург, ул. Мира, 19
Цепное горение водорода
Реакцией зарождения цепей является реакция диссоциации атома водорода Н2 + ν = 2Н. Далее идет последовательная цепь реакций:
Н + О2 = ОН + О
О + Н2 = ОН + Н
(ОН + Н2 = Н2О + Н)·2
Н + 3Н2 + О2 = 3Н + 2Н2О
Складывая эти реакции, причем последнюю дважды, чтобы исключить из итоговой реакции комплексы ОН, получим результирующую реакцию в виде Н + 3Н2 + О2 = 3Н + 2Н2О. Из последнего соотношения видно, что вступление одного атома водорода в реакцию параллельно с образованием конечных продуктов вызывает появление трех новых атомов водорода, т.е. имеется процесс разветвления цепей. Дальнейшее развитие цепей обусловливает прогрессивное нарастание свободных атомов и радикалов, поэтому со временем реакция ускоряется, приобретая взрывной характер.
Горение оксида углерода и углеводородов.
По разветвленным цепным реакциям протекает горение и других составляющих газообразных топлив: оксида углерода, метана и других углеводородов. На горение оксида углерода существенное влияние оказывает наличие в газе паров воды, которые участвуют в реакциях продолжения цепей. Поэтому в выражение для скорости горения оксида углерода входит концентрация паров воды:
![]() . (3.7)
. (3.7)
Как показывает эксперимент, сухой оксид углерода практически не горит. Это связано с тем, что в отсутствие радикалов Н и ОН горение СО не имеет разветвленного цепного механизма. При появлении атомарного кислорода О2 + ν = 2О, он тут же вступает в реакцию с оксидом углерода О + СО = СО2, что приводит к обрыву цепей. Появление в смеси радикалов Н и ОН приводит к образованию дополнительных радикалов О (Н + О2 = ОН + О). Кроме того, при протекании реакции ОН + СО = СО2 + Н дополнительно генерируются радикалы Н, что приводит к разветвленному механизму горения СО. Таким образом, при помощи водяных паров или водорода в пламени создаются концентрации Н и ОН, необходимые для реакций разветвления цепей.
Экспериментально установлено, что скорость горения углеродов меньше, чем скорость горения водорода и оксида углерода. Горение их протекает по более сложным механизмам, одновременно с процессом горения углеводородов протекают реакции термического разложения с образованием сажистого углерода. Полное описание горения метана предполагает рассмотрение более 400 реакций. Основные из них следующие: реакция отщепления первого атома водорода от метана в присутствии кислорода (СН4 + О2 СН3 + Н + О2), образование радикалов О и ОН (Н + О2 ОН + О), реакции образования и окисления метанола и диссоциация формальдегида (СН3 + ОН СН3ОН, СН3ОН + О НСНО + Н2О, НСНО Н2 + СО) с образованием водорода и оксида углерода. Далее водород и оксид углерода сгорают по своим цепным механизмам. В отсутствии кислорода идет термическая диссоциация метана с образованием в конечном итоге сажистого углерода (СН4 = 2Н2 + С).
3.3. Распространение пламени
Интенсивность горения неподвижных или ламинарно-движущихся горючих газовых смесей характеризуется нормальной скоростью распространения пламени Un (пламя распространяется по нормали к фронту горения). Рассмотрим процесс распространения пламени в предварительно подготовленной горючей смеси, когда эта смесь движется внутри трубки. В результате начавшегося горения создается фронт пламени толщиной и перемещающийся в направлении движения смеси. Стабилизация фронта пламени наблюдается при равенстве скоростей смеси и противоположно направленной скорости перемещения фронта пламени. Скорость нормального распространения пламени зависит от состава смеси (она максимальна в стехиометрической смеси), от температуры, от вида горючего газа и окислителя и имеет следующие значения: СО + воздух – 0,43 м/с; СН4 + воздух – 0,38 м/с; Н2 + воздух – 2,65 м/с; Н2 + О2 – 13 м/с.
Распространение пламени можно рассматривать как непрерывный процесс прогрессирующего ускорения реакции при прохождении газа через узкую зону пламени в условиях параллельного переноса теплоты теплопроводностью и диффузионного переноса продуктов горения, в том числе активных центров в свежую смесь и свежей смеси в зону горения [10].
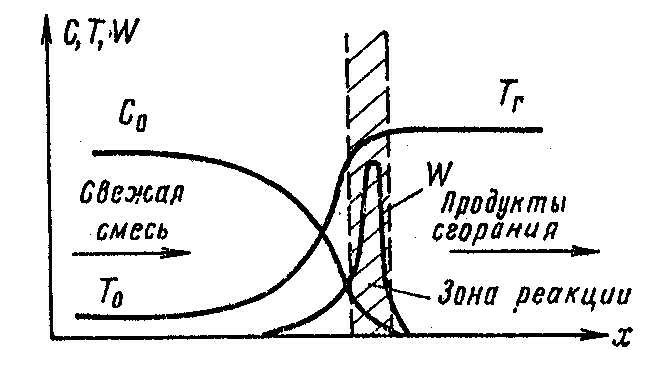
При распространении пламени фронт делит массу газа на две части: впереди – слабо нагретая газовая смесь, позади – сильно нагретые продукты сгорания. В зоне горения температура изменяется от начальной Т0 до температуры горения Тг, при этом уменьшается концентрация горючих веществ от С0 до 0. Скорость реакции зависит от концентрации горючих веществ С и температуры Т, поэтому в зоне пламени она проходит через максимум (увеличивается с повышением температуры и уменьшается по мере уменьшения концентрации горючих). Чем больше скорость химической реакции, тем больше скорость распространения пламени и меньше время пребывания газа в зоне пламени (рис. 3.5).
|
Рис. 3.4. Изменение температуры, концентрации горючих веществ и скорости реакции во фронте пламени
|
|
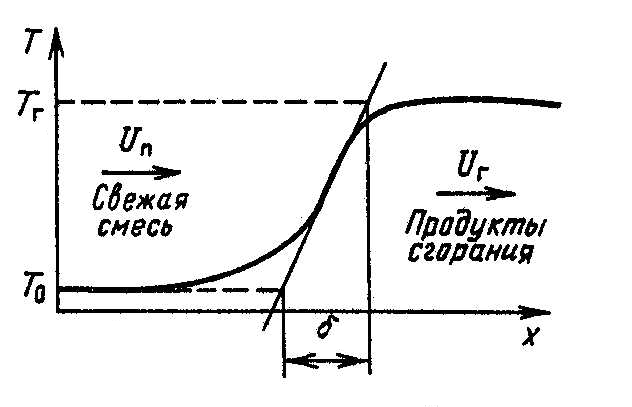
Рис. 3.5. Определение толщины фронта пламени
|
|
|
Заменим
истинное распределение температур
ломаной линией, проведя касательную в
точке перегиба и продолжив до пересечения
с прямым Т0
и Тг.
Расстояние между точками пересечения
– тепловая ширина фронта пламени.
Максимальный градиент температур в
пламени можно представить в виде
![]() .
Поток теплоты из зоны пламени идет на
нагрев свежей смеси теплопроводностью
.
Поток теплоты из зоны пламени идет на
нагрев свежей смеси теплопроводностью
![]() .
С другой стороны, эта теплота затрачивается
на подогрев смеси в количестве ·Un·1
(1 кг/м3· 1м/с 1м2 = 1 кг/с)
от температуры Т0
до Тг:
.
С другой стороны, эта теплота затрачивается
на подогрев смеси в количестве ·Un·1
(1 кг/м3· 1м/с 1м2 = 1 кг/с)
от температуры Т0
до Тг:![]() .
Приравнивая выражения для q,
получим соотношение, связывающее
нормальную скорость распространения
и толщину фронта пламени:
.
Приравнивая выражения для q,
получим соотношение, связывающее
нормальную скорость распространения
и толщину фронта пламени:
![]() ,
(3.8)
,
(3.8)
где a – коэффициент температуропроводности, м2/с.
Опыт показывает, что при нормальном распространении пламени химические реакции протекают в очень тонком слое, отделяющем несгоревшую часть от продуктов сгорания. Толщина фронта пламени даже для медленно горящих смесей составляет доли миллиметров.
Решение уравнений теплопроводности и массопереноса позволяет получить аналитическое выражение для нормальной скорости распространения пламени. Для реакций первого порядка при адиабатных условиях скорость нормального распространения пламени может быть определена по формуле [11]
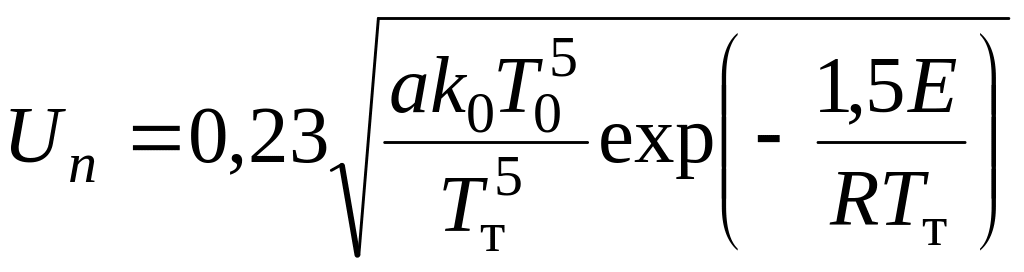 , (3.9)
, (3.9)
где а – коэффициент температуропроводности, м2/с; k0 и Е – предэкспоненциальный множитель и энергия активации уравнения Аррениуса для данной реакции горения, м/с и Дж/моль; Т0 и Тт – начальная и теоретическая температура горения, К; R=8,314 Дж/моль – универсальная газовая постоянная.
Рис.
3.6. Зависимость скорости нормального
распространения пламени от коэффициента
избытка воздуха для смеси метан-воздух
Анализ данного выражения показывает, что скорость нормального распространения пламени, в первую очередь, зависит от энергии активации и теоретической температуры горения. Теоретическая температура горения, в свою очередь, зависит от состава исходной горючей смеси. Максимальная температура горения достигается при коэффициенте избытка воздуха, близком к единице (рис. 3.6), следовательно, и максимальная скорость распространения пламени достигается в стехиометрической смеси. Предварительный подогрев смеси увеличивает Un, так как при этом повышается температура горения. Инертные добавки снижают скорость горения, поскольку при этом снижается температура горения.